Damıtma

Distilasyon veya klasik distilasyon, seçici kaynatma ve yoğunlaştırma kullanarak bileşenleri veya maddeleri sıvı bir karışımdan ayırma işlemidir. Kuru damıtma, gaz halindeki ürünleri (sıvı veya katı olarak yoğunlaşabilen) üretmek için katı maddelerin ısıtılmasıdır. Kuru damıtma, yıkıcı damıtma veya çatlama gibi kimyasal değişiklikler içerebilir ve bu makale kapsamında ele alınmamaktadır. Distilasyon esasen tam ayrıştırma (neredeyse saf bileşenler) ile sonuçlanabilir veya karışımdaki seçilen bileşenlerin konsantrasyonunu artıran kısmi bir ayrıştırma olabilir. Her iki durumda da süreç, karışımın bileşenlerinin göreceli uçuculuğundaki farklılıklardan yararlanır. Endüstriyel uygulamalarda damıtma, pratik olarak evrensel öneme sahip bir birim işlemdir, ancak kimyasal bir reaksiyon değil, fiziksel bir ayırma işlemidir. ⓘ
Distilasyonun birçok uygulaması vardır. Örneğin:
- Fermente ürünlerin damıtılması, yüksek alkol içeriğine sahip damıtılmış içecekler üretir veya ticari değeri olan diğer fermantasyon ürünlerini ayırır.
- Damıtma, tuzdan arındırma için etkili ve geleneksel bir yöntemdir.
- Petrol endüstrisinde, petrol stabilizasyonu, ham petrolün buhar basıncını düşüren, böylece depolama ve taşıma için güvenli hale getiren ve uçucu hidrokarbonların atmosferik emisyonlarını azaltan bir kısmi damıtma şeklidir. Petrol rafinerilerindeki orta akım operasyonlarında, fraksiyonel damıtma, ham petrolün yakıtlara ve kimyasal besleme stoklarına dönüştürülmesi için ana operasyon sınıfıdır.
- Kriyojenik damıtma, havanın endüstriyel kullanım için bileşenlerine (özellikle oksijen, nitrojen ve argon) ayrılmasını sağlar.
- Kimya endüstrisinde, kimyasal sentezin büyük miktarlardaki ham sıvı ürünleri, diğer ürünlerden, safsızlıklardan veya reaksiyona girmemiş başlangıç maddelerinden ayırmak için damıtılır. ⓘ
Özellikle damıtılmış içeceklerin damıtılması için kullanılan bir tesis, bir damıtma tesisidir. Damıtma ekipmanının kendisi bir imbiktir. ⓘ


Damıtma ya da distilasyon, iki veya daha fazla bileşen içeren bir karışımın ısıtılıp, buhar ve sıvı faz oluşturmak suretiyle daha uçucu bileşence zengin karışımların elde edilmesini sağlayan ayırma işlemidir. Ayırma işlemi sırasında, buhar faz daha uçucu olan A bileşeni tarafından zenginleşirken, sıvı faz ise kaynama sıcaklığı daha yüksek olan B bileşenince zenginleşir. Fakat yüzde 100 A içeren bir buhar faz elde edilemez. ⓘ
Diğer bir tanımlama ile; tüm bileşenlerinin uçucu olmak zorunda olduğu, yüksek oranlarda ayırmaya izin veren bir çeşit ayırma işlemidir. İki veya daha fazla bileşenli sıvı karışımlarının ısıtılıp buhar ve sıvı faz oluşturulması suretiyle, daha uçucu bileşence zengin karışımların elde edilmesine denir. ⓘ
Damıtmanın gerçekleştirilebilmesi için temel şart, denge durumuna erişmiş buhar-sıvı sisteminde, buhar fazın sıvı fazdan farklı bileşime sahip olmasıdır. Buhar ve sıvı faz bileşimleri aynı olursa, damıtmada yeterli bir ayırma gerçekleşmez. ⓘ
Damıtma, özellikle organik bileşiklerin saflaştırılması ve ayrılmasında en çok kullanılan yöntemlerden biridir. Kaynama noktasında bulunan bir sıvıya daha fazla ısı verilirse sıvının sıcaklığı artmaz, verilen ısı sıvının buhar haline dönüşmesini sağlar. Sıcaklık, sıvının tamamen buhar halinde uzaklaşmasına kadar sabit kalır. Bu yöntemle buhar basınçları farklı olan sıvılar birbirinden ayrılabilir. ⓘ
Çeşitli parametreler göz önüne alınarak damıtma çeşitlerinin sınıflandırılması mümkündür. Çalışma şekline göre sürekli-kesikli; besleme akımına göre ikili sistem-çoklu sistem; alınan ürün akımının sayısına göre tek akım-çok akım; ayırma işleminde ek besleme akımı kullanılıp kullanılmamasına göre azeotropik-ekstraktif-tuz katkılı; kolon iç yapısına göre raflı kolon-dolgulu kolon gibi sınıflandırmalar mümkündür. Ayrıca riflaks varlığına göre de sınıflandırma söz konusudur. ⓘ
Orta çağ simyacıları; zaç yağı [H2SO4], kezzap [HNO3] ve Tuz ruhu [HCL] gibi maddeleri de damıtma yöntemiyle elde etmişlerdir. ⓘ
Tarihçe

Damıtmanın ilk kanıtları, parfümeri işlemlerini anlatan M.Ö. 1200'lere tarihlenen Akad tabletlerinde bulunmuştur. Bu tabletler, damıtmanın ilkel bir biçiminin eski Mezopotamya'daki Babilliler tarafından bilindiğine dair metinsel kanıtlar sunmaktadır. MS 1. yüzyılda Roma Mısır'ında İskenderiye'de çalışan simyacılarla ilgili olarak da damıtmaya dair erken kanıtlar bulunmuştur. ⓘ
Damıtma işleminin eski Hint alt kıtasında uygulandığı, Pakistan'daki Taxila, Shaikhan Dheri, Charsadda ve Hindistan'daki Rang Mahal'de bulunan ve Ortak Çağ'ın ilk yüzyıllarına tarihlenen pişmiş kil imbiklerden ve alıcılardan anlaşılmaktadır. Allchin bu pişmiş toprak damıtma tüplerinin "bambuyu taklit etmek için yapıldığını" belirtmektedir. Bu "Gandhara imbikleri" sadece çok zayıf likör üretebiliyordu, çünkü düşük ısıda buharları toplamanın etkili bir yolu yoktu. Damıtılmış su, Afrodisiaslı İskender'in süreci tanımladığı MS 200'lerden beri kullanılmaktadır. Diğer sıvıların damıtılmasına yönelik çalışmalar 3. yüzyılda Panopolisli Zosimus yönetimindeki erken Bizans Mısır'ında devam etmiştir. ⓘ
Çin'de damıtma Doğu Han Hanedanlığı döneminde (MS 1.-2. yüzyıllar) başlamış olabilir, ancak arkeolojik kanıtlara göre içeceklerin damıtılması Jin (12.-13. yüzyıllar) ve Güney Song (10.-13. yüzyıllar) hanedanlıklarında başlamıştır. ⓘ
Câbir ibn Hayyân (Latince: Geber, dokuzuncu yüzyıl) ve Ebû Bekir er-Râzî (Latince: Rhazes, yaklaşık 865-925) gibi Ortaçağ Müslüman kimyagerleri çeşitli maddelerin damıtılmasıyla ilgili kapsamlı deneyler yapmışlardır. ⓘ
Şarabın damıtılması Kindî'ye (MS 801-873) ve Fârâbî'ye (MS 872-950) atfedilen Arapça eserlerde ve Zehrâvî'nin (Latince: Abulcasis, 936-1013) Kitâbü't-Tasrîf'inin (daha sonra Liber servatoris olarak Latinceye çevrilmiştir) 28. kitabında yer almaktadır. On ikinci yüzyılda, şarabın tuzla damıtılmasıyla aqua ardens ("yanan su", yani etanol) üretimine ilişkin tarifler bir dizi Latince eserde yer almaya başlamış ve on üçüncü yüzyılın sonunda Batı Avrupalı kimyagerler arasında yaygın olarak bilinen bir madde haline gelmiştir. Taddeo Alderotti'nin (1223-1296) çalışmaları, alkolün konsantre edilmesi için su soğutmalı bir imbikten tekrarlanan damıtmayı içeren ve %90 saflıkta alkol elde edilebilen bir yöntemi tanımlamaktadır. ⓘ
Organik maddelerin fraksiyonel damıtılması, Cremonalı Gerard (yaklaşık 1114-1187) tarafından Liber de septuaginta adıyla Latinceye çevrilen Kitâbü's-Seb'în ("Yetmişin Kitabı") gibi Câbir b. Hayyân'a atfedilen eserlerde önemli bir rol oynar. Cabirilerin hayvansal ve bitkisel maddelerin ve daha az oranda da mineral maddelerin fraksiyonel damıtılmasıyla ilgili deneyleri, yanlışlıkla İbn Sina'ya atfedilen ve Latinceye çevrilerek Roger Bacon (yak. 1220-1292) için en önemli simya kaynağını oluşturacak olan De anima in arte alkimiae adlı Arapça eserin ana konusudur. ⓘ
Çin'in Hebei eyaletinin Qinglong kentindeki bir arkeolojik alanda 12. yüzyıla tarihlenen bir imbik bulunmuştur. Damıtılmış içecekler Yuan hanedanlığı döneminde (13.-14. yüzyıllar) yaygındı. ⓘ
1500 yılında Alman simyacı Hieronymus Braunschweig, yalnızca damıtma konusuna adanmış ilk kitap olan Liber de arte destillandi'yi (Damıtma Sanatı Kitabı) yayınladı ve bunu 1512 yılında çok daha genişletilmiş bir versiyon izledi. 1651'de John French, uygulama üzerine ilk büyük İngilizce derleme olan Damıtma Sanatı'nı yayınladı, ancak bunun çoğunun Braunschweig'ın çalışmasından türetildiği iddia edildi. Bu, operasyonun tezgah ölçeğinden ziyade endüstriyel ölçeğini gösteren, içinde insanların bulunduğu diyagramları içermektedir. ⓘ


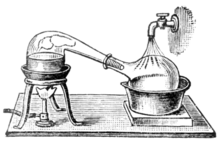


Simya kimya bilimine dönüştükçe, damıtma işlemleri için imbik adı verilen kaplar kullanılmaya başlandı. Hem imbikler hem de imbikler, damıtılan suyu yoğunlaştırmak ve toplamak üzere aşağıya damlamasını sağlamak için hava soğutmalı kondansatör görevi gören, aşağıya doğru bir açıyla yana bakan uzun boyunlu cam kap formlarıdır. Daha sonraları bakır imbikler icat edilmiştir. Perçinli bağlantılar genellikle çeşitli karışımlar, örneğin çavdar unundan yapılmış bir hamur kullanılarak sıkı tutulurdu. Bu imbiklerde genellikle gaga etrafında, örneğin alkolün yoğunlaşmasını daha verimli hale getiren soğuk su kullanan bir soğutma sistemi bulunurdu. Bunlara çömlek imbiği denirdi. Günümüzde imbiklerin ve çömlek imbiklerin yerini çoğu endüstriyel süreçte daha verimli damıtma yöntemleri almıştır. Ancak çömlek imbikleri konyak, İskoç viskisi, İrlanda viskisi, tekila, rom, cachaça ve bazı votkalar gibi bazı kaliteli alkollerin hazırlanmasında hala yaygın olarak kullanılmaktadır. Çeşitli malzemelerden (ahşap, kil, paslanmaz çelik) yapılmış çömlek imbikler de çeşitli ülkelerde kaçakçılar tarafından kullanılmaktadır. Küçük çömlek imbikler de çiçek suyu veya uçucu yağların evde üretiminde kullanılmak üzere satılmaktadır. ⓘ
Damıtmanın ilk biçimleri, bir buharlaştırma ve bir yoğunlaştırma kullanan toplu işlemleri içeriyordu. Saflık, kondensatın daha fazla damıtılmasıyla geliştirilmiştir. Daha büyük hacimler sadece damıtma işleminin tekrarlanmasıyla işleniyordu. Kimyagerlerin saf bir bileşik elde etmek için 500 ila 600 kadar damıtma işlemi gerçekleştirdiği bildirilmektedir. ⓘ
19. yüzyılın başlarında, ön ısıtma ve geri akış da dahil olmak üzere modern tekniklerin temelleri geliştirildi. 1822'de Anthony Perrier ilk sürekli imbiklerden birini geliştirdi ve ardından 1826'da Robert Stein bu tasarımı geliştirerek patentli imbiğini yaptı. 1830'da Aeneas Coffey tasarımı daha da geliştirmek için bir patent aldı. Coffey'in sürekli imbiği modern petrokimya ünitelerinin arketipi olarak kabul edilebilir. Fransız mühendis Armand Savalle 1846 civarında buhar regülatörünü geliştirdi. 1877'de Ernest Solvay'a amonyak distilasyonu için bir tepsi kolonu için ABD Patenti verildi ve aynı ve sonraki yıllarda yağlar ve alkollü içkiler için bu temada gelişmeler görüldü. ⓘ
Kimya mühendisliğinin 19. yüzyılın sonunda bir disiplin olarak ortaya çıkmasıyla birlikte, deneysel yöntemlerden ziyade bilimsel yöntemler uygulanabilir hale gelmiştir. Yirminci yüzyılın başlarında gelişen petrol endüstrisi, Ernest Thiele'nin McCabe-Thiele yöntemi ve Fenske denklemi gibi doğru tasarım yöntemlerinin geliştirilmesine ivme kazandırmıştır. Amerika Birleşik Devletleri'nde okyanusu tuzdan arındırma aracı olarak damıtmayı kullanan ilk endüstriyel tesis, bölgeye su güvenliği getirme umuduyla 1961 yılında Freeport, Teksas'ta açıldı. Güçlü bilgisayarların mevcudiyeti, damıtma kolonlarının doğrudan bilgisayar simülasyonlarına izin vermiştir. ⓘ
Uygulamalar
Damıtma uygulaması kabaca dört gruba ayrılabilir: laboratuvar ölçeği, endüstriyel damıtma, parfümeri ve tıbbi ürünler için bitkilerin damıtılması (bitkisel damıtma) ve gıda işleme. Son ikisi, damıtmanın gerçek bir saflaştırma yöntemi olarak değil, daha çok içeceklerin ve bitkilerin işlenmesinde kaynak malzemelerden tüm uçucuları damıtığa aktarmak için kullanılması nedeniyle ilk ikisinden belirgin bir şekilde farklıdır. ⓘ
Laboratuvar ölçekli distilasyon ile endüstriyel distilasyon arasındaki temel fark, laboratuvar ölçekli distilasyonun genellikle kesikli olarak gerçekleştirilirken, endüstriyel distilasyonun genellikle sürekli olarak gerçekleşmesidir. Kesikli distilasyonda, kaynak malzemenin bileşimi, distilasyon bileşiklerinin buharları ve distilat distilasyon sırasında değişir. Kesikli distilasyonda, bir imbik bir yığın besleme karışımı ile şarj edilir (beslenir), daha sonra bileşen fraksiyonlarına ayrılır, bunlar en uçucudan daha az uçucuya doğru sırayla toplanır ve dip kısımlar - kalan en az veya uçucu olmayan fraksiyon - sonunda çıkarılır. Daha sonra durultucu yeniden şarj edilebilir ve işlem tekrarlanabilir. ⓘ
Sürekli distilasyonda kaynak malzemeler, buharlar ve distilat, kaynak malzemenin dikkatli bir şekilde yenilenmesi ve sistemdeki hem buhar hem de sıvıdan fraksiyonların çıkarılmasıyla sabit bir bileşimde tutulur. Bu, ayırma işleminin daha ayrıntılı bir şekilde kontrol edilmesini sağlar. ⓘ
İdealleştirilmiş model
Bir sıvının kaynama noktası, sıvının buhar basıncının sıvının etrafındaki basınca eşit olduğu ve kabarcıkların ezilmeden oluşmasını sağlayan sıcaklıktır. Özel bir durum, sıvının buhar basıncının ortamdaki atmosfer basıncına eşit olduğu normal kaynama noktasıdır. ⓘ
Belirli bir basınçtaki bir sıvı karışımında, her bileşenin verilen basınca karşılık gelen kaynama noktasında kaynadığı ve her bileşenin buharlarının ayrı ayrı ve saf olarak toplanmasına izin verdiği yanlış bir kanıdır. Ancak, idealize edilmiş bir sistemde bile bu gerçekleşmez. İdealleştirilmiş damıtma modelleri esasen Raoult yasası ve Dalton yasası tarafından yönetilir ve buhar-sıvı dengelerinin sağlandığını varsayar. ⓘ
Raoult yasası, bir çözeltinin buhar basıncının 1) çözeltideki her bir kimyasal bileşenin buhar basıncına ve 2) her bir bileşenin oluşturduğu çözelti fraksiyonuna, diğer bir deyişle mol fraksiyonuna bağlı olduğunu belirtir. Bu yasa ideal çözeltiler veya farklı bileşenlere sahip ancak moleküler etkileşimleri saf çözeltilerle aynı veya çok benzer olan çözeltiler için geçerlidir. ⓘ
Dalton yasası, toplam basıncın karışımdaki her bir bileşenin kısmi basınçlarının toplamı olduğunu belirtir. Çok bileşenli bir sıvı ısıtıldığında, her bir bileşenin buhar basıncı artacak ve böylece toplam buhar basıncının yükselmesine neden olacaktır. Toplam buhar basıncı sıvıyı çevreleyen basınca ulaştığında kaynama meydana gelir ve sıvı, sıvının büyük kısmı boyunca gaza dönüşür. Belirli bir bileşime sahip bir karışım, bileşenler karşılıklı olarak çözündüğünde belirli bir basınçta bir kaynama noktasına sahiptir. Sabit bileşimli bir karışımın birden fazla kaynama noktası yoktur. ⓘ
Tek kaynama noktasının bir anlamı da hafif bileşenlerin asla temiz bir şekilde "önce kaynamamasıdır". Kaynama noktasında tüm uçucu bileşenler kaynar, ancak bir bileşen için buhardaki yüzdesi toplam buhar basıncındaki yüzdesi ile aynıdır. Daha hafif bileşenler daha yüksek kısmi basınca sahiptir ve bu nedenle buharda yoğunlaşır, ancak daha ağır uçucu bileşenler de (daha küçük) bir kısmi basınca sahiptir ve buharda daha düşük bir konsantrasyonda olsa da zorunlu olarak buharlaşır. Aslında, kesikli damıtma ve fraksiyonlama karışımın bileşimini değiştirerek başarılı olur. Kesikli damıtmada karışım buharlaşarak bileşimini değiştirir; fraksiyonlamada ise fraksiyonlama kolonunda daha yüksekte bulunan sıvı daha fazla ışık içerir ve daha düşük sıcaklıklarda kaynar. Bu nedenle, belirli bir karışımdan başlayarak, bir kaynama noktası yerine bir kaynama aralığına sahip gibi görünür, ancak bunun nedeni bileşiminin değişmesidir: her ara karışımın kendi tekil kaynama noktası vardır. ⓘ
İdealize edilmiş model, benzen ve toluen gibi kimyasal olarak benzer sıvılar söz konusu olduğunda doğrudur. Diğer durumlarda, en ünlüsü etanol ve su karışımında olmak üzere, Raoult yasası ve Dalton yasasından ciddi sapmalar gözlenir. Bu bileşikler birlikte ısıtıldıklarında, buhar fazı ve sıvı fazın aynı bileşimi içerdiği bir azeotrop oluştururlar. Rastgele bileşenlerden oluşan bir karışımın davranışını tahmin etmek için kullanılabilecek hesaplama yöntemleri olmasına rağmen, doğru buhar-sıvı dengesi verilerini elde etmenin tek yolu ölçüm yapmaktır. ⓘ
Bir bileşen karışımını damıtma yoluyla tamamen saflaştırmak mümkün değildir, çünkü bu karışımdaki her bileşenin sıfır kısmi basınca sahip olmasını gerektirir. Ultra saf ürünler hedefleniyorsa, daha fazla kimyasal ayırma uygulanmalıdır. İkili bir karışım buharlaştırıldığında ve diğer bileşen, örneğin bir tuz, pratik amaçlar için sıfır kısmi basınca sahip olduğunda, işlem daha basittir. ⓘ
Kesikli veya diferansiyel distilasyon

A ve B gibi iki uçucu maddenin ideal bir karışımını, A daha yüksek uçuculuğa veya daha düşük kaynama noktasına sahip olacak şekilde, karışım kaynayana kadar bir kesikli damıtma düzeneğinde (açılış resminde gösterilen aparat gibi) ısıtmak, sıvının üzerinde A ve B karışımı içeren bir buharla sonuçlanır. Sıvıdaki oran orijinal karışımın nasıl hazırlandığına göre belirlenirken, buhardaki oran daha uçucu olan A bileşiği açısından zenginleşecektir (Raoult Kanunu nedeniyle, yukarıya bakın). Buhar kondansatörden geçer ve sistemden uzaklaştırılır. Bu da, kalan sıvıdaki bileşik oranının artık başlangıçtaki orandan farklı olduğu anlamına gelir (yani, B'de başlangıç sıvısına göre daha fazla zenginleşir). ⓘ
Bu da karışımın kaynama noktasının yükselmesine, buharın sıcaklığının artmasına ve gaz fazındaki A : B oranının değişmesine neden olur (damıtma devam ettikçe gaz fazındaki B oranı artar). Bu da damıtıkta yavaşça değişen bir A : B oranıyla sonuçlanır. ⓘ
İki A ve B bileşeni arasındaki buhar basıncı farkı büyükse - genellikle kaynama noktaları farkı olarak ifade edilir - damıtmanın başlangıcındaki karışım A bileşeninde oldukça zenginleşir ve A bileşeni damıtıldığında, kaynayan sıvı B bileşeninde zenginleşir. ⓘ
Sürekli damıtma
Sürekli distilasyon, bir sıvı karışımının sürekli olarak (kesintisiz) prosese beslendiği ve operasyon sırasında zaman içinde çıkış akışları meydana geldikçe ayrılan fraksiyonların sürekli olarak çıkarıldığı devam eden bir distilasyondur. Sürekli damıtma, kaynatılmış ve ayrı olarak buhar olarak yakalanmış ve daha sonra bir sıvıya yoğunlaştırılmış en az bir uçucu damıtma fraksiyonu dahil olmak üzere en az iki çıkış fraksiyonu üretir. Her zaman bir dip (veya kalıntı) fraksiyonu vardır, bu da yoğunlaştırılmış bir buhar olarak ayrı olarak yakalanmamış en az uçucu kalıntıdır. ⓘ
Sürekli distilasyon, konsantrasyonların zaman içinde değişmemesi açısından kesikli distilasyondan farklıdır. Sürekli distilasyon keyfi bir süre boyunca sabit bir durumda çalıştırılabilir. Belirli bileşimdeki herhangi bir kaynak malzeme için, sürekli damıtmada ürünlerin saflığını etkileyen ana değişkenler, pratikte tepsi sayısı veya salmastra yüksekliği ile belirlenen geri akış oranı ve teorik denge aşamalarının sayısıdır. Reflü, kondansatörden kolona geri akış olup, belirli sayıda tepsi ile daha iyi bir ayrıştırma sağlayan bir geri dönüşüm oluşturur. Denge aşamaları, bileşimlerin buhar-sıvı dengesine ulaştığı, ayırma işlemini tekrarlayan ve bir geri akış oranı verildiğinde daha iyi ayırmaya izin veren ideal adımlardır. Yüksek geri akış oranına sahip bir kolon daha az aşamaya sahip olabilir, ancak büyük miktarda sıvıyı geri akıtır ve büyük bir tutma ile geniş bir kolon verir. Tersine, düşük reflü oranına sahip bir kolon çok sayıda kademeye sahip olmalıdır, bu da daha uzun bir kolon gerektirir. ⓘ
Genel iyileştirmeler
Hem kesikli hem de sürekli distilasyonlar, distilasyon şişesinin üstünde bir fraksiyonlama kolonu kullanılarak geliştirilebilir. Kolon, buhar ve kondensatın temas etmesi için daha geniş bir yüzey alanı sağlayarak ayırmayı iyileştirir. Bu, mümkün olduğunca uzun süre dengede kalmasına yardımcı olur. Kolon, her biri kendi buhar-sıvı dengesine sahip, zenginleştirilmiş, kaynayan bir sıvı karışımı içeren küçük alt sistemlerden ('tepsiler' veya 'tabaklar') bile oluşabilir. ⓘ
Laboratuvar ölçekli ve endüstriyel ölçekli fraksiyonlama kolonları arasında farklılıklar vardır, ancak prensipler aynıdır. Laboratuvar ölçekli fraksiyonlama kolonlarının örnekleri (artan verimlilikte) şunları içerir
- Hava kondansatörü
- Vigreux kolonu (genellikle sadece laboratuvar ölçeğinde)
- Paketlenmiş kolon (cam boncuklar, metal parçalar veya kimyasal olarak inert diğer malzemelerle paketlenmiş)
- Eğirme bandı distilasyon sistemi. ⓘ
Laboratuvar prosedürleri
Laboratuvar ölçekli distilasyonlar neredeyse sadece kesikli distilasyonlar olarak yürütülür. Damıtmada kullanılan ve bazen imbik olarak da adlandırılan cihaz, en azından kaynak maddenin ısıtıldığı bir yeniden kaynatıcı veya kazan, ısıtılmış buharın tekrar sıvı hale soğutulduğu bir yoğunlaştırıcı ve damıtık olarak adlandırılan konsantre veya saflaştırılmış sıvının toplandığı bir alıcıdan oluşur. Damıtma için çeşitli laboratuvar ölçekli teknikler mevcuttur (ayrıca bakınız damıtma türleri). ⓘ
Tamamen kapalı bir damıtma aparatı aşırı ve hızla değişen iç basınçla karşılaşabilir ve bu da bağlantı yerlerinden patlayarak açılmasına neden olabilir. Bu nedenle, iç basıncın atmosferik basınçla eşitlenmesine izin vermek için genellikle bazı yollar açık bırakılır (örneğin, alıcı şişede). Alternatif olarak, aparatı atmosferik basınçtan daha düşük bir basınçta tutmak için bir vakum pompası kullanılabilir. İlgili maddeler havaya veya neme duyarlıysa, atmosferle bağlantı, istenmeyen hava bileşenlerini temizleyen malzemelerle dolu bir veya daha fazla kurutma tüpü veya hareketli bir sıvı bariyeri sağlayan kabarcıklar aracılığıyla yapılabilir. Son olarak, istenmeyen hava bileşenlerinin girişi, aparata nitrojen gibi uygun bir inert gazın düşük ama sabit bir akışı pompalanarak önlenebilir. ⓘ
Basit damıtma

Basit damıtmada buhar hemen bir yoğunlaştırıcıya yönlendirilir. Sonuç olarak distilat saf değildir, aksine bileşimi verilen sıcaklık ve basınçtaki buharların bileşimiyle aynıdır. Bu konsantrasyon Raoult yasasını takip eder. ⓘ
Sonuç olarak, basit damıtma yalnızca sıvıların kaynama noktaları büyük ölçüde farklı olduğunda (temel kural 25 °C'dir) veya sıvıları uçucu olmayan katılardan veya yağlardan ayırırken etkilidir. Bu durumlarda, bileşenlerin buhar basınçları genellikle distilatın amaçlanan amaç için yeterince saf olabilmesini sağlayacak kadar farklıdır. ⓘ
Basit bir damıtma işleminin kesit şeması sağda gösterilmektedir. Kaynatma şişesi 2'deki başlangıç sıvısı 15, bir silikon yağ banyosu (turuncu, 14) aracılığıyla kombine bir ocak gözü ve manyetik karıştırıcı 13 ile ısıtılır. Buhar kısa bir Vigreux kolonundan 3, ardından bir Liebig kondansatöründen 5 akar, 6 ve 7 numaralı portlardan dolaşan su (mavi) ile soğutulur. Yoğunlaşan sıvı, bir soğutma banyosunda (mavi, 16) bulunan alıcı şişeye 8 damlar. Adaptör 10, bir vakum pompasına takılabilen bir bağlantıya 9 sahiptir. Bileşenler buzlu cam bağlantılarla bağlanmıştır. ⓘ
Fraksiyonel distilasyon
Birçok durumda, karışımdaki bileşenlerin kaynama noktaları Raoult yasasının dikkate alınmasını gerektirecek kadar yakın olacaktır. Bu nedenle, bileşenleri paketlenmiş bir fraksiyonlama kolonu içinde tekrarlanan buharlaşma-yoğuşma döngüleri ile ayırmak için fraksiyonel distilasyon kullanılmalıdır. Ardışık damıtmalarla yapılan bu ayırma işlemi rektifikasyon olarak da adlandırılır. ⓘ
Saflaştırılacak çözelti ısıtıldıkça, buharları fraksiyonlama kolonuna yükselir. Yükseldikçe soğur, kondansatör duvarlarında ve salmastra malzemesinin yüzeylerinde yoğunlaşır. Burada kondensat, yükselen sıcak buharlar tarafından ısıtılmaya devam eder; bir kez daha buharlaşır. Ancak, taze buharların bileşimi bir kez daha Raoult yasası tarafından belirlenir. Her buharlaşma-yoğunlaşma döngüsü (teorik plaka olarak adlandırılır) daha uçucu bileşenin daha saf bir çözeltisini verecektir. Gerçekte, belirli bir sıcaklıktaki her döngü fraksiyonlama kolonunda tam olarak aynı konumda gerçekleşmez; teorik plaka bu nedenle doğru bir tanımdan ziyade bir kavramdır. ⓘ
Daha fazla teorik plaka daha iyi ayrımlara yol açar. Dönen bant distilasyon sistemi, yükselen buharları inen kondensat ile yakın temasa zorlamak için teflon veya metalden dönen bir bant kullanır ve teorik plakaların sayısını artırır. ⓘ
Buhar distilasyonu
Vakum distilasyonu gibi buhar distilasyonu da ısıya duyarlı bileşiklerin distilasyonu için kullanılan bir yöntemdir. Buharın sıcaklığını kontrol etmek bir ısıtma elemanının yüzeyini kontrol etmekten daha kolaydır ve çok yüksek bir sıcaklıkta ısıtma yapmadan yüksek oranda ısı transferine izin verir. Bu işlem, ham maddenin ısıtılmış bir karışımı boyunca buharın kabarcıklandırılmasını içerir. Raoult yasasına göre, hedef bileşiğin bir kısmı buharlaşacaktır (kısmi basıncına uygun olarak). Buhar karışımı soğutulur ve yoğunlaştırılır, genellikle bir yağ tabakası ve bir su tabakası elde edilir. ⓘ
Çeşitli aromatik bitki ve çiçeklerin buhar distilasyonu iki ürünle sonuçlanabilir; uçucu bir yağ ve sulu bir bitkisel distilat. Uçucu yağlar genellikle parfümeri ve aromaterapide kullanılırken, sulu distilatların aromaterapi, gıda işleme ve cilt bakımında birçok uygulaması vardır. ⓘ


- Karıştırıcı çubuk/çarpma önleyici granüller
- Hala tencere
- Fraksiyonlama kolonu
- Termometre/Kaynama noktası sıcaklığı
- Teflon musluk 1
- Soğuk parmak
- Soğutma suyu çıkışı
- Soğutma suyu içinde
- Teflon musluk 2
- Vakum/gaz girişi
- Teflon musluk 3
- Hala alıcı ⓘ
Vakum distilasyonu
Bazı bileşiklerin kaynama noktaları çok yüksektir. Bu tür bileşikleri kaynatmak için, sıcaklığı artırmak yerine bu tür bileşiklerin kaynatıldığı basıncı düşürmek genellikle daha iyidir. Basınç bileşiğin buhar basıncına düşürüldüğünde (verilen sıcaklıkta), kaynama ve damıtma işleminin geri kalanı başlayabilir. Bu teknik vakum distilasyonu olarak adlandırılır ve laboratuvarda yaygın olarak döner buharlaştırıcı şeklinde bulunur. ⓘ
Bu teknik, atmosferik basınçta ayrışma sıcaklığının ötesinde kaynayan ve bu nedenle atmosferik basınç altında kaynatılmaya çalışıldığında ayrışacak olan bileşikler için de çok kullanışlıdır. ⓘ
Kısa yol ve moleküler distilasyon
Moleküler distilasyon, 0,01 torr basıncın altında vakumlu distilasyondur. 0,01 torr, sıvıların serbest moleküler akış rejiminde olduğu, yani moleküllerin ortalama serbest yolunun ekipmanın boyutuyla karşılaştırılabilir olduğu yüksek vakumun bir büyüklük sırasıdır. Gaz fazı artık buharlaştırılacak madde üzerinde önemli bir basınç uygulamaz ve sonuç olarak buharlaşma hızı artık basınca bağlı değildir. Yani, akışkan dinamiğinin süreklilik varsayımları artık geçerli olmadığından, kütle taşınımı akışkan dinamiğinden ziyade moleküler dinamik tarafından yönetilir. Bu nedenle, sıcak yüzey ile soğuk yüzey arasında kısa bir yol gereklidir, tipik olarak bir besleme filmi ile kaplı bir sıcak plaka, aralarında bir görüş hattı bulunan bir soğuk plakanın yanına asılır. Moleküler damıtma, yağların saflaştırılması için endüstriyel olarak kullanılmaktadır. ⓘ

- Karıştırıcı çubuklu/çarpma önleyici granüllü durultma kabı
- Soğuk parmak - yoğuşmayı yönlendirmek için bükülmüş
- Soğutma suyu çıkışı
- soğutma suyu
- Vakum/gaz girişi
- Damıtma şişesi/distilat. ⓘ
Kısa yol distilasyonu, distilatın genellikle sadece birkaç santimetre olmak üzere kısa bir mesafe kat etmesini içeren ve normalde düşük basınçta yapılan bir distilasyon tekniğidir. Klasik bir örnek, iki hazneyi ayıran bir kondansatöre ihtiyaç duymadan, distilatın bir cam ampulden diğerine geçmesini içeren bir distilasyon olabilir. Bu teknik genellikle yüksek sıcaklıklarda kararsız olan bileşikler için veya az miktarda bileşiği saflaştırmak için kullanılır. Bunun avantajı, ısıtma sıcaklığının (düşük basınçta) sıvının standart basınçtaki kaynama noktasından çok daha düşük olabilmesi ve damıtılan maddenin yoğunlaşmadan önce sadece kısa bir mesafe kat etmek zorunda olmasıdır. Kısa bir yol, aparatın kenarlarında çok az bileşik kaybı olmasını sağlar. Kugelrohr aparatı, distilat fraksiyonlarını toplamak için genellikle birden fazla hazne içeren bir tür kısa yol distilasyon yöntemidir. ⓘ
Havaya duyarlı vakum distilasyonu
Bazı bileşikler havaya duyarlı olmalarının yanı sıra yüksek kaynama noktalarına sahiptir. Yukarıda örneklendiği gibi basit bir vakum distilasyon sistemi kullanılabilir; bu sistemde distilasyon tamamlandıktan sonra vakum inert bir gazla değiştirilir. Ancak, fraksiyonların düşük basınç altında toplanması isteniyorsa bu daha az tatmin edici bir sistemdir. Bunu yapmak için kondansatörün ucuna bir "inek" veya "domuz" adaptörü eklenebilir veya daha iyi sonuçlar için veya havaya çok duyarlı bileşikler için Perkin üçgen aparatı kullanılabilir. ⓘ
Perkin üçgeni, bir dizi cam veya Teflon musluk aracılığıyla, damıtmanın ana gövdesi vakumdan veya ısı kaynağından çıkarılmadan fraksiyonların durultucunun geri kalanından izole edilmesini sağlayan ve böylece geri akış durumunda kalabilen araçlara sahiptir. Bunu yapmak için, numune önce musluklar vasıtasıyla vakumdan izole edilir, numune üzerindeki vakum daha sonra inert bir gazla (nitrojen veya argon gibi) değiştirilir ve daha sonra durdurulabilir ve çıkarılabilir. Daha sonra sisteme yeni bir toplama kabı eklenebilir, boşaltılabilir ve ikinci bir fraksiyonu toplamak için musluklar aracılığıyla distilasyon sistemine geri bağlanabilir ve tüm fraksiyonlar toplanana kadar bu şekilde devam eder. ⓘ
Bölge distilasyonu
Bölge distilasyonu, uzun bir kapta, hareketli sıvı bölgede rafine maddenin kısmi erimesi ve soğuk bölgede kondensat çekiminde katı fazdaki buharın yoğunlaşması ile gerçekleşen bir distilasyon işlemidir. Proses teorik olarak çalışmaktadır. Bölge ısıtıcısı kabın üstünden altına doğru hareket ettiğinde, düzensiz kirlilik dağılımına sahip katı kondensat oluşur. Daha sonra kondensatın en saf kısmı ürün olarak çıkarılabilir. İşlem, alınan kondensatın kabın alt kısmına rafine madde yerine taşınmasıyla (devirsiz) birçok kez tekrarlanabilir. Kondensattaki düzensiz safsızlık dağılımı (yani saflaştırma verimliliği) iterasyon sayısı ile artar. Bölge distilasyonu, bölge yeniden kristalizasyonunun distilasyon analoğudur. Kondensattaki safsızlık dağılımı, damıtmanın ayırma faktörü α için kristalleşmenin dağılım katsayısı k'nın değiştirilmesiyle bilinen bölge yeniden kristalleşme denklemleri ile tanımlanır. ⓘ
Kapalı sistem vakum distilasyonu (kriyovap)
Yoğuşmayan gaz, ilk pompalama sırasında kendiliğinden buharlaşan nispeten uçucu yardımcı çözücünün buharı ile aparattan dışarı atılabilir ve bu normal yağ veya diyaframlı pompa ile sağlanabilir. ⓘ
Diğer tipler
- Reaktif distilasyon prosesi, reaksiyon kabının imbik olarak kullanılmasını içerir. Bu proseste, ürün genellikle reaktanlarından önemli ölçüde daha düşük kaynama noktasındadır. Reaktanlardan ürün oluştukça buharlaştırılır ve reaksiyon karışımından uzaklaştırılır. Bu teknik, kesikli prosese karşı sürekli prosese bir örnektir; avantajları arasında reaksiyon kabını başlangıç malzemesiyle doldurmak için daha az duruş süresi ve daha az çalışma yer alır. "Reaktan üzerinden" damıtma reaktif damıtma olarak sınıflandırılabilir. Tipik olarak distilasyon beslemesinden uçucu safsızlığı gidermek için kullanılır. Örneğin, karbondioksiti sudan uzaklaştırmak için biraz kireç eklenebilir ve ardından amonyak izlerini gidermek için biraz sülfürik asit eklenmiş ikinci bir damıtma yapılabilir.
- Katalitik distilasyon, ürünleri reaktanlardan sürekli olarak ayırmak için distile edilirken reaktanların katalize edildiği prosestir. Bu yöntem, denge reaksiyonlarının tamamlanmasına yardımcı olmak için kullanılır.
- Pervaporasyon, sıvı karışımlarının gözeneksiz bir membrandan kısmi buharlaştırma yoluyla ayrılması için kullanılan bir yöntemdir.
- Ekstraktif distilasyon, karışımdaki diğer bileşenlerle azeotrop oluşturmayan, karışabilir, yüksek kaynama noktalı, nispeten uçucu olmayan bir bileşen olan çözücü varlığında distilasyon olarak tanımlanır.
- Flaş buharlaştırma (veya kısmi buharlaştırma), doymuş bir sıvı akışı bir kısma vanasından veya başka bir kısma cihazından geçerek basınçta bir azalmaya uğradığında meydana gelen kısmi buharlaşmadır. Bu işlem en basit birim işlemlerden biridir ve sadece bir denge aşamasına sahip bir damıtmaya eşdeğerdir.
- Kodistilasyon, iki bileşiğin karışabilir olmadığı karışımlar üzerinde gerçekleştirilen damıtmadır. Laboratuvarda, Dean-Stark aparatı sentez ürünlerinden suyu uzaklaştırmak için bu amaçla kullanılır. Bleidner aparatı, iki geri akışlı çözücü içeren başka bir örnektir.
- Membran distilasyonu, ayrıştırılacak bir karışımın buharlarının, karışımın bir bileşenini seçici olarak geçiren bir membrandan geçirildiği bir distilasyon türüdür. Buhar basıncı farkı itici güçtür. Deniz suyunun tuzdan arındırılmasında ve organik ve inorganik bileşenlerin giderilmesinde potansiyel uygulamaları vardır. ⓘ
Birim buharlaştırma işlemi "damıtma" olarak da adlandırılabilir:
- Döner buharlaştırmada, bir numuneden toplu çözücüleri çıkarmak için bir vakum damıtma aparatı kullanılır. Vakum tipik olarak bir su aspiratörü veya bir membran pompası tarafından oluşturulur.
- Bir Kugelrohr aparatında, yüksek kaynama noktalı (> 300 °C) bileşikleri damıtmak için tipik olarak (genellikle (yüksek) vakumla birlikte) kısa yollu bir damıtma aparatı kullanılır. Cihaz, damıtılacak bileşiğin içine yerleştirildiği bir fırın, fırının dışında bulunan bir alıcı kısım ve numuneyi döndüren bir araçtan oluşur. Vakum normalde yüksek vakum pompası kullanılarak oluşturulur. ⓘ
Diğer kullanımlar:
- Kuru damıtma veya yıkıcı damıtma, ismine rağmen, gerçek anlamda damıtma değil, piroliz olarak bilinen ve katı maddelerin inert veya indirgeyici bir atmosferde ısıtıldığı ve yüksek kaynama noktalı sıvılar ve piroliz ürünleri içeren uçucu fraksiyonların toplandığı kimyasal bir reaksiyondur. Metanol elde etmek için ahşabın tahrip edici damıtılması, yaygın adı olan odun alkolünün köküdür.
- Dondurarak damıtma, buharlaştırma yerine dondurmayı kullanan benzer bir saflaştırma yöntemidir. Gerçek anlamda damıtma değil, ürünün ana likör olduğu ve damıtmaya eşdeğer ürünler üretmeyen bir yeniden kristalleştirmedir. Bu işlem, sırasıyla etanol ve şeker içeriğini artırmak için buzlu bira ve buzlu şarap üretiminde kullanılır. Ayrıca applejack üretmek için de kullanılır. Damıtmanın aksine, dondurarak damıtma zehirli konjenerleri uzaklaştırmak yerine yoğunlaştırır; Sonuç olarak, birçok ülke sağlık önlemi olarak bu tür applejack'i yasaklamaktadır. Ayrıca, buharlaştırma yoluyla damıtma, farklı kaynama noktalarına sahip oldukları için bunları ayırabilir.
- Filtrasyon yoluyla damıtma: Doğa felsefesi olarak da bilinen erken dönem simya ve kimyada, kılcal filtrasyon yoluyla "damıtma" o zamanlar bir damıtma biçimi olarak biliniyordu. Bu yöntemde bir dizi fincan ya da kase, su ya da berrak bir sıvı ile ıslatılmış pamuk ya da keçe benzeri bir malzemeden bir "fitil" ile basamaklı bir destek üzerine yerleştirilir ve her adımda ıslatılmış bezden aşağıya doğru kılcal hareket yoluyla damlayarak sıvıda bir "saflaştırma" yaratır, üst kaselerde katı maddeleri geride bırakır ve nemlendirilmiş bezden kılcal hareket yoluyla sonraki ürünü saflaştırırdı. Bu, yöntemi kullananlar tarafından filtreleme yoluyla "distillatio" olarak adlandırılmıştır. ⓘ
Azeotropik süreç
Çözeltinin bileşenleri arasındaki etkileşimler, Raoult yasasının geçerli olmadığı çoğu süreçte ideal olmayan karışımlar gerektirdiğinden, çözeltiye özgü özellikler yaratır. Bu tür etkileşimler, saf bir bileşikmiş gibi davranan (yani, bir aralık yerine tek bir sıcaklıkta kaynayan) sabit kaynama noktalı bir azeotrop ile sonuçlanabilir. Bir azeotropta, çözelti verilen bileşeni buharla aynı oranda içerir, böylece buharlaşma saflığı değiştirmez ve damıtma ayırmayı etkilemez. Örneğin, etil alkol ve su 78,1 °C'de %95,6'lık bir azeotrop oluşturur. ⓘ
Azeotropun kullanım için yeterince saf olmadığı düşünülüyorsa, saf bir distilat elde etmek üzere azeotropu kırmak için bazı teknikler mevcuttur. Bu teknikler azeotropik distilasyon olarak bilinir. Bazı teknikler bunu azeotropik bileşimin üzerinden "atlayarak" gerçekleştirir (yeni bir azeotrop oluşturmak için başka bir bileşen ekleyerek veya basıncı değiştirerek). Diğerleri ise kimyasal ya da fiziksel olarak safsızlığı gidererek ya da tutarak çalışır. Örneğin, etanolü %95'in üzerinde saflaştırmak için, çözünür suyu çözünmeyen kristalizasyon suyuna dönüştürmek üzere bir kurutma maddesi (veya potasyum karbonat gibi kurutucu) eklenebilir. Moleküler elekler de genellikle bu amaç için kullanılır. ⓘ
Su ve toluen gibi karışmayan sıvılar kolayca azeotrop oluşturur. Genellikle bu azeotroplar düşük kaynama noktalı azeotrop olarak adlandırılır çünkü azeotropun kaynama noktası her iki saf bileşenin kaynama noktasından daha düşüktür. Azeotropun sıcaklığı ve bileşimi, Raoult yasası kullanılmadan saf bileşenlerin buhar basıncından kolayca tahmin edilebilir. Azeotrop, bir damıtma düzeneğinde, üstte yoğunlaşan iki sıvı tabakayı ayırmak için bir sıvı-sıvı ayırıcı (bir dekantör) kullanılarak kolayca kırılır. İki sıvı katmandan yalnızca biri damıtma düzeneğine geri akıtılır. ⓘ
Su içinde ağırlıkça yüzde 20 hidroklorik asit karışımı gibi yüksek kaynama noktalı azeotroplar da mevcuttur. Adından da anlaşılacağı üzere, azeotropun kaynama noktası, saf bileşenlerden herhangi birinin kaynama noktasından daha yüksektir. ⓘ
DeRosier Probleminde olduğu gibi azeotropik damıtmaları kırmak ve damıtma sınırlarını aşmak için damıtıktaki hafif anahtarın bileşimini artırmak gerekir. ⓘ
Tek yönlü basınç manipülasyonu ile bir azeotropun kırılması
Bir azeotrop içindeki bileşenlerin kaynama noktaları bir bant oluşturmak üzere üst üste biner. Bir azeotropu vakuma veya pozitif basınca maruz bırakarak, her birinin farklı buhar basıncı eğrilerinden yararlanarak bir bileşenin kaynama noktasını diğerinden uzaklaştırmak mümkündür; eğriler azeotropik noktada üst üste gelebilir, ancak azeotropik noktanın her iki tarafındaki basınç ekseni boyunca aynı kalması olası değildir. Sapma yeterince büyük olduğunda, iki kaynama noktası artık örtüşmez ve böylece azeotropik bant kaybolur. ⓘ
Bu yöntem bir damıtmaya başka kimyasallar ekleme ihtiyacını ortadan kaldırabilir, ancak iki potansiyel dezavantajı vardır. ⓘ
Negatif basınç altında vakum kaynağı için güç gerekir ve distilatların kaynama noktalarının azalması, distilat buharlarının vakum kaynağına kaybolmasını önlemek için kondansatörün daha soğuk çalıştırılmasını gerektirir. Artan soğutma talepleri genellikle ek enerji ve muhtemelen yeni ekipman veya soğutma sıvısı değişikliği gerektirecektir. ⓘ
Alternatif olarak, pozitif basınç gerekiyorsa, standart cam eşyalar kullanılamaz, basınçlandırma için enerji kullanılması gerekir ve kaynamayı gerçekleştirmek için gereken daha yüksek sıcaklıklar nedeniyle distilasyonda ayrışma gibi yan reaksiyonların meydana gelme olasılığı daha yüksektir. ⓘ
Tek yönlü bir damıtma, pozitif veya negatif olmak üzere tek yönde bir basınç değişimine dayanacaktır. ⓘ
Basınç salınımlı damıtma
Basınç salınımlı distilasyon esasen azeotropik karışımları kırmak için kullanılan tek yönlü distilasyonla aynıdır, ancak burada hem pozitif hem de negatif basınçlar kullanılabilir. ⓘ
Bu, damıtmanın seçiciliğini artırır ve bir kimyagerin enerji israfına neden olan aşırı basınç ve sıcaklıklardan kaçınarak damıtmayı optimize etmesine olanak tanır. Bu özellikle ticari uygulamalarda önemlidir. ⓘ
Basınç salınımlı damıtma uygulamasının bir örneği, etil asetatın etanolden katalitik sentezinden sonra endüstriyel saflaştırılması sırasında görülür. ⓘ
Endüstriyel proses

Büyük ölçekli endüstriyel distilasyon uygulamaları hem kesikli hem de sürekli fraksiyonel, vakum, azeotropik, ekstraktif ve buhar distilasyonunu içerir. Sürekli, kararlı durum fraksiyonel distilasyonun en yaygın kullanılan endüstriyel uygulamaları petrol rafinerileri, petrokimya ve kimya tesisleri ve doğal gaz işleme tesisleridir. ⓘ
Bu tür endüstriyel damıtmayı kontrol etmek ve optimize etmek için standartlaştırılmış bir laboratuvar yöntemi olan ASTM D86 oluşturulmuştur. Bu test yöntemi, petrol ürünlerinin kaynama aralığı özelliklerini nicel olarak belirlemek için bir laboratuvar kesikli damıtma ünitesi kullanarak petrol ürünlerinin atmosferik damıtılmasını kapsar. ⓘ
Endüstriyel distilasyon tipik olarak distilasyon kuleleri veya distilasyon kolonları olarak bilinen, çapları yaklaşık 0,65 ila 16 metre (2 ft 2 inç ila 52 ft 6 inç) ve yükseklikleri yaklaşık 6 ila 90 metre (20 ila 295 ft) veya daha fazla olan büyük, dikey silindirik kolonlarda gerçekleştirilir. Ham petrolün damıtılmasında olduğu gibi proses beslemesi farklı bir bileşime sahip olduğunda, kolon boyunca aralıklarla bulunan sıvı çıkışları farklı kaynama noktalarına veya kaynama aralıklarına sahip farklı fraksiyonların veya ürünlerin çekilmesini sağlar. "En hafif" ürünler (en düşük kaynama noktasına sahip olanlar) kolonların üst kısmından çıkar ve "en ağır" ürünler (en yüksek kaynama noktasına sahip olanlar) kolonun alt kısmından çıkar ve genellikle dip kısım olarak adlandırılır. ⓘ
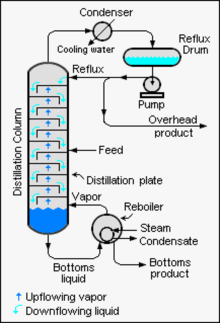
Endüstriyel kuleler, ürünlerin daha eksiksiz bir şekilde ayrılmasını sağlamak için reflü kullanır. Reflü, tipik, büyük ölçekli bir endüstriyel distilasyon kulesinin şematik diyagramında gösterildiği gibi, bir distilasyon veya fraksiyonlama kulesinden gelen yoğunlaştırılmış üst sıvı ürünün kulenin üst kısmına geri gönderilen kısmını ifade eder. Kulenin içinde, aşağı akan reflü sıvısı yukarı akan buharların soğutulmasını ve yoğunlaştırılmasını sağlayarak damıtma kulesinin verimliliğini arttırır. Belirli bir teorik plaka sayısı için ne kadar çok geri akış sağlanırsa, kulenin düşük kaynama noktalı maddeleri yüksek kaynama noktalı maddelerden ayırması o kadar iyi olur. Alternatif olarak, istenen belirli bir ayırma için ne kadar fazla reflü sağlanırsa, gereken teorik plaka sayısı o kadar az olur. Kimya mühendisleri, distilasyon kolonunda saflaştırılan ürünler için hangi reflü oranı ve plaka sayısı kombinasyonunun hem ekonomik hem de fiziksel olarak uygun olduğunu seçmelidir. ⓘ
Bu tür endüstriyel fraksiyonlama kuleleri, sıvı oksijen, sıvı nitrojen ve yüksek saflıkta argon üreten kriyojenik hava ayrıştırmada da kullanılır. Klorosilanların damıtılması, yarı iletken olarak kullanılmak üzere yüksek saflıkta silikon üretimini de sağlar. ⓘ
Bir damıtma kulesinin tasarımı ve işletimi beslemeye ve istenen ürünlere bağlıdır. Basit, ikili bileşenli bir besleme söz konusu olduğunda McCabe-Thiele yöntemi veya Fenske denklemi gibi analitik yöntemler kullanılabilir. Çok bileşenli bir besleme için, hem tasarım hem de işletim için simülasyon modelleri kullanılır. Ayrıca, distilasyon kulelerinde kullanılan buhar-sıvı temas cihazlarının ("plakalar" veya "tepsiler" olarak adlandırılır) verimleri tipik olarak teorik %100 verimli denge aşamasından daha düşüktür. Bu nedenle, bir damıtma kulesi teorik buhar-sıvı denge aşamalarının sayısından daha fazla tepsiye ihtiyaç duyar. Tepsi verimliliklerini tahmin etmek için çeşitli modeller öne sürülmüştür. ⓘ
Modern endüstriyel kullanımlarda, kolon boyunca düşük basınç düşüşleri gerektiğinde tepsiler yerine kolonda bir salmastra malzemesi kullanılır. Salmastrayı tercih eden diğer faktörler şunlardır: vakum sistemleri, daha küçük çaplı kolonlar, aşındırıcı sistemler, köpürmeye eğilimli sistemler, düşük sıvı tutma gerektiren sistemler ve kesikli damıtma. Buna karşılık, plakalı kolonları tercih eden faktörler şunlardır: beslemede katı madde bulunması, yüksek sıvı hızları, büyük kolon çapları, karmaşık kolonlar, geniş besleme bileşimi varyasyonuna sahip kolonlar, kimyasal reaksiyonlu kolonlar, absorpsiyon kolonları, temel ağırlık toleransı ile sınırlı kolonlar, düşük sıvı hızı, büyük geri dönüş oranı ve proses dalgalanmalarına maruz kalan prosesler. ⓘ

Bu salmastra malzemesi Raschig halkaları gibi rastgele dökülmüş salmastralar (25-76 milimetre (1-3 inç) genişliğinde) ya da yapılandırılmış sac metal olabilir. Sıvılar salmastranın yüzeyini ıslatma eğilimindedir ve buharlar kütle transferinin gerçekleştiği bu ıslatılmış yüzeyden geçer. Her bir tepsinin ayrı bir buhar-sıvı denge noktasını temsil ettiği geleneksel tepsi distilasyonunun aksine, dolgulu bir kolondaki buhar-sıvı denge eğrisi süreklidir. Bununla birlikte, dolgulu kolonlar modellenirken, daha geleneksel tepsilere göre dolgulu kolonun ayırma verimliliğini belirtmek için bir dizi "teorik aşama" hesaplamak yararlıdır. Farklı şekillerdeki ambalajlar farklı yüzey alanlarına ve ambalajlar arasında farklı boşluk alanlarına sahiptir. Bu faktörlerin her ikisi de ambalaj performansını etkiler. ⓘ
Salmastra şekli ve yüzey alanına ek olarak rastgele veya yapılandırılmış salmastranın performansını etkileyen bir diğer faktör de salmastralı yatağa giren sıvı ve buhar dağılımıdır. Belirli bir ayrıştırma yapmak için gereken teorik aşama sayısı, belirli bir buhar/sıvı oranı kullanılarak hesaplanır. Sıvı ve buhar, dolgulu yatağa girerken yüzeysel kule alanı boyunca eşit olarak dağılmazsa, dolgulu yatakta sıvı-buhar oranı doğru olmayacak ve gerekli ayırma sağlanamayacaktır. Salmastra düzgün çalışmıyor gibi görünecektir. Teorik bir plakaya eşdeğer yükseklik (HETP) beklenenden daha büyük olacaktır. Sorun salmastranın kendisinde değil, dolgulu yatağa giren sıvıların yanlış dağılımındadır. Sıvıların yanlış dağılımı buhardan daha sık karşılaşılan bir sorundur. Dolgulu yatağa besleme ve geri akış sağlamak için kullanılan sıvı dağıtıcıların tasarımı, salmastranın maksimum verimlilikte çalışması için kritik öneme sahiptir. Dolgulu yatağa giren sıvıyı eşit bir şekilde dağıtmak için bir sıvı dağıtıcının etkinliğini değerlendirme yöntemleri referanslarda bulunabilir. Bu konuda Fractionation Research, Inc. (genellikle FRI olarak bilinir) tarafından önemli çalışmalar yapılmıştır. ⓘ
Çok etkili distilasyon
Çok etkili damıtmanın amacı, tuzdan arındırmada veya bazı durumlarda ultra saf su üretiminde bir aşamada kullanılmak üzere prosesin enerji verimliliğini artırmaktır. Etki sayısı, kW-h/m3 geri kazanılan su rakamıyla ters orantılıdır ve tek etkili damıtma ile karşılaştırıldığında birim enerji başına geri kazanılan su hacmini ifade eder. Bir etki yaklaşık 636 kW-h/m3'tür.
- Çok aşamalı flaş damıtma, makalede belirtildiği gibi termal enerji girdisi ile 20'den fazla etki elde edebilir.
- Buhar sıkıştırmalı buharlaştırma - Üreticilere göre ticari büyük ölçekli üniteler elektrik enerjisi girdisiyle yaklaşık 72 etki elde edebilir. ⓘ
Aralarında ısı eşanjörlerinin bulunduğu birden fazla haznenin kullanıldığı ve basitçe çok etkili damıtma (MED) olarak adlandırılan bir proses de dahil olmak üzere çok etkili damıtma proseslerinin başka birçok türü vardır. ⓘ
Gıda işlemede
İçecekler
Karbonhidrat içeren bitki materyalleri mayalanmaya bırakılır ve bu süreçte seyreltik bir etanol çözeltisi üretilir. Viski ve rom gibi alkollü içkiler bu seyreltik etanol çözeltilerinin damıtılmasıyla hazırlanır. Su, esterler ve diğer alkoller de dahil olmak üzere etanol dışındaki bileşenler, içeceğin lezzetini oluşturan yoğuşma suyunda toplanır. Bu içeceklerden bazıları daha sonra daha fazla aroma bileşiği ve karakteristik tatlar elde etmek için fıçılarda veya diğer kaplarda saklanır. ⓘ
Galeri
 |
Kimyanın başlangıcında imbikler yalnızca damıtma işlemleri için laboratuvar ekipmanı olarak kullanılıyordu. ⓘ |
 |
Kuru ve oksijensiz toluen damıtmak için basit bir kurulum. |
 |
Petrol rafinerilerinde yaygın olarak kullanılan endüstriyel ölçekli bir vakum damıtma kolonunun şeması |
 |
Döner buharlaştırıcı, vakum kullanarak çözücüleri daha düşük sıcaklıklarda daha hızlı bir şekilde damıtabilir. |
 |
Yarı mikro ölçekli aparat kullanarak damıtma. Eklemsiz tasarım, parçaları birbirine takma ihtiyacını ortadan kaldırır. Armut şeklindeki şişe, benzer büyüklükteki yuvarlak tabanlı şişeye kıyasla kalıntının son damlasına kadar alınmasını sağlar. Küçük tutma hacmi kayıpları önler. Çeşitli damıtıkları üç alıcı şişeye kanalize etmek için bir "domuz" kullanılır. Gerekirse damıtma işlemi pig'deki vakum adaptörü kullanılarak vakum altında gerçekleştirilebilir. |
Türleri
Normal atmosfer basıncında yapılan damıtma türleri
- Normal damıtma: Kaynama sıcaklığına yakın sıcaklıklarda bozunmayan maddelere uygulanır.
- Fraksiyonlu damıtma: Kaynama noktaları birbirine yakın maddelerin ayrılmasında kullanılır.
- Su buharı damıtması: Suda çözünmeyen ve miktarı az olan maddeleri uçucu olmayan karışımlardan ayırmak için özellikle madde 100 oC nin üzerinde kaynıyorsa ve kaynama noktasına yakın sıcaklıklarda bozunuyorsa su buharı destilasyonu kullanılır. Kaynama sıcaklıklarının altında bozunabilen maddeler için de kullanılır.
- Kuru damıtma: Katı maddelerin ısı etkisiyle parçalanıp distile edilebilir maddeler vermesi ve bunların distile edilmesi esasına dayanır. En büyük sakıncası katı maddelerin ısıyı iyi iletmemesi ve parçalanma sonucu istenmeyen ürünlerin de oluşmasıdır.çalışma şekli normal distilasyonda olduğu gibidir.Ayırma ve saflaştırmadan çok sentez tekniği ( örneğin keton sentezi ) olarak önem taşır. ⓘ
Normal atmosfer basıncından düşük basınçlarda yapılan distilasyon türü
- Vakum damıtması: Kaynama sıcaklıklarının altında bozunabilen maddeler için kullanılır. Maddeler bir vakum içerisinde damıtılır.
| Kimya ile ilgili bu madde taslak seviyesindedir. Madde içeriğini genişleterek Vikipedi'ye katkı sağlayabilirsiniz. ⓘ |
