Entalpi
| Termodinamik ⓘ |
|---|
 |
|
Entalpi, maddenin yapısında depoladığı her türden enerjilerin toplamıdır. H ile simgelenir. Bir mol maddede depolanmış enerjiye o maddenin molar entalpisi denir. ⓘ
Maddelerin kesin entalpilerinin hesaplanması çok zordur. Bu yüzden çoğu çalışmalarda entalpi değeri olarak, maddenin değiştirilebilen ısı potansiyelinin kapsadığı termal entalpileri kullanılır. Bu entalpi değeri maddenin sıfır derece Kelvin sıcaklıktan mevcut sıcaklığına yükseltilmesi için yüklenen ısılarla faz değiştirme ısılarının toplamına eşittir. ⓘ
Kimyasal tepkimelerde, girenlerle ürünler arasındaki fark belirlenir. Ürünlerin entalpileri toplamı ile girenlerin entalpileri toplamı arasındaki farka, tepkimenin entalpi değişimi ya da tepkime entalpisi adı verilir ve ∆H ile simgelenir. ∆H değerleri - ve + olabilir bu tepkimenin ısıveren veya ısıalan olduğunu belirler. Termodinamikte ısı ve işin toplamına eşittir. Maddenin fiziksel haline, sıcaklık ve basınca, madde miktarına bağlı olarak değişebilir. Formülsel olarak "H = U + Pv" şeklinde ifade edilir. U maddenin iç enerjisi, Pv ise maddenin toplam sahip olduğu potansiyel enerjiyi gösterir. ⓘ
Her kimyasal tepkimede az ya da çok ısı alınır ya da verilir. Sabit basınç altında, kimyasal bir tepkimede açığa çıkan ya da alınan ısıya tepkime entalpisi denir. Sabit hacimde fiziksel değişim ikiye ayrılır: endoterm ve ekzoterm. Ekzotermik tepkimeler ısı veren tepkimelerdir, endotermik tepkimeler ise ısı alan tepkimelerdir. ⓘ
Entalpi; madde miktarına, maddenin fiziksel haline, basınca ve ortamın sıcaklığına bağlıdır. ∆H: (+) işaretli ise ya da ∆H > 0 ise olay endotermiktir. ∆H: (-) işaretli ise ya da ∆H < 0 ise olay ekzotermiktir. ⓘ
| Kimya ile ilgili bu madde taslak seviyesindedir. Madde içeriğini genişleterek Vikipedi'ye katkı sağlayabilirsiniz. |
| Termodinamik ile ilgili bu madde taslak seviyesindedir. Madde içeriğini genişleterek Vikipedi'ye katkı sağlayabilirsiniz. ⓘ |
Entalpi /ˈɛnθəlpi/ (![]() listen), termodinamik bir sistemin özelliği olup, sistemin iç enerjisi ile basınç ve hacminin çarpımının toplamıdır. Kimyasal, biyolojik ve fiziksel sistemlerde, geniş ortam atmosferi tarafından uygun bir şekilde sağlanan sabit bir basınçta yapılan birçok ölçümde kullanılan bir durum fonksiyonudur. Basınç-hacim terimi, sistemin fiziksel boyutlarını oluşturmak için, yani çevresini yer değiştirerek ona yer açmak için gereken işi ifade eder. Basınç-hacim terimi genel koşullarda katılar ve sıvılar için çok küçük, gazlar için ise oldukça küçüktür. Bu nedenle entalpi, kimyasal sistemlerdeki enerjinin yerine geçer; bağ, kafes, çözünme ve kimyadaki diğer "enerjiler" aslında entalpi farklarıdır. Bir durum fonksiyonu olarak entalpi, yalnızca iç enerji, basınç ve hacmin nihai konfigürasyonuna bağlıdır, buna ulaşmak için izlenen yola değil. ⓘ
listen), termodinamik bir sistemin özelliği olup, sistemin iç enerjisi ile basınç ve hacminin çarpımının toplamıdır. Kimyasal, biyolojik ve fiziksel sistemlerde, geniş ortam atmosferi tarafından uygun bir şekilde sağlanan sabit bir basınçta yapılan birçok ölçümde kullanılan bir durum fonksiyonudur. Basınç-hacim terimi, sistemin fiziksel boyutlarını oluşturmak için, yani çevresini yer değiştirerek ona yer açmak için gereken işi ifade eder. Basınç-hacim terimi genel koşullarda katılar ve sıvılar için çok küçük, gazlar için ise oldukça küçüktür. Bu nedenle entalpi, kimyasal sistemlerdeki enerjinin yerine geçer; bağ, kafes, çözünme ve kimyadaki diğer "enerjiler" aslında entalpi farklarıdır. Bir durum fonksiyonu olarak entalpi, yalnızca iç enerji, basınç ve hacmin nihai konfigürasyonuna bağlıdır, buna ulaşmak için izlenen yola değil. ⓘ
Uluslararası Birimler Sisteminde (SI) entalpi için ölçü birimi joule'dür. Halen kullanılmakta olan diğer tarihsel geleneksel birimler arasında kalori ve İngiliz ısı birimi (BTU) bulunmaktadır. ⓘ
Bir sistemin toplam entalpisi doğrudan ölçülemez çünkü iç enerji bilinmeyen, kolayca erişilemeyen veya termodinamiğin ilgi alanına girmeyen bileşenler içerir. Pratikte, entalpideki değişim sabit basınçtaki ölçümler için tercih edilen ifadedir çünkü enerji transferinin tanımını basitleştirir. Sistemin içine veya dışına madde transferi de engellendiğinde ve hiçbir elektrik veya şaft işi yapılmadığında, sabit basınçta entalpi değişimi çevreyle ısı yoluyla değiş tokuş edilen enerjiye eşittir. ⓘ
Kimyada, standart reaksiyon entalpisi, standart durumlarındaki reaktanların (p = 1 bar; genellikle T = 298 K) standart durumlarındaki ürünlere dönüştüğü zamanki entalpi değişimidir. Bu miktar, sabit basınç ve sıcaklıktaki standart reaksiyon ısısıdır, ancak ilk ve son basınç ve sıcaklığın standart duruma karşılık gelmesi koşuluyla, ölçüm sırasında sıcaklık değişse bile kalorimetrik yöntemlerle ölçülebilir. Entalpi bir durum fonksiyonu olduğu için değer ilk durumdan son duruma giden yola bağlı değildir. ⓘ
Kimyasal maddelerin entalpileri genellikle standart durum olarak 1 bar (100 kPa) basınç için listelenir. Reaksiyonlar için entalpiler ve entalpi değişimleri sıcaklığın bir fonksiyonu olarak değişir, ancak tablolar genellikle maddelerin 25 °C'deki (298 K) standart oluşum ısılarını listeler. Endotermik (ısı emen) süreçler için ΔH değişimi pozitif bir değerdir; ekzotermik (ısı salan) süreçler için negatiftir. ⓘ
İdeal bir gazın entalpisi, basıncından veya hacminden bağımsızdır ve yalnızca termal enerjisiyle ilişkili olan sıcaklığına bağlıdır. Yaygın sıcaklık ve basınçlardaki gerçek gazlar genellikle bu davranışa yakındır, bu da pratik termodinamik tasarım ve analizi basitleştirir. ⓘ
Tanım
Termodinamik bir sistemin entalpisi H, iç enerjisi ile basınç ve hacminin çarpımının toplamı olarak tanımlanır:
- H = U + pV,
Burada U iç enerji, p basınç ve V sistemin hacmidir; p.V bazen basınç enerjisi ƐP olarak da adlandırılır. ⓘ
Entalpi kapsamlı bir özelliktir; sistemin büyüklüğü ile orantılıdır (homojen sistemler için). Yoğun özellikler olarak, özgül entalpi h = H/m, sistemin m kütle birimine atıfta bulunur ve molar entalpi Hm, H/n'dir, burada n mol sayısıdır. Homojen olmayan sistemler için entalpi, bileşen alt sistemlerin entalpilerinin toplamıdır:
- H, tüm alt sistemlerin toplam entalpisidir,
- k çeşitli alt sistemleri ifade eder,
- Hk her bir alt sistemin entalpisini ifade eder. ⓘ
Kapalı bir sistem statik bir yerçekimi alanında termodinamik dengede olabilir, böylece basıncı p yükseklikle sürekli değişirken, denge gereksinimi nedeniyle sıcaklığı T yükseklikle değişmez. (Buna bağlı olarak, sistemin yerçekimsel potansiyel enerji yoğunluğu da rakımla değişir). O zaman entalpi toplamı bir integral haline gelir:
- ρ ("rho") yoğunluktur (birim hacim başına kütle),
- h özgül entalpidir (birim kütle başına entalpi),
- (ρh) entalpi yoğunluğunu (birim hacim başına entalpi) temsil eder,
- dV, sistem içindeki sonsuz küçük bir hacim öğesini, örneğin sonsuz ince bir yatay katmanın hacmini ifade eder, bu nedenle integral, hacmin tüm öğelerinin entalpilerinin toplamını temsil eder. ⓘ
Kapalı homojen bir sistemin entalpisi, entropisi S[p] ve basıncı p doğal durum değişkenleri olarak aşağıdaki gibi türetilen en basit formdaki dH için bir diferansiyel ilişki sağlayan enerji fonksiyonu H(S,p)'dir. Sonsuz küçük bir süreç için kapalı sistemler için termodinamiğin birinci yasasından başlıyoruz:
- 𝛿Q sisteme eklenen küçük bir ısı miktarıdır,
- 𝛿W sistem tarafından gerçekleştirilen küçük bir iş miktarıdır. ⓘ
Sadece tersinir süreçlerin veya saf ısı transferinin dikkate alındığı homojen bir sistemde, termodinamiğin ikinci yasası 𝛿Q = T dS değerini verir; T mutlak sıcaklık ve dS sistemin entropisindeki S sonsuz küçük değişimdir. Ayrıca, yalnızca pV iş yapılırsa, 𝛿W = p dV olur. Sonuç olarak, ⓘ
Bu ifadenin her iki tarafına d(pV) eklendiğinde
Bu yüzden
Diğer ifadeler
Yukarıdaki dH'nin entropi ve basınç cinsinden ifadesi bazı okuyuculara yabancı gelebilir. Sıcaklık ve basınç gibi daha doğrudan ölçülebilir değişkenler cinsinden ifadeler de vardır:
Burada Cp sabit basınçtaki ısı kapasitesi, α ise (kübik) termal genleşme katsayısıdır:
Bu ifade ile, prensip olarak, Cp ve V p ve T'nin fonksiyonları olarak biliniyorsa entalpi belirlenebilir. Çünkü T, H entalpisi için doğal bir değişken değildir. ⓘ
Sabit basınçta, dP = 0 olduğundan İdeal bir gaz için, süreç bir basınç değişikliği içerse bile dH bu forma indirgenir, çünkü αT = 1,. ⓘ
Daha genel bir formda, birinci yasa iç enerjiyi kimyasal potansiyel ve çeşitli tiplerdeki parçacıkların sayısını içeren ek terimlerle tanımlar. Bu durumda dH için diferansiyel ifade şöyle olur ⓘ
Burada μi, i-tipi bir parçacık için parçacık başına kimyasal potansiyeldir ve Ni bu tür parçacıkların sayısıdır. Son terim μi dni (dni sisteme eklenen i bileşeninin mol sayısı ve bu durumda μi molar kimyasal potansiyel) veya μi dmi (dmi sisteme eklenen i bileşeninin kütlesi ve bu durumda μi spesifik kimyasal potansiyel) olarak da yazılabilir. ⓘ
Karakteristik fonksiyonlar ve doğal durum değişkenleri
Entalpi, H(S[p], p, {Ni}), bir sistemin termodinamiğini enerji gösteriminde ifade eder. Bir durum fonksiyonu olarak, argümanları hem bir yoğun hem de birkaç kapsamlı durum değişkenini içerir. S[p], p ve {Ni} durum değişkenlerinin bu gösterimde doğal durum değişkenleri olduğu söylenir. Çevredeki faktörler tarafından belirlendikleri süreçleri tanımlamak için uygundurlar. Örneğin, sanal bir atmosferik hava parseli farklı bir yüksekliğe hareket ettiğinde, onu çevreleyen basınç değişir ve süreç genellikle o kadar hızlıdır ki ısı transferi için çok az zaman vardır. Bu, meteorolojide kullanılan adyabatik yaklaşımın temelidir. ⓘ
Entalpi ile eşlenik olarak, bu argümanlarla, termodinamik bir sistemin durumunun diğer karakteristik fonksiyonu, entropinin, S[p](H, p, {Ni}), aynı durum değişkenleri listesinin bir fonksiyonu olarak, entropinin, S[p], listede entalpi, H ile değiştirilmesi dışında, entropi temsilini ifade eder. H, p ve {Ni} durum değişkenlerinin bu gösterimde doğal durum değişkenleri olduğu söylenir. Deneysel olarak kontrol edildikleri süreçleri tanımlamak için uygundurlar. Örneğin, H ve p ısı transferine izin verilerek ve sadece sistemin hacmini belirleyen piston üzerindeki dış basınç değiştirilerek kontrol edilebilir. ⓘ
Fiziksel yorumlama
U terimi sistemin enerjisidir ve pV terimi, ortamın basıncının sabit kalması halinde sisteme "yer açmak" için gerekli olan iş olarak yorumlanabilir. Bir sistem, örneğin p basıncında ve T sıcaklığında V hacmindeki bir gazın n molü yaratıldığında veya mutlak sıfırdan mevcut durumuna getirildiğinde, iç enerjisi U artı pV'ye eşit enerji sağlanmalıdır; burada pV, ortam (atmosfer) basıncına karşı itme sırasında yapılan iştir. ⓘ
Fizik ve istatistiksel mekanikte sabit hacimli bir sistemin iç özelliklerini incelemek daha ilginç olabilir ve bu nedenle iç enerji kullanılır. Kimyada, deneyler genellikle sabit atmosfer basıncında yapılır ve basınç-hacim işi atmosferle küçük, iyi tanımlanmış bir enerji alışverişini temsil eder, böylece ΔH reaksiyon ısısı için uygun ifadedir. Bir ısı motoru için, tam bir çevrimden sonra entalpisindeki değişim sıfıra eşittir, çünkü son ve ilk durum eşittir. ⓘ
Isı ile ilişki
Entalpi artışı ve ısı kaynağı arasındaki ilişkiyi tartışmak için, kapalı sistemler için birinci yasaya dönüyoruz, fizik işaret konvansiyonu ile: dU = δQ - δW, burada δQ ısısı iletim, radyasyon, Joule ısıtması ile sağlanır. Bunu, yüzeyde sabit bir basıncın olduğu özel duruma uygulayacağız. Bu durumda iş p dV ile verilir (burada p yüzeydeki basınç, dV ise sistemin hacmindeki artıştır). Uzun menzilli elektromanyetik etkileşim durumları, formülasyonlarında daha fazla durum değişkeni gerektirir ve burada ele alınmamıştır. Bu durumda birinci yasa şu şekildedir:
Şimdi,
Bu yüzden
Sistem sabit basınç altındaysa, dp = 0 olur ve sonuç olarak sistemin entalpisindeki artış eklenen ısıya eşit olur:
Bu nedenle 19. yüzyılda artık kullanılmayan ısı içeriği terimi kullanılmıştır. ⓘ
Uygulamalar
Termodinamikte entalpi, "hiçlikten" bir sistem yaratmak için gerekenleri belirleyerek hesaplanabilir; gereken mekanik iş, pV, termodinamik sistemin yaratılması sırasında ortaya çıkan koşullara göre farklılık gösterir. ⓘ
P basıncının sabit kaldığı varsayılarak, sistemin oluşturulması için yer açmak üzere çevreden parçacıkları uzaklaştırmak için enerji sağlanmalıdır; bu pV terimidir. Sağlanan enerji aynı zamanda aktivasyon enerjilerini, iyonlaşma enerjilerini, karışım enerjilerini, buharlaşma enerjilerini, kimyasal bağ enerjilerini ve benzerlerini içeren iç enerjideki U değişimini de sağlamalıdır. Bunlar birlikte entalpi U + pV'deki değişimi oluşturur. Sabit basınçtaki sistemler için, pV işi dışında harici bir iş yapılmadığında, entalpideki değişim sistem tarafından alınan ısıdır. ⓘ
Sabit basınçta sabit sayıda parçacık içeren basit bir sistem için entalpi farkı, izobarik termodinamik bir süreçten elde edilebilecek maksimum termal enerji miktarıdır. ⓘ
Reaksiyon ısısı
Bir sistemin toplam entalpisi doğrudan ölçülemez; bunun yerine bir sistemin entalpi değişimi ölçülür. Entalpi değişimi aşağıdaki denklemle tanımlanır:
- ΔH "entalpi değişimi "dir,
- Hf, sistemin nihai entalpisidir (kimyasal bir reaksiyonda, ürünlerin veya denge halindeki sistemin entalpisi),
- Hi sistemin başlangıç entalpisidir (kimyasal bir reaksiyonda, reaktanların entalpisi). ⓘ
Sabit basınçta ekzotermik bir reaksiyon için, sistemin entalpi değişimi, ΔH, reaksiyon ürünlerinin reaktanlardan daha küçük bir entalpiye sahip olması nedeniyle negatiftir ve herhangi bir elektrik veya şaft işi yapılmazsa reaksiyonda açığa çıkan ısıya eşittir. Başka bir deyişle, entalpideki genel düşüş ısı üretimi ile sağlanır. Tersine, sabit basınçlı endotermik bir reaksiyon için ΔH pozitiftir ve reaksiyonda emilen ısıya eşittir. ⓘ
Entalpi H = U + pV olarak tanımlandığında, sabit basınçtaki entalpi değişimi ΔH = ΔU + p ΔV olur. Ancak çoğu kimyasal reaksiyon için p ΔV iş terimi, yaklaşık olarak ΔH'ye eşit olan ΔU iç enerji değişiminden çok daha küçüktür. Örnek olarak, karbon monoksit 2 CO(g) + O2(g) → 2 CO2(g) yanması için, ΔH = -566,0 kJ ve ΔU = -563,5 kJ'dir. Farklar çok küçük olduğu için, reaksiyon entalpileri genellikle reaksiyon enerjileri olarak tanımlanır ve bağ enerjileri açısından analiz edilir. ⓘ
Spesifik entalpi
Düzgün bir sistemin özgül entalpisi h = H/m olarak tanımlanır, burada m sistemin kütlesidir. Özgül entalpi için SI birimi kilogram başına joule'dür. Diğer spesifik miktarlarda h = u + pv ile ifade edilebilir, burada u spesifik iç enerji, p basınç ve v spesifik hacimdir, bu da 1/ρ'ye eşittir, burada ρ yoğunluktur. ⓘ
Entalpi değişimleri
Entalpi değişimi, bir dönüşüm veya kimyasal reaksiyon geçiren termodinamik bir sistemin bileşenlerinde gözlemlenen entalpi değişimini tanımlar. Süreç tamamlandıktan sonraki entalpi, yani reaksiyonun tamamlandığı varsayılarak ürünlerin entalpisi ile sistemin, yani reaktanların başlangıç entalpisi arasındaki farktır. Bu süreçler yalnızca ilk ve son durumları ile belirtilir, böylece tersi için entalpi değişimi ileri süreç için olanın negatifidir. ⓘ
Yaygın bir standart entalpi değişimi, çok sayıda madde için belirlenmiş olan oluşum entalpisidir. Entalpi değişimleri rutin olarak ölçülür ve CRC Handbook of Chemistry and Physics gibi kimyasal ve fiziksel referans çalışmalarında derlenir. Aşağıda termodinamikte yaygın olarak tanınan entalpi değişimlerinden bir seçki verilmiştir. ⓘ
Bu tanınmış terimler kullanıldığında genellikle değişim niteleyicisi atılır ve özellik basitçe 'proses entalpisi' olarak adlandırılır. Bu özellikler genellikle referans değerler olarak kullanıldığından, standartlaştırılmış bir dizi çevresel parametre veya standart koşullar için alıntı yapmak çok yaygındır:
- Bir atmosfer (1 atm veya 101.325 kPa) veya 1 bar basınç
- 25 °C veya 298,15 K sıcaklık
- Element veya bileşik çözelti içinde bulunduğunda 1,0 M'lık bir konsantrasyon
- Normal fiziksel durumlarındaki elementler veya bileşikler, yani standart durum
Bu tür standartlaştırılmış değerler için entalpi adının önüne genellikle standart terimi eklenir, örneğin standart oluşum entalpisi. ⓘ
Kimyasal özellikler:
- Tepkime entalpisi, bir mol madde tamamen tepkimeye girdiğinde termodinamik sistemin bir bileşeninde gözlenen entalpi değişimi olarak tanımlanır.
- Oluşum entalpisi, bir bileşiğin bir molü temel öncüllerinden oluştuğunda termodinamik sistemin bir bileşeninde gözlenen entalpi değişimi olarak tanımlanır.
- Yanma entalpisi, bir maddenin bir molü oksijenle tamamen yandığında termodinamik sistemin bir bileşeninde gözlenen entalpi değişimi olarak tanımlanır.
- Hidrojenasyon entalpisi, doymamış bir bileşiğin bir molü fazla hidrojenle tamamen reaksiyona girerek doymuş bir bileşik oluşturduğunda termodinamik sistemin bir bileşeninde gözlenen entalpi değişimi olarak tanımlanır.
- Atomlaşma entalpisi, bir maddenin bir molünü kendisini oluşturan atomlara tamamen ayırmak için gereken entalpi değişimi olarak tanımlanır.
- Nötralizasyon entalpisi, bir asit ve bir baz reaksiyona girdiğinde bir mol su oluştuğunda termodinamik bir sistemin bir bileşeninde gözlemlenen entalpi değişimi olarak tanımlanır.
- Standart Çözelti Entalpisi, bir mol çözünen madde fazla miktarda çözücü içinde tamamen çözündüğünde termodinamik sistemin bir bileşeninde gözlenen entalpi değişimi olarak tanımlanır, böylece çözelti sonsuz seyreltide olur.
- Standart Denatürasyon entalpisi (biyokimya), bir mol bileşiği denatüre etmek için gereken entalpi değişimi olarak tanımlanır.
- Hidrasyon entalpisi, bir mol gaz iyonu suda tamamen çözünerek bir mol sulu iyon oluşturduğunda gözlemlenen entalpi değişimi olarak tanımlanır. ⓘ
Fiziksel özellikler:
- Füzyon entalpisi, bir mol maddenin durumunu katıdan sıvıya tamamen değiştirmek için gereken entalpi değişimi olarak tanımlanır.
- Buharlaşma entalpisi, bir mol maddenin halini sıvıdan gaza tamamen değiştirmek için gereken entalpi değişimi olarak tanımlanır.
- Süblimleşme entalpisi, bir mol maddenin halini katıdan gaza tamamen değiştirmek için gereken entalpi değişimi olarak tanımlanır.
- Kafes entalpisi, iyonik bir bileşiğin bir molünü birbirinden sonsuz uzaklıkta (yani çekim kuvveti olmadan) ayrılmış gaz iyonlarına ayırmak için gereken enerji olarak tanımlanır.
- Karıştırma entalpisi, iki (reaksiyona girmeyen) kimyasal maddenin karıştırılması üzerine entalpi değişimi olarak tanımlanır. ⓘ
Açık sistemler
Termodinamik açık sistemlerde, kütle (maddelerin) sistem sınırlarının içine ve dışına akabilir. Açık sistemler için termodinamiğin birinci yasası şöyle der: Bir sistemin iç enerjisindeki artış, sisteme giren kütle ve ısınma yoluyla eklenen enerji miktarından, dışarı akan kütle ve sistem tarafından yapılan iş yoluyla kaybedilen miktarın çıkarılmasına eşittir:
Burada Uin sisteme giren ortalama iç enerji, Uout ise sistemden çıkan ortalama iç enerjidir. ⓘ

Açık sistemin sınırları tarafından çevrelenen uzay bölgesine genellikle kontrol hacmi denir ve fiziksel duvarlara karşılık gelebilir veya gelmeyebilir. Kontrol hacminin şeklini, içeri veya dışarı tüm akış yüzeyine dik olacak şekilde seçersek, sisteme giren kütle akışı, kütleyi sisteme iten bir akışkan pistonu gibi iş yapar ve sistem, kütlenin dışarı akışı üzerinde, sanki bir akışkan pistonunu tahrik ediyormuş gibi iş yapar. Bu durumda yapılan iki tür iş vardır: yukarıda açıklanan ve akışkan üzerinde yapılan akış işi (buna genellikle pV işi de denir) ve türbin veya pompa gibi bazı mekanik cihazlarda yapılabilen şaft işi. ⓘ
Bu iki iş türü denklemde ifade edilir
Kontrol hacmi (cv) için yukarıdaki denklemde yerine koyma sonucu elde edilir:
Entalpi tanımı, H, bu termodinamik potansiyeli açık sistemler için akışkanlarda hem iç enerji hem de pV işini hesaba katmak için kullanmamıza izin verir:
Sistem sınırının da hareket etmesine izin verirsek (örneğin hareket eden pistonlar nedeniyle), açık sistemler için birinci yasanın oldukça genel bir biçimini elde ederiz. Zaman türevleri açısından şöyle okunur:
ısının sağlandığı, kütlenin sisteme aktığı ve sınırların hareket ettiği çeşitli k yerleri üzerindeki toplamlarla. Ḣk terimleri entalpi akışlarını temsil eder ve şu şekilde yazılabilir ⓘ
ṁk sırasıyla k konumundaki kütle akışı ve ṅk molar akış. dVk/dt terimi, k konumundaki sistem hacminin değişim oranını temsil eder ve bu da sistem tarafından yapılan pV gücüyle sonuçlanır. P parametresi, şaft gücü gibi sistem tarafından yapılan diğer tüm güç biçimlerini temsil eder, ancak örneğin bir elektrik santrali tarafından üretilen elektrik gücü de olabilir. ⓘ
Önceki ifadenin yalnızca kinetik enerji akış hızı sistem girişi ve çıkışı arasında korunuyorsa geçerli olduğunu unutmayın. Aksi takdirde, entalpi dengesine dahil edilmesi gerekir. Bir cihazın kararlı durum çalışması sırasında (bkz. türbin, pompa ve motor), ortalama dU/dt sıfıra eşit olarak ayarlanabilir. Bu, kimyasal reaksiyonların olmadığı durumlarda bu cihazların ortalama güç üretimi için kullanışlı bir ifade verir:
Burada köşeli parantezler zaman ortalamalarını gösterir. Entalpinin teknik önemi, yukarıda formüle edildiği gibi açık sistemler için birinci yasadaki varlığıyla doğrudan ilişkilidir. ⓘ
Diyagramlar

Önemli maddelerin entalpi değerleri ticari yazılımlar kullanılarak elde edilebilir. Pratik olarak tüm ilgili malzeme özellikleri ya tablo halinde ya da grafik olarak elde edilebilir. Çeşitli basınçlar için sıcaklığın fonksiyonu olarak özgül entalpiyi veren h-T diyagramları ve çeşitli T için p'nin fonksiyonu olarak h'yi veren h-p diyagramları gibi birçok diyagram türü vardır. Erime eğrisini ve doymuş sıvı ve buhar değerlerini izobarlar ve izentalplerle birlikte verir. Bu diyagramlar, ısı mühendisinin elindeki güçlü araçlardır. ⓘ
Bazı temel uygulamalar
Şekildeki a'dan h'ye kadar olan noktalar bu bölümdeki tartışmada rol oynamaktadır.
Nokta !T (K) !p (bar) !s (kJ/(kg K)) !h (kJ/kg) a 300 1 6.85 461 b 380 2 6.85 530 c 300 200 5.16 430 d 270 1 6.79 430 e 108 13 3.55 100 f 77.2 1 3.75 100 g 77.2 1 2.83 28 h 77.2 1 5.41 230
e ve g noktaları doymuş sıvılardır ve h noktası doymuş bir gazdır. ⓘ
Kısma
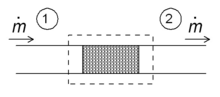
Entalpi kavramının basit uygulamalarından biri, Joule-Thomson genişlemesi olarak da bilinen kısma işlemidir. Şekilde gösterildiği gibi bir akış direncinden (valf, gözenekli tıkaç veya başka herhangi bir akış direnci türü) bir akışkanın sabit bir adyabatik akışı ile ilgilidir. Bu süreç, ortam sıcaklığı ile buzdolabının içi arasındaki sıcaklık düşüşünden sorumlu olduğu ev tipi buzdolaplarının kalbinde yer aldığı için çok önemlidir. Aynı zamanda birçok sıvılaştırıcı türünde de son aşamadır. ⓘ
Kararlı bir akış rejimi için sistemin entalpisinin (noktalı dikdörtgen) sabit olması gerekir. Dolayısıyla ⓘ
Kütle akışı sabit olduğundan, akış direncinin iki tarafındaki özgül entalpiler aynıdır:
Yani, birim kütle başına entalpi kısma sırasında değişmez. Bu ilişkinin sonuçları yukarıdaki T-s diyagramı kullanılarak gösterilebilir. c noktası 200 bar ve oda sıcaklığındadır (300 K). Joule-Thomson genleşmesi 200 bardan 1 bara kadar 400 ve 450 kJ/kg izentalpleri arasında yer alan kabaca 425 kJ/kg'lık (diyagramda gösterilmemiştir) sabit entalpi eğrisini takip eder ve yaklaşık 270 K sıcaklıktaki d noktasında sona erer. Dolayısıyla 200 bardan 1 bara genleşme azotu 300 K'den 270 K'ye soğutur. Valfte çok fazla sürtünme vardır ve çok fazla entropi üretilir, ancak yine de son sıcaklık başlangıç değerinin altındadır. ⓘ
e noktası, h = 100 kJ/kg ile doymuş sıvı çizgisi üzerinde olacak şekilde seçilmiştir. Kabaca p = 13 bar ve T = 108 K'ye karşılık gelir. Bu noktadan 1 bar basınca kadar kısma iki fazlı bölgede (f noktası) sona erer. Bu, gaz ve sıvı karışımının kısma vanasını terk ettiği anlamına gelir. Entalpi kapsamlı bir parametre olduğundan, f'deki entalpi (hf) f'deki sıvı oranı (xf) ile çarpılan g'deki entalpiye (hg) artı f'deki gaz oranı (1 - xf) ile çarpılan h'deki entalpiye (hh) eşittir. Yani ⓘ
Sayılarla: 100 = xf × 28 + (1 - xf) × 230, yani xf = 0,64. Bu, kısma valfinden çıkan sıvı-gaz karışımındaki sıvının kütle oranının %64 olduğu anlamına gelir. ⓘ
Kompresörler

Bir P gücü örneğin elektrik gücü olarak uygulanır. Eğer sıkıştırma adyabatik ise, gaz sıcaklığı artar. Tersine çevrilebilir durumda, T-s diyagramında dikey bir çizgiye karşılık gelen sabit entropide olacaktır. Örneğin, azotun 1 bardan (a noktası) 2 bara (b' noktası) sıkıştırılması 300 K'den 380 K'ye bir sıcaklık artışına neden olur. Sıkıştırılmış gazın ortam sıcaklığı Ta'da çıkmasını sağlamak için, örneğin soğutma suyu ile ısı değişimi gereklidir. İdeal durumda sıkıştırma izotermaldir. Çevreye olan ortalama ısı akışı Q̇'dir. Sistem kararlı durumda olduğu için birinci yasa şunları verir ⓘ
Sıkıştırma için gereken minimum güç, sıkıştırmanın tersine çevrilebilir olması halinde gerçekleşir. Bu durumda açık sistemler için termodinamiğin ikinci yasası şunları verir ⓘ
Q̇'nin ortadan kaldırılması minimum güç sağlar ⓘ
Örneğin, 1 kg azotun 1 bardan 200 bara sıkıştırılması en az (hc - ha) - Ta(sc - sa)'ya mal olur. T-s diyagramı ile elde edilen verilerle (430 - 461) - 300 × (5.16 - 6.85) = 476 kJ/kg değerini buluruz. ⓘ
Güç için bağıntı şu şekilde yazılarak daha da basitleştirilebilir ⓘ
dh = T ds + v dp ile, bu nihai bağıntı ile sonuçlanır ⓘ
Tarihçe ve etimoloji
Entalpi terimi termodinamik tarihinde nispeten geç bir dönemde, 20. yüzyılın başlarında ortaya atılmıştır. Enerji modern anlamda 1802 yılında Thomas Young tarafından, entropi ise 1865 yılında Rudolf Clausius tarafından ortaya atılmıştır. Enerji, iş yapma kapasitesi fikrini ifade etmek için "iş" anlamına gelen Yunanca ἔργον (ergon) kelimesinin kökünü kullanır. Entropi, Yunanca dönüşüm veya dönme anlamına gelen τροπή (tropē) kelimesini kullanır. Entalpi, Yunanca θάλπος (thalpos) "sıcaklık, ısı" sözcüğünün kökünü kullanır. ⓘ
Terim eski ısı içeriği kavramını ifade eder, çünkü dH sadece sabit basınçta bir süreçte kazanılan ısı miktarını ifade eder, ancak basıncın değişken olduğu genel durumda ifade etmez. Josiah Willard Gibbs açıklık getirmek için "sabit basınç için ısı fonksiyonu" terimini kullanmıştır. ⓘ
"Isı içeriği" H kavramının ortaya atılması Benoît Paul Émile Clapeyron ve Rudolf Clausius ile ilişkilidir (Clausius-Clapeyron ilişkisi, 1850). ⓘ
Entalpi terimi ilk kez 1909 yılında basılı olarak ortaya çıkmıştır. Büyük olasılıkla bir yıl önce Paris'teki Soğutma Enstitüsü'nün ilk toplantısında sözlü olarak tanıtmış olan Heike Kamerlingh Onnes'e atfedilmektedir. Ancak 1920'lerde, özellikle de 1927'de yayınlanan Mollier Buhar Tabloları ve Diyagramları ile yaygınlık kazanmıştır. ⓘ
1920'lere kadar H sembolü, biraz tutarsız bir şekilde, genel olarak "ısı" için kullanılıyordu. H'nin entalpi veya "sabit basınçtaki ısı içeriği" ile sınırlı olarak tanımlanması 1922 yılında Alfred W. Porter tarafından resmen önerilmiştir. ⓘ














































