Paladyum
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Paladyum | |||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Telaffuz | /pəˈleɪdiəm/ (pə-LAY-dee-əm) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Görünüş | gümüşi beyaz | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Standart atom ağırlığı Ar°(Pd) |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Periyodik tabloda paladyum | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atom numarası (Z) | 46 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grup | Grup 10 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dönem | dönem 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | d-blok | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektron konfigürasyonu | [[[Kripton|Kr]]] 4d10 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kabuk başına elektron | 2, 8, 18, 18 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fiziksel özellikler | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| STP'de Faz | katı | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Erime noktası | 1828,05 K (1554,9 °C, 2830,82 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kaynama noktası | 3236 K (2963 °C, 5365 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Yoğunluk (r.t.'ye yakın) | 12,023 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| sıvı olduğunda (m.p.'de) | 10,38 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Füzyon ısısı | 16,74 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Buharlaşma ısısı | 358 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar ısı kapasitesi | 25,98 J/(mol-K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
Buhar basıncı
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomik özellikler | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oksidasyon durumları | 0, +1, +2, +3, +4 (hafif bazik bir oksit) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegatiflik | Pauling ölçeği: 2.20 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| İyonlaşma enerjileri |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomik yarıçap | ampi̇ri̇k: 137 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalent yarıçap | 139±6 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waals yarıçapı | 163 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Paladyumun spektral çizgileri | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Diğer özellikler | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Doğal oluşum | ilkel | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristal yapı | yüz merkezli kübik (fcc) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ses hızı ince çubuk | 3070 m/s (20 °C'de) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termal genleşme | 11,8 µm/(m⋅K) (25 °C'de) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termal iletkenlik | 71,8 W/(m⋅K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektriksel direnç | 105,4 nΩ⋅m (20 °C'de) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Manyetik sıralama | paramanyetik | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar manyetik duyarlılık | +567,4×10-6 cm3/mol (288 K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Young modülü | 121 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kayma modülü | 44 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Yığın modülü | 180 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Poisson oranı | 0.39 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohs sertliği | 4.75 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vickers sertliği | 400-600 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brinell sertliği | 320-610 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS Numarası | 7440-05-3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tarih | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| İsimlendirme | adını Pallas Athena'dan alan Pallas asteroidinden almıştır. | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Keşif ve ilk izolasyon | William Hyde Wollaston (1802) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Paladyumun ana izotopları | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
Paladyum, sembolü Pd ve atom numarası 46 olan kimyasal bir elementtir. İngiliz kimyager William Hyde Wollaston tarafından 1803 yılında keşfedilen nadir ve parlak gümüşi beyaz bir metaldir. Adını, Yunan tanrıçası Athena'nın Pallas'ı öldürdüğünde kazandığı lakabından alan asteroid Pallas'tan almıştır. Paladyum, platin, rodyum, rutenyum, iridyum ve osmiyum, platin grubu metaller (PGM'ler) olarak adlandırılan bir element grubunu oluşturur. Benzer kimyasal özelliklere sahiptirler, ancak paladyum en düşük erime noktasına sahiptir ve içlerinde en az yoğun olanıdır. ⓘ
Paladyum ve eşdeğeri platin arzının yarısından fazlası, otomobil egzozundaki zararlı gazların (hidrokarbonlar, karbon monoksit ve nitrojen dioksit) %90 kadarını zararsız maddelere (nitrojen, karbon dioksit ve su buharı) dönüştüren katalitik konvertörlerde kullanılmaktadır. Paladyum ayrıca elektronik, diş hekimliği, tıp, hidrojen arıtma, kimyasal uygulamalar, yeraltı suyu arıtma ve mücevherat alanlarında da kullanılmaktadır. Paladyum, hidrojen ve oksijenin elektrik, ısı ve su üretmek için reaksiyona girdiği yakıt hücrelerinin önemli bir bileşenidir. ⓘ
Paladyum ve diğer PGM'lerin cevher yatakları nadirdir. En geniş yataklar Güney Afrika'daki Transvaal Havzasını kapsayan Bushveld Igneous Complex'in norit kuşağında, Amerika Birleşik Devletleri'nin Montana eyaletindeki Stillwater Complex'te; Kanada'nın Ontario eyaletindeki Sudbury Basin ve Thunder Bay District'te ve Rusya'daki Norilsk Complex'te bulunmuştur. Geri dönüşüm de çoğunlukla hurdaya çıkmış katalitik konvertörlerden elde edilen bir kaynaktır. Çok sayıda uygulama ve sınırlı tedarik kaynakları, önemli bir yatırım ilgisiyle sonuçlanmaktadır. ⓘ
Gümüş gibi parlaktır. Gayet ince dağılmış bir hâlde iken periyotlar sisteminde kendisinin üstünde bulunan nikelden daha fazla hidrojen gazını çözer. Paladyumda çözünmüş bulunan hidrojen nikelde olduğu gibi çok aktif bir hâldedir ve doymamış organik bileşikleri hidrojenlendirebilir. Hiçbir gaz geçirmeyen levha hâlindeki paladyum, hidrojen gazını geçirir. Paladyum, tuzlarında ekseriyetle +2 değerlikte olup bunlar kahverengidirler. Kahverengi ve nem kapıcı billurlardan oluşan karbon monoksit tarafından koloidal şekilde bulunan ve siyah renkte olan paladyum metaline indirgenir. ⓘ
Türk Parası Kıymetini Koruma Kanunu hakkında, 32 sayılı kararda yapılan değişikliklerle paladyum resmen değerli maden olarak kanuna eklendi. ⓘ
Özellikleri
Paladyum periyodik tabloda 10. gruba aittir, ancak en dış elektronlardaki konfigürasyon Hund kuralına uygundur. 5s orbitalindeki elektronlar 4d orbitallerini doldurmak için göç eder, çünkü 5s2 4d8 konfigürasyonu yerine tamamen dolu bir 4d10 kabuğuna sahip olmak enerjik olarak daha elverişlidir. ⓘ
| Z | Element | Elektron/kabuk sayısı ⓘ |
|---|---|---|
| 28 | nikel | 2, 8, 16, 2 (veya 2, 8, 17, 1) |
| 46 | PALADYUM | 2, 8, 18, 18, 0 |
| 78 | platin | 2, 8, 18, 32, 17, 1 |
| 110 | darmstadtium | 2, 8, 18, 32, 32, 16, 2 (öngörülen) |
5. periyotta benzersiz olan bu 5s0 konfigürasyonu, paladyumu sadece bir eksik elektron kabuğuna sahip en ağır element yapar ve üzerindeki tüm kabuklar boştur. ⓘ
Paladyum, platine benzeyen yumuşak gümüş-beyaz bir metal görünümündedir. Platin grubu metaller arasında en az yoğun ve en düşük erime noktasına sahip olanıdır. Tavlandığında yumuşak ve sünektir ve soğuk işlendiğinde mukavemeti ve sertliği büyük ölçüde artar. Paladyum konsantre nitrik asitte, sıcak, konsantre sülfürik asitte ve ince öğütüldüğünde hidroklorik asitte yavaşça çözünür. Oda sıcaklığında aqua regia içinde kolayca çözünür. ⓘ
Paladyum standart sıcaklıkta oksijenle reaksiyona girmez (ve bu nedenle havada kararmaz). 800 °C'ye kadar ısıtılan paladyum bir paladyum(II) oksit (PdO) tabakası üretecektir. Muhtemelen monoksit yüzey tabakasının oluşumu nedeniyle zamanla yavaşça hafif kahverengimsi bir renk geliştirebilir. ⓘ
Düşük sıcaklıkta alfa parçacık bombardımanı ile üretilen kusurlu paladyum filmleri Tc=3.2 K olan süper iletkenlik sergiler. ⓘ
İzotoplar
Doğal olarak oluşan paladyum, altısı kararlı olmak üzere yedi izotoptan oluşur. En kararlı radyoizotoplar 6,5 milyon yıllık yarı ömre sahip 107Pd (doğada bulunur), 17 günlük 103Pd ve 3,63 günlük 100Pd'dir. Atom ağırlıkları 90.94948(64) u (91Pd) ile 122.93426(64) u (123Pd) arasında değişen on sekiz diğer radyoizotop karakterize edilmiştir. Bunların 101Pd (yarı ömür: 8,47 saat), 109Pd (yarı ömür: 13,7 saat) ve 112Pd (yarı ömür: 21 saat) hariç yarı ömürleri otuz dakikadan azdır. ⓘ
Atomik kütle birimi değerleri en bol bulunan kararlı izotop olan 106Pd'den daha düşük olan izotoplar için birincil bozunma modu elektron yakalama olup birincil bozunma ürünü rodyumdur. Atomik kütlesi 106'dan büyük olan Pd izotopları için birincil bozunma modu beta bozunmasıdır ve bu bozunmanın birincil ürünü gümüştür. ⓘ
Radyojenik 107Ag, 107Pd'nin bir bozunma ürünüdür ve ilk olarak 1978 yılında 1976 Santa Clara meteoritinde keşfedilmiştir. Keşifçiler, demir çekirdekli küçük gezegenlerin birleşme ve farklılaşmasının nükleosentetik bir olaydan 10 milyon yıl sonra meydana gelmiş olabileceğini öne sürmektedir. Güneş Sistemi'nin oluşumundan bu yana erimiş olan cisimlerde gözlemlenen 107Pd ve Ag korelasyonları, erken Güneş Sistemi'nde kısa ömürlü nüklitlerin varlığını yansıtıyor olmalıdır. 107
Pd ayrıca 235'in kendiliğinden veya indüklenmiş fisyonunda bir fisyon ürünü olarak üretilir
U. Çevrede çok hareketli olmadığından ve nispeten düşük bir bozunma enerjisine sahip olduğundan, 107
Pd genellikle uzun ömürlü fisyon ürünleri arasında daha az endişe verici olanlardan biri olarak kabul edilir. ⓘ
Bileşikler
Paladyum bileşikleri öncelikle 0 ve +2 oksidasyon durumunda bulunur. Daha az yaygın olan diğer haller de tanınmaktadır. Genel olarak paladyum bileşikleri platin bileşiklerine diğer elementlerden daha çok benzemektedir. ⓘ
β-PdCl2'nin yapısı ⓘ
Paladyum (II)
Paladyum (II) klorür, diğer paladyum bileşikleri için temel başlangıç maddesidir. Paladyumun klor ile reaksiyonu sonucu ortaya çıkar. Baryum sülfat üzerinde paladyum, karbon üzerinde paladyum ve karbon üzerinde paladyum klorür gibi heterojen paladyum katalizörleri hazırlamak için kullanılır. Nitrik asit içindeki PdCl2 çözeltileri, yine çok yönlü bir reaktif olan paladyum (II) asetat vermek için asetik asit ile reaksiyona girer. PdCl2, PdCl2L2 tipinde kare düzlemsel kompleksler vermek üzere ligandlarla (L) reaksiyona girer. Bu tür komplekslere bir örnek, benzonitril türevi PdX2(PhCN)2'dir.
- PdCl2 + 2 L → PdCl2L2 (L = PhCN, PPh3, NH3, vb.)
Bis(trifenilfosfin)paladyum(II) diklorür kompleksi faydalı bir katalizördür. ⓘ



Paladyum(0)
Paladyum, PdL4, PdL3 ve PdL2 formülüne sahip bir dizi zerovalent kompleks oluşturur. Örneğin, PdCl2(PPh3)2 ve PPh3 karışımının indirgenmesi tetrakis(trifenilfosfin)paladyum(0) verir:
- 2 PdCl2(PPh3)2 + 4 PPh3 + 5 N2H4 → 2 Pd(PPh3)4 + N2 + 4 N2H5+Cl- ⓘ
Bir diğer önemli paladyum(0) kompleksi olan tris(dibenzylideneacetone)dipalladium(0) (Pd2(dba)3), dibenzylideneacetone varlığında sodyum tetrakloropalladatın indirgenmesiyle hazırlanır. ⓘ
Paladyum(0) ve paladyum(II), Richard F. Heck, Ei-ichi Negishi ve Akira Suzuki'ye verilen 2010 Nobel Kimya Ödülü'nde de kabul edildiği gibi, birleştirme reaksiyonlarında katalizördür. Bu tür reaksiyonlar, ince kimyasalların sentezi için yaygın olarak uygulanmaktadır. Öne çıkan birleşme reaksiyonları arasında Heck, Suzuki, Sonogashira birleşmesi, Stille reaksiyonları ve Kumada birleşmesi yer almaktadır. Palladyum(II) asetat, tetrakis(trifenilfosfin)palladyum(0) (Pd(PPh3)4 ve tris(dibenzilidenaseton)dipalladyum(0) (Pd2(dba)3) ya katalizör ya da ön katalizör olarak görev yapar. ⓘ
Diğer oksidasyon durumları
Pd(IV) bileşikleri nispeten nadir olmakla birlikte, bir örnek sodyum hekzakloropalladat(IV), Na2[PdCl6]'dır. Birkaç paladyum(III) bileşiği de bilinmektedir. Paladyum(VI) 2002 yılında iddia edilmiş, ancak daha sonra çürütülmüştür. ⓘ
Karışık değerlikli paladyum kompleksleri mevcuttur, örneğin Pd4(CO)4(OAc)4Pd(acac)2, alternatif olarak birbirine bağlı Pd4(CO)4(OAc)4 ve Pd(acac)2 birimleri ile sonsuz bir Pd zincir yapısı oluşturur. ⓘ
Daha elektropozitif bir elementle alaşım yapıldığında, Paladyum negatif bir yük kazanabilir. Bu tür bileşikler galyum palladid gibi palladidler olarak bilinir. R'nin Skandiyum, İtriyum veya lantanitlerden herhangi biri olduğu RPd3 stokiyometrisine sahip palladidler mevcuttur. ⓘ
Oluşum
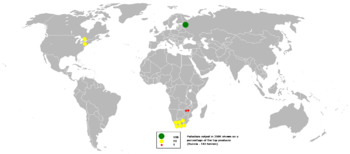
Toplam paladyum madeni üretimi 2016 yılında 208.000 kilograma ulaşırken, Rusya 82.000 kilogramla en büyük üretici olmuş, onu Güney Afrika, Kanada ve ABD izlemiştir. Rusya'nın Norilsk Nickel şirketi, dünya üretiminin %39'unu gerçekleştirerek küresel olarak en büyük paladyum üreticileri arasında ilk sırada yer almaktadır. ⓘ
Paladyum, Ural Dağları, Avustralya, Etiyopya, Kuzey ve Güney Amerika'daki plaser yataklarında altın ve diğer platin grubu metallerle alaşımlı serbest metal olarak bulunabilir. Paladyum üretimi için bu yataklar sadece küçük bir rol oynamaktadır. En önemli ticari kaynaklar Sudbury Havzası, Ontario'da bulunan nikel-bakır yatakları ve Sibirya'daki Norilsk-Talnakh yataklarıdır. Diğer büyük yatak ise Güney Afrika Bushveld Magmatik Kompleksi içindeki Merensky Reef platin grubu metaller yatağıdır. Montana'daki Stillwater magmatik kompleksi ve Ontario'daki Lac des Îles magmatik kompleksinin Roby bölgesi cevher kütlesi Kanada ve Amerika Birleşik Devletleri'ndeki diğer iki paladyum kaynağıdır. Paladyum nadir bulunan cooperite ve polarite minerallerinde bulunur. Daha birçok Pd minerali bilinmektedir, ancak bunların hepsi çok nadirdir. ⓘ
Paladyum ayrıca nükleer fisyon reaktörlerinde üretilir ve kullanılmış nükleer yakıttan çıkarılabilir (bkz. değerli metallerin sentezi), ancak paladyum için bu kaynak kullanılmamaktadır. Mevcut nükleer yeniden işleme tesislerinin hiçbiri yüksek seviyeli radyoaktif atıklardan paladyum çıkaracak donanıma sahip değildir. Kullanılmış yakıtta Paladyum geri kazanımı için bir komplikasyon da 107
Pd hafif radyoaktif uzun ömürlü bir fisyon ürünüdür. Son kullanıma bağlı olarak, 107 Pd'nin katkıda bulunduğu radyoaktivite
Pd, geri kazanılan Paladyumu maliyetli bir izotop ayrıştırma adımı olmadan kullanılamaz hale getirebilir. ⓘ
Uygulamalar


Günümüzde paladyumun en büyük kullanım alanı katalitik konvertörlerdir. Paladyum ayrıca mücevherat, dişçilik, saat yapımı, kan şekeri test şeritleri, uçak bujileri, cerrahi aletler ve elektrik kontaklarında da kullanılmaktadır. Paladyum ayrıca profesyonel enine (konser veya klasik) flüt yapımında da kullanılmaktadır. Bir emtia olarak, paladyum külçeleri XPD ve 964 ISO para birimi kodlarına sahiptir. Paladyum bu kodlara sahip olan sadece dört metalden biridir, diğerleri altın, gümüş ve platindir. Hidrojeni adsorbe ettiği için paladyum, 1980'lerin sonlarındaki tartışmalı soğuk füzyon deneylerinin önemli bir bileşeniydi. ⓘ
Kataliz
Karbon üzerindeki paladyumda olduğu gibi ince bir şekilde bölündüğünde, paladyum çok yönlü bir katalizör oluşturur; hidrojenasyon, dehidrojenasyon ve petrol kırma gibi heterojen katalitik işlemleri hızlandırır. Paladyum, Lindlar Paladyumu olarak da adlandırılan Lindlar katalizörü için de gereklidir. Organik kimyadaki çok sayıda karbon-karbon bağlanma reaksiyonu paladyum bileşik katalizörleri tarafından kolaylaştırılır. Örneğin
- Heck reaksiyonu
- Suzuki kaplin
- Tsuji-Trost reaksiyonları
- Wacker süreci
- Negishi reaksiyonu
- Stille kaplin
- Sonogashira kaplini ⓘ
(Bkz. paladyum bileşikleri ve paladyum katalizli birleştirme reaksiyonları). ⓘ
İletken malzemeler üzerinde dağıldığında paladyum, alkali ortamda birincil alkollerin oksidasyonu için mükemmel bir elektrokatalizördür. Paladyum aynı zamanda homojen kataliz için çok yönlü bir metaldir ve oldukça seçici kimyasal dönüşümler için çok çeşitli ligandlarla birlikte kullanılır. ⓘ
2010 yılında Nobel Kimya Ödülü "organik sentezde paladyum katalizli çapraz birleşmeler için" Richard F. Heck, Ei-ichi Negishi ve Akira Suzuki'ye verilmiştir. 2008 yılında yapılan bir çalışma, paladyumun karbon-flor bağları için etkili bir katalizör olduğunu göstermiştir. ⓘ
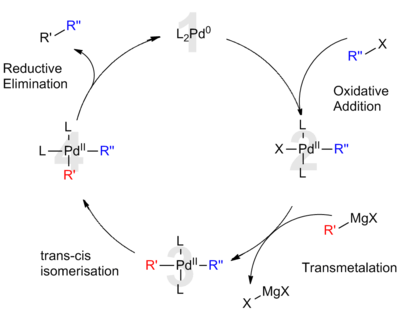
Paladyum katalizi öncelikle organik kimya ve endüstriyel uygulamalarda kullanılmakla birlikte, sentetik biyoloji için bir araç olarak kullanımı artmaktadır; 2017 yılında, paladyum nanopartiküllerinin etkili in vivo katalitik aktivitesi, memelilerde hastalığı tedavi etmek için gösterilmiştir. ⓘ
Elektronik
Paladyumun elektronikteki ilk büyük uygulaması, elektrotlar için paladyumun (ve paladyum-gümüş alaşımının) kullanıldığı çok katmanlı seramik kapasitörlerdir. Paladyum (bazen nikel ile alaşımlı) tüketici elektroniğinde ve lehim malzemelerinde bileşen ve konektör kaplaması için kullanılır veya kullanılabilir. Johnson Matthey raporuna göre elektronik sektörü 2006 yılında 1.07 milyon troy ons (33 ton) paladyum tüketmiştir. ⓘ
Teknoloji
Hidrojen ısıtılmış paladyumdan kolayca difüze olur ve Pd membranlı membran reaktörleri yüksek saflıkta hidrojen üretiminde kullanılır. Paladyum, elektrokimyasal çalışmalarda paladyum-hidrojen elektrotlarında kullanılır. Paladyum (II) klorür, karbon monoksit gazını karbon dioksite kolayca katalize eder ve karbon monoksit dedektörlerinde kullanışlıdır. ⓘ
Hidrojen depolama
Paladyum oda sıcaklıklarında hidrojeni kolayca adsorbe ederek x 1'den küçük olduğunda paladyum hidrit PdHx oluşturur. Bu özellik birçok geçiş metali için ortak olsa da, paladyum benzersiz bir şekilde yüksek bir emme kapasitesine sahiptir ve x 1'e yaklaşana kadar sünekliğini kaybetmez. Bu özellik, verimli, ucuz ve güvenli bir hidrojen yakıt depolama ortamı tasarlamak için araştırılmıştır, ancak paladyumun kendisi şu anda bu amaç için engelleyici derecede pahalıdır. Paladyumdaki hidrojen içeriği, hidrojen artışı ile azalan ve PdH0.62 için sıfır olan manyetik duyarlılık ile ilişkilendirilebilir. Herhangi bir yüksek oranda, katı çözelti diyamanyetik hale gelir. ⓘ
Paladyum ayrıca hidrojen saflaştırma membranları aracılığıyla hidrojen saflaştırma için de kullanılır. ⓘ
Diş Hekimliği
Paladyum, korozyonu azaltmak ve nihai restorasyonun metalik parlaklığını artırmak için bazı dental amalgam alaşımlarında az miktarda (yaklaşık %0,5) kullanılır. ⓘ
Mücevher
Paladyum, 1939'dan beri mücevheratta değerli bir metal olarak, paladyumun doğal beyaz renginin rodyum kaplamayı gerektirmediği "beyaz altın" adı verilen alaşımlarda platine alternatif olarak kullanılmaktadır. Paladyum platinden çok daha az yoğundur. Altına benzer şekilde, paladyum 100 nm (1⁄250,000 inç) kadar ince yapraklar halinde dövülebilir. Platinin aksine, paladyum 400 °C (752 °F) üzerindeki sıcaklıklarda oksidasyon nedeniyle renk değiştirebilir, bu da onu daha kırılgan ve dolayısıyla mücevheratta kullanım için daha az uygun hale getirir; bunu önlemek için, mücevherat için tasarlanan paladyum kontrollü koşullar altında ısıtılır. ⓘ
2004 yılından önce paladyumun mücevheratta başlıca kullanım alanı beyaz altın üretimiydi. Paladyum beyaz altının en popüler üç alaşım metalinden biridir (nikel ve gümüş de kullanılabilir). Paladyum-altın nikel-altından daha pahalıdır, ancak nadiren alerjik reaksiyonlara neden olur (ancak nikel ile bazı çapraz alerjiler ortaya çıkabilir). ⓘ
İkinci Dünya Savaşı sırasında platin stratejik bir kaynak haline geldiğinde, birçok mücevher bandı paladyumdan yapılmıştır. Paladyum, dökümün teknik zorluğu nedeniyle mücevheratta çok az kullanılıyordu. Döküm sorununun çözülmesiyle birlikte, başlangıçta platin fiyatı artarken paladyum fiyatının düşmesi nedeniyle mücevheratta paladyum kullanımı artmıştır. Altın ve platin fiyatlarının hızla yükseldiği 2004 yılının başlarında Çin, 2005 yılında 37 ton tüketerek hacimli paladyum takı üretmeye başladı. Platinin göreceli fiyatındaki müteakip değişiklikler paladyum talebini 2009 yılında 17,4 tona düşürmüştür. Katalizör olarak paladyuma olan talep, Ocak 2019'da paladyumun fiyatını platinin fiyatından yaklaşık %50 daha yüksek bir seviyeye çıkarmıştır. ⓘ
Ocak 2010'da, Birleşik Krallık'taki tahlil ofisleri tarafından paladyum için damgalar tanıtıldı ve saf veya alaşımlı paladyum reklamı yapan tüm mücevherler için damgalama zorunlu hale geldi. Eşyalar, alaşımın binde 500, 950 veya 999 parçası paladyum olarak işaretlenebilir. ⓘ
Altından yapılan dolmakalem uçları bazen gümüş (altın yerine) görünümü istendiğinde paladyum ile kaplanır. Sheaffer onlarca yıldır paladyum kaplamayı ya altın uçlara vurgu olarak ya da altını tamamen kaplayarak kullanmaktadır. ⓘ
Paladyum ayrıca lüks marka Hermes tarafından, en ünlüsü çok aranan Birkin olan el çantalarının donanımını kaplayan metallerden biri olarak kullanılmaktadır. ⓘ
Fotoğrafçılık
Platinotip baskı sürecinde, fotoğrafçılar platin veya paladyum tuzları kullanarak güzel sanatlara yönelik siyah-beyaz baskılar yaparlar. Genellikle platinle birlikte kullanılan paladyum, gümüşe bir alternatif oluşturur. ⓘ
Sağlık üzerindeki etkileri
Toksisite
| Tehlikeler | |
|---|---|
| GHS etiketlemesi: | |
Piktogramlar
|

|
Sinyal kelimesi
|
Uyarı |
Tehlike bildirimleri
|
H317 |
Önlem ifadeleri
|
P261, P273, P280, P302+P352, P321, P333+P313, P363, P501 |
| NFPA 704 (yangın elması) | |
Paladyum, geleneksel olarak ölçüldüğünde (örneğin LD50) düşük toksisiteye sahip bir metaldir. Paladyum toksisitesinin mekanizması üzerine yapılan son araştırmalar, karaciğer ve böbrekte daha uzun bir zaman diliminde ve hücresel düzeyde ölçüldüğünde yüksek toksisiteye işaret etmektedir. Mitokondri, mitokondriyal membran potansiyelinin çökmesi ve hücresel glutatyon (GSH) seviyesinin azalması yoluyla paladyum toksisitesinde kilit bir role sahip gibi görünmektedir. Bu son çalışmaya kadar, paladyumun yutulduğunda insan vücudu tarafından zayıf bir şekilde emildiği düşünülüyordu. Su sümbülü gibi bitkiler düşük seviyelerdeki paladyum tuzları tarafından öldürülür, ancak diğer bitkilerin çoğu bunu tolere eder, ancak testler %0.0003'ün üzerindeki seviyelerde büyümenin etkilendiğini göstermektedir. Yüksek dozlarda paladyum zehirli olabilir; kemirgenler üzerinde yapılan testler kanserojen olabileceğini göstermektedir, ancak yukarıda bahsedilen son araştırmaya kadar, elementin insanlara zarar verdiğine dair net bir kanıt yoktu. ⓘ
Önlemler
Diğer platin grubu metaller gibi, dökme Pd de oldukça inerttir. Kontakt dermatit rapor edilmiş olsa da, etkilere ilişkin veriler sınırlıdır. Paladyuma karşı alerjik reaksiyon gösteren kişilerin nikele de tepki gösterdiği gösterilmiştir, bu nedenle alerjisi olan kişilerde paladyum içeren diş alaşımlarının kullanılmasından kaçınılması tavsiye edilir. ⓘ
Paladyumun bir kısmı katalitik konvertörlü araçların egzoz gazlarıyla birlikte yayılır. Bu tür arabalardan 4 ila 108 ng/km arasında paladyum partikülü salınırken, gıdalardan toplam alımın kişi başına günde 2 µg'dan az olduğu tahmin edilmektedir. İkinci olası paladyum kaynağı diş restorasyonudur ve bu restorasyondan paladyum alımının kişi başına günde 15 µg'dan az olduğu tahmin edilmektedir. Paladyum ya da bileşikleriyle çalışan kişiler çok daha yüksek bir alım miktarına sahip olabilir. Paladyum klorür gibi çözünebilir bileşikler için, %99'u 3 gün içinde vücuttan atılır. ⓘ
Çözünebilir paladyum bileşiklerinin farelerdeki medyan öldürücü dozu (LD50) oral uygulama için 200 mg/kg ve intravenöz uygulama için 5 mg/kg'dır. ⓘ
Tarih

William Hyde Wollaston Temmuz 1802'de laboratuvar defterine yeni bir soy metal keşfettiğini not etti ve aynı yılın Ağustos ayında bu metale paladyum adını verdi. Wollaston malzemenin bir miktarını saflaştırdı ve Nisan 1803'te Soho'daki küçük bir dükkanda keşfedenin adını vermeden satışa sundu. Paladyumun platin ve cıva alaşımı olduğunu iddia eden Richard Chenevix'in sert eleştirilerinden sonra, Wollaston anonim olarak 20 tane sentetik paladyum alaşımı için 20 sterlin ödül teklif etti. Chenevix paladyum üzerine yaptığı deneyleri yayınladıktan sonra 1803 yılında Copley Madalyası aldı. Wollaston 1804 yılında rodyumun keşfini yayınladı ve paladyum üzerine yaptığı bazı çalışmalardan bahsetti. Paladyumun kaşifi olduğunu 1805'teki bir yayınında açıklamıştır. ⓘ
Paladyum, 1802 yılında Wollaston tarafından iki ay önce keşfedilen asteroit 2 Pallas'tan sonra adlandırılmıştır. Wollaston paladyumu Güney Amerika'daki ham platin cevherinde, cevheri aqua regia'da çözerek, çözeltiyi sodyum hidroksit ile nötralize ederek ve platini amonyum klorür ile amonyum kloroplatinat olarak çöktürerek buldu. Paladyum metalini çıkarmak için ısıtılan paladyum (II) siyanür bileşiğini oluşturmak için merkürik siyanür ekledi. ⓘ
Paladyum klorür bir zamanlar günde 0,065 g (vücut ağırlığının kilogramı başına yaklaşık bir miligram) oranında tüberküloz tedavisi olarak reçete edildi. Bu tedavinin birçok olumsuz yan etkisi vardı ve daha sonra yerini daha etkili ilaçlara bıraktı. ⓘ
Paladyumun çoğu otomobil endüstrisinde katalitik dönüştürücüler için kullanılmaktadır. Paladyum ve diğer nadir metalleri içerdikleri için katalitik konvertörler hırsızların hedefidir. Rusya'nın küresel pazara paladyum arzı 2000 yılına kadar defalarca ertelenmiş ve kesintiye uğramıştır; siyasi nedenlerle ihracat kotası zamanında verilmemiştir. Bunu izleyen piyasa paniği, Ocak 2001'de fiyatı troy ons başına 1.340 $ (43 $/g) ile tüm zamanların en yüksek seviyesine çıkardı. O sıralarda Ford Motor Company, paladyum kıtlığı nedeniyle otomobil üretiminin sekteye uğrayacağından korkarak metali stokladı. Fiyatlar 2001'in başlarında düştüğünde Ford yaklaşık 1 milyar dolar kaybetti. ⓘ
Dünya paladyum talebi 1990 yılında 100 tondan 2000 yılında yaklaşık 300 tona yükselmiştir. Amerika Birleşik Devletleri Jeoloji Araştırmaları'na göre 2006 yılında madenlerden elde edilen küresel paladyum üretimi 222 tondu. Rusya'nın Kırım'ı ilhak etmesinin ardından, yaptırımların Rusya'nın paladyum ihracatını engelleyebileceğinden dolayı, pek çok kişi paladyum arzının istikrarlı bir şekilde devam etmesinden endişe duyuyordu; Rusya'nın paladyum ihracatına getirilecek herhangi bir kısıtlama, 2014 yılında zaten büyük bir paladyum açığı olması beklenen durumu daha da kötüleştirebilirdi. Bu endişeler paladyum fiyatlarını 2001'den bu yana en yüksek seviyesine çıkardı. Eylül 2014'te ons başına 900 doların üzerine çıktı. Ancak 2016 yılında paladyum, Rusya'nın istikrarlı arzı sürdürmeyi başarması nedeniyle ons başına 614 dolar civarında seyretti. Ocak 2019'da paladyum vadeli işlemleri, özellikle otomotiv endüstrisinden gelen güçlü talep nedeniyle rekor düzeyde ilk kez ons başına 1.344 doları aştı. Paladyum 6 Ocak 2020'de troy ons başına 2.024,64 $'a (65,094 $/g) ulaşarak ilk kez troy ons başına 2.000 $'ı geçti. Fiyat Mayıs 2021 ve Mart 2022'de troy ons başına 3.000 doların üzerine çıktı. ⓘ
Yatırım olarak paladyum
Küresel paladyum satışları 2017 yılında 8,84 milyon ons (250,6 metrik ton) olarak gerçekleşmiş, bunun %86'sı otomotiv katalitik konvertörlerinin üretiminde kullanılmış, bunu endüstriyel, mücevher ve yatırım amaçlı kullanımlar izlemiştir. Küresel platinin %75'inden fazlası ve paladyumun %40'ı Güney Afrika'da çıkarılmaktadır. Paladyumun %44'ü Rusya'nın madencilik şirketi Norilsk Nickel tarafından üretilirken, geri kalanının büyük bir kısmı ABD ve Kanada merkezli madenler tarafından üretilmektedir. ⓘ
Paladyum fiyatı 3 Mayıs 2021'de, esas olarak otomobil endüstrisinden gelen katalitik konvertör talebine ilişkin spekülasyonlar nedeniyle ons başına 2.981,40 dolarla tüm zamanların en yüksek seviyesine ulaştı. Paladyum spot piyasada "XPD" kodu ile işlem görmektedir. ABD doları cinsinden işlem gördüğünde kod "XPDUSD" olur. Metalin daha sonraki bir fazlası, Rus hükümetinin Sovyet Dönemi'nden kalma stokları yılda yaklaşık 1,6 ila 2 milyon ons (45,4 ila 56,7 metrik ton) oranında satmasından kaynaklanmıştır. Bu stokların miktarı ve durumu bir devlet sırrıdır. ⓘ
Mart 2022'deki Rusya-Ukrayna Savaşı sırasında paladyum fiyatları Mart ayının ilk gününden bu yana %13 artmıştır. Rusya, Avrupa'nın başlıca tedarikçisidir ve ülke küresel üretimin %37'sini sağlamaktadır. ⓘ
Paladyum üreticileri
- Norilsk Nickel (MCX: GMKN, LSE: MNOD), paladyum tozu ve külçeleri.
- North American Palladium (NYSE: PAL), Thunder Bay, Ontario yakınlarındaki Lac des Iles paladyum madenini işleten Kanada'nın en büyük paladyum üreticisi.
- Stillwater Mining (NYSE: SWC), Montana'da büyük bir Kuzey Amerikalı paladyum madencisi. ⓘ
Borsada işlem gören ürünler
WisdomTree Physical Palladium (LSE: PHPD) tahsis edilmiş külçe paladyum ile desteklenmektedir ve dünyanın ilk paladyum ETF'sidir. Londra Borsası'nda PHPD, Xetra Trading System, Euronext ve Milan olarak listelenmiştir. ETFS Physical Palladium Shares (NYSE: PALL) New York Borsasında işlem gören bir ETF'dir. ⓘ
Külçe sikkeler ve çubuklar
Paladyuma yatırım yapmanın geleneksel bir yolu, paladyumdan yapılmış külçe sikkeler ve çubuklar satın almaktır. Mevcut paladyum sikkeleri arasında Kanada Paladyum Akçaağaç Yaprağı, Çin Panda'sı ve Amerikan Paladyum Kartalı bulunmaktadır. Doğrudan külçe paladyum yatırımının likiditesi altın ve gümüşe göre daha düşüktür çünkü paladyum sikkelerinin dolaşımı düşüktür. ⓘ




