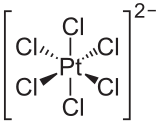Platin
 | |||||||||||||||||||||||||||||||||||||||||
| Platin | |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Telaffuz | /ˈplætɪnəm/ (PLAT-in-əm) | ||||||||||||||||||||||||||||||||||||||||
| Görünüş | gümüşi beyaz | ||||||||||||||||||||||||||||||||||||||||
| Standart atom ağırlığı Ar°(Pt) |
| ||||||||||||||||||||||||||||||||||||||||
| Periyodik tabloda platin | |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| Atom numarası (Z) | 78 | ||||||||||||||||||||||||||||||||||||||||
| Grup | Grup 10 | ||||||||||||||||||||||||||||||||||||||||
| Dönem | dönem 6 | ||||||||||||||||||||||||||||||||||||||||
| Blok | d-blok | ||||||||||||||||||||||||||||||||||||||||
| Elektron konfigürasyonu | [[[Ksenon|Xe]]] 4f14 5d9 6s1 | ||||||||||||||||||||||||||||||||||||||||
| Kabuk başına elektron | 2, 8, 18, 32, 17, 1 | ||||||||||||||||||||||||||||||||||||||||
| Fiziksel özellikler | |||||||||||||||||||||||||||||||||||||||||
| STP'de Faz | katı | ||||||||||||||||||||||||||||||||||||||||
| Erime noktası | 2041,4 K (1768,3 °C, 3214,9 °F) | ||||||||||||||||||||||||||||||||||||||||
| Kaynama noktası | 4098 K (3825 °C, 6917 °F) | ||||||||||||||||||||||||||||||||||||||||
| Yoğunluk (r.t.'ye yakın) | 21,45 g/cm3 | ||||||||||||||||||||||||||||||||||||||||
| sıvı olduğunda (m.p.'de) | 19,77 g/cm3 | ||||||||||||||||||||||||||||||||||||||||
| Füzyon ısısı | 22,17 kJ/mol | ||||||||||||||||||||||||||||||||||||||||
| Buharlaşma ısısı | 510 kJ/mol | ||||||||||||||||||||||||||||||||||||||||
| Molar ısı kapasitesi | 25,86 J/(mol-K) | ||||||||||||||||||||||||||||||||||||||||
Buhar basıncı
| |||||||||||||||||||||||||||||||||||||||||
| Atomik özellikler | |||||||||||||||||||||||||||||||||||||||||
| Oksidasyon durumları | -3, -2, -1, 0, +1, +2, +3, +4, +5, +6 (hafif bazik bir oksit) | ||||||||||||||||||||||||||||||||||||||||
| Elektronegatiflik | Pauling ölçeği: 2.28 | ||||||||||||||||||||||||||||||||||||||||
| İyonlaşma enerjileri |
| ||||||||||||||||||||||||||||||||||||||||
| Atomik yarıçap | ampi̇ri̇k: 139 pm | ||||||||||||||||||||||||||||||||||||||||
| Kovalent yarıçap | 136±5 pm | ||||||||||||||||||||||||||||||||||||||||
| Van der Waals yarıçapı | 175 pm | ||||||||||||||||||||||||||||||||||||||||
| Platinin spektral çizgileri | |||||||||||||||||||||||||||||||||||||||||
| Diğer özellikler | |||||||||||||||||||||||||||||||||||||||||
| Doğal oluşum | ilkel | ||||||||||||||||||||||||||||||||||||||||
| Kristal yapı | yüz merkezli kübik (fcc) | ||||||||||||||||||||||||||||||||||||||||
| Ses hızı ince çubuk | 2800 m/s (r.t.'de) | ||||||||||||||||||||||||||||||||||||||||
| Termal genleşme | 8,8 µm/(m⋅K) (25 °C'de) | ||||||||||||||||||||||||||||||||||||||||
| Termal iletkenlik | 71,6 W/(m⋅K) | ||||||||||||||||||||||||||||||||||||||||
| Elektriksel direnç | 105 nΩ⋅m (20 °C'de) | ||||||||||||||||||||||||||||||||||||||||
| Manyetik sıralama | paramanyetik | ||||||||||||||||||||||||||||||||||||||||
| Molar manyetik duyarlılık | +201,9 × 10-6 cm3/mol (290 K) | ||||||||||||||||||||||||||||||||||||||||
| Çekme mukavemeti | 125-240 MPa | ||||||||||||||||||||||||||||||||||||||||
| Young modülü | 168 GPa | ||||||||||||||||||||||||||||||||||||||||
| Kayma modülü | 61 GPa | ||||||||||||||||||||||||||||||||||||||||
| Yığın modülü | 230 GPa | ||||||||||||||||||||||||||||||||||||||||
| Poisson oranı | 0.38 | ||||||||||||||||||||||||||||||||||||||||
| Mohs sertliği | 3.5 | ||||||||||||||||||||||||||||||||||||||||
| Vickers sertliği | 400-550 MPa | ||||||||||||||||||||||||||||||||||||||||
| Brinell sertliği | 300-500 MPa | ||||||||||||||||||||||||||||||||||||||||
| CAS Numarası | 7440-06-4 | ||||||||||||||||||||||||||||||||||||||||
| Tarih | |||||||||||||||||||||||||||||||||||||||||
| Keşif | Antonio de Ulloa (1735) | ||||||||||||||||||||||||||||||||||||||||
| Platinin ana izotopları | |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
Platin, sembolü Pt ve atom numarası 78 olan kimyasal bir elementtir. Yoğun, dövülebilir, sünek, yüksek oranda reaktif olmayan, değerli, gümüşümsü-beyaz bir geçiş metalidir. Adı, plata "gümüş" kelimesinin küçültülmüş hali olan İspanyolca platina kelimesinden gelmektedir. ⓘ
Platin, platin element grubunun ve periyodik element tablosunun 10. grubunun bir üyesidir. Doğal olarak oluşan altı izotopu vardır. Yaklaşık 5 μg/kg ortalama bolluğu ile yerkabuğunda nadir bulunan elementlerden biridir. Bazı nikel ve bakır cevherlerinin yanı sıra, çoğunlukla dünya üretiminin %80'ini oluşturan Güney Afrika'daki bazı doğal yataklarda bulunur. Yerkabuğundaki azlığı nedeniyle yılda sadece birkaç yüz ton üretilir ve önemli kullanım alanları göz önüne alındığında oldukça değerlidir ve önemli bir değerli metal emtiasıdır. ⓘ
Platin en az reaktif metallerden biridir. Yüksek sıcaklıklarda bile korozyona karşı olağanüstü bir dirence sahiptir ve bu nedenle asil bir metal olarak kabul edilir. Sonuç olarak, platin genellikle doğal platin olarak kimyasal olarak birleşmemiş halde bulunur. Çeşitli nehirlerin alüvyonlu kumlarında doğal olarak bulunduğundan, ilk olarak Kolomb öncesi Güney Amerika yerlileri tarafından sanat eserleri üretmek için kullanılmıştır. Avrupa yazılarında 16. yüzyıl gibi erken bir tarihte platine atıfta bulunulmuştur, ancak Antonio de Ulloa 1748 yılında Kolombiya kökenli yeni bir metal hakkında bir rapor yayınlayana kadar bilim insanları tarafından araştırılmaya başlanmamıştır. ⓘ
Platin katalitik dönüştürücülerde, laboratuvar ekipmanlarında, elektrik kontaklarında ve elektrotlarda, platin dirençli termometrelerde, diş hekimliği ekipmanlarında ve mücevheratta kullanılır. Platin, cam endüstrisinde platini "ıslatmayan" erimiş camı manipüle etmek için kullanılır. Ağır bir metal olarak, tuzlarına maruz kalındığında sağlık sorunlarına yol açar; ancak korozyon direnci nedeniyle, metalik platin olumsuz sağlık etkileriyle ilişkilendirilmemiştir. Sisplatin, oksaliplatin ve karboplatin gibi platin içeren bileşikler, belirli kanser türlerine karşı kemoterapide uygulanmaktadır. ⓘ
Saf platin, 2015 yılından bu yana sürekli olarak saf altından daha ucuzdur. 2021'in başlarında platinin değeri troy ons başına 1.055 ABD Doları ile 1.320 ABD Doları arasında değişmekteydi. ⓘ
Platin, periyodik cetvelde Pt simgesi ile gösterilen kimyasal bir element olup atom numarası 78'dir. Ağır, dövülebilir, sünek, grimsi beyaz renkli, geçiş metalleri grubunda, kıymetli metallerdendir. Altından sonraki en kıymetli metaldir. Korozyona dayanıklı olup bazı bakır ve nikel cevherlerinde bulunur. Kuyumculukta, laboratuvar cihazlarında, elektrik kontaktlarında, diş hekimliğinde ve otomobil egzoz kontrol cihazlarında kullanılır. ⓘ

Simyacıların platin için kullandıkları simge, altın ve gümüşün simgelerinin bir araya getirilmiş şeklidir. ⓘ
Özellikleri
Fiziksel
Saf platin parlak, sünek ve dövülebilir, gümüş-beyaz bir metaldir. Platin altın, gümüş veya bakırdan daha sünektir, dolayısıyla saf metaller arasında en sünek olanıdır, ancak altından daha az dövülebilirdir. Metal korozyona karşı mükemmel direnç gösterir, yüksek sıcaklıklarda kararlıdır ve kararlı elektriksel özelliklere sahiptir. Platin 500 °C'de PtO2 oluşturarak oksitlenir; bu oksit termal olarak kolayca çıkarılabilir. Platin tetraflorür oluşturmak için 500 °C'de (932 °F) flor ile kuvvetli bir şekilde reaksiyona girer. Ayrıca klor, brom, iyot ve sülfür tarafından da saldırıya uğrar. Platin hidroklorik ve nitrik asitte çözünmez, ancak sıcak aqua regia (nitrik ve hidroklorik asit karışımı) içinde çözünerek kloroplatinik asit, H2PtCl6 oluşturur. ⓘ
Fiziksel özellikleri ve kimyasal kararlılığı onu endüstriyel uygulamalar için kullanışlı kılmaktadır. Aşınma ve kararmaya karşı direnci, ince mücevherlerde kullanım için çok uygundur. ⓘ
Kimyasal

Platinin en yaygın oksidasyon durumları +2 ve +4'tür. +1 ve +3 oksidasyon durumları daha az yaygındır ve genellikle bimetalik (veya polimetalik) türlerdeki metal bağları ile stabilize edilirler. Beklendiği gibi, tetrakoordinat platin(II) bileşikleri 16 elektronlu kare düzlemsel geometrileri benimseme eğilimindedir. Elementel platin genellikle reaktif olmamasına rağmen, sulu kloroplatinik asit (H2PtCl6) vermek için sıcak aqua regia içinde çözünür:
- Pt + 4 HNO3 + 6 HCl → H2PtCl6 + 4 NO2 + 4 H2O ⓘ
Yumuşak bir asit olarak platin, dimetil sülfoksit (DMSO) gibi kükürde karşı büyük bir afiniteye sahiptir; çok sayıda DMSO kompleksi rapor edilmiştir ve reaksiyon çözücüsünün seçiminde dikkatli olunmalıdır. ⓘ
2007 yılında Alman bilim adamı Gerhard Ertl, platin (katalitik dönüştürücü) üzerinde karbon monoksitin katalitik oksidasyonunun ayrıntılı moleküler mekanizmalarını belirlediği için Nobel Kimya Ödülü'nü kazanmıştır. ⓘ
İzotoplar
Platinin doğal olarak oluşan altı izotopu vardır: 190
Pt, 192
Pt, 194
Pt, 195
Pt, 196
Pt, ve 198
Pt. Bunların en bol bulunanı 195
Pt, tüm platinin %33,83'ünü oluşturur. Sıfır olmayan spine sahip tek kararlı izotoptur. Çekirdeğin 1/2 spini ve diğer elverişli manyetik özellikleri 195
Pt NMR. Spini ve büyük bolluğu nedeniyle, 195
Pt uydu pikleri de sıklıkla 1
H ve 31
P NMR spektroskopisi (örneğin, Pt-fosfin ve Pt-alkil kompleksleri için). 190
Pt sadece %0,01 ile en az bulunan izotoptur. Doğal olarak oluşan izotoplardan sadece 190
Pt kararsızdır, ancak 6,5×1011 yıllık bir yarı ömürle bozunur ve 15 Bq/kg doğal platin aktivitesine neden olur. 198
Pt alfa bozunmasına uğrayabilir, ancak bozunması hiç gözlemlenmemiştir (yarı ömrünün 3,2×1014 yıldan daha uzun olduğu bilinmektedir); bu nedenle kararlı kabul edilir. Platinin ayrıca atomik kütlesi 165 ila 204 arasında değişen 34 sentetik izotopu vardır, bu da bilinen toplam izotop sayısını 40 yapar. Bunlardan en az kararlı olanları 165
Pt ve 166
Pt, yarı ömürleri 260 µs iken, en kararlı olan 193
Yarılanma ömrü 50 yıl olan Pt. Çoğu platin izotopu beta bozunumu ve alfa bozunumunun bir kombinasyonu ile bozunur. 188
Pt, 191
Pt, ve 193
Pt öncelikle elektron yakalama yoluyla bozunur. 190
Pt ve 198
Pt'nin enerjik olarak elverişli çift beta bozunma yollarına sahip olduğu tahmin edilmektedir. ⓘ
Oluşum



Platin son derece nadir bir metaldir ve yerkabuğunda sadece 0,005 ppm konsantrasyonda bulunur. Bazen gümüş ile karıştırılır. Platin genellikle doğal platin olarak ve diğer platin grubu metaller ve çoğunlukla demir ile alaşım halinde kimyasal olarak birleşmemiş halde bulunur. Çoğu zaman doğal platin alüvyon yataklarındaki ikincil yataklarda bulunur. Kolombiya'nın Chocó Departmanında Kolomb öncesi insanlar tarafından kullanılan alüvyon yatakları hala platin grubu metaller için bir kaynaktır. Bir başka büyük alüvyon yatağı da Rusya'nın Ural Dağları'ndadır ve halen çıkarılmaktadır. ⓘ
Nikel ve bakır yataklarında platin grubu metaller sülfitler (örneğin, (Pt,Pd)S), tellüritler (örneğin, PtBiTe), antimonitler (PdSb) ve arsenitler (örneğin, PtAs2) ve nikel veya bakır ile uç alaşımlar olarak ortaya çıkar. Platin arsenit, sperrylite (PtAs2), Ontario, Kanada'daki Sudbury Basin yatağındaki nikel cevherleriyle ilişkili önemli bir platin kaynağıdır. Platinum, Alaska'da 1927 ve 1975 yılları arasında yaklaşık 17.000 kg (550.000 ozt) çıkarılmıştır. Maden 1990 yılında faaliyetlerini durdurmuştur. Nadir sülfit minerali kooperit, (Pt,Pd,Ni)S, paladyum ve nikel ile birlikte platin içerir. Cooperite, Güney Afrika, Gauteng, Bushveld kompleksi içindeki Merensky Resifi'nde meydana gelir. ⓘ
1865 yılında Güney Afrika'nın Bushveld bölgesinde kromitler tespit edilmiş, bunu 1906 yılında platinin keşfi izlemiştir. 1924 yılında jeolog Hans Merensky, Güney Afrika'daki Bushveld Igneous Complex'te büyük miktarda platin kaynağı keşfetti. Merensky'nin bulduğu ve Merensky Resifi olarak adlandırılan özel katman, dünyada bilinen platinin yaklaşık %75'ini içermektedir. Rusya'da Norilsk yakınlarındaki büyük bakır-nikel yatakları ve Kanada'daki Sudbury Havzası diğer iki büyük yataktır. Sudbury Havzası'nda işlenen büyük miktardaki nikel cevheri, platinin cevherde sadece 0,5 ppm olarak bulunmasını telafi etmektedir. Amerika Birleşik Devletleri'nde, örneğin Montana'daki Absaroka Range'de daha küçük rezervler bulunabilir. 2010 yılında Güney Afrika yaklaşık %77'lik payla en büyük platin üreticisi olmuş, onu %13 ile Rusya izlemiştir. 2010 yılında dünya üretimi 192.000 kg (423.000 lb) olmuştur. ⓘ
Hindistan'ın Tamil Nadu eyaletinde büyük platin yatakları mevcuttur. ⓘ
Platin Ay'da ve meteoritlerde daha yüksek bollukta bulunur. Buna paralel olarak platin, Dünya'da çarpma sonrası volkanizma ile ilişkili olan ve ekonomik olarak çıkarılabilen bolide çarpma bölgelerinde biraz daha yüksek bollukta bulunur; Sudbury Havzası buna bir örnektir. ⓘ
Bileşikler
Halojenürler
Yukarıda bahsedilen hekzakloroplatinik asit muhtemelen en önemli platin bileşiğidir, çünkü diğer birçok platin bileşiğinin öncüsü olarak hizmet eder. Tek başına, fotoğrafçılıkta, çinko gravürlerde, silinmez mürekkepte, kaplamada, aynalarda, porselen boyamada ve katalizör olarak çeşitli uygulamaları vardır. ⓘ
Hekzakloroplatinik asidin amonyum klorür gibi bir amonyum tuzu ile muamelesi, amonyum çözeltilerinde nispeten çözünmeyen amonyum hekzakloroplatinat verir. Bu amonyum tuzunun hidrojen varlığında ısıtılması onu elementel platine indirger. Potasyum hekzakloroplatinat da benzer şekilde çözünmez ve hekzakloroplatinik asit potasyum iyonlarının gravimetri ile tayininde kullanılmıştır. ⓘ
Hekzakloroplatinik asit ısıtıldığında, platin(IV) klorür ve platin(II) klorür yoluyla elementel platine ayrışır, ancak reaksiyonlar kademeli olarak gerçekleşmez:
- (H3O)2PtCl6-nH2O ⇌ PtCl4 + 2 HCl + (n + 2) H2O
- PtCl4 ⇌ PtCl2 + Cl2
- PtCl2 ⇌ Pt + Cl2 ⓘ
Her üç reaksiyon da tersinirdir. Platin(II) ve platin(IV) bromürler de bilinmektedir. Platin hekzaflorür oksijeni oksitleyebilen güçlü bir oksitleyicidir. ⓘ
Oksitler
'Adams katalizörü' olarak da bilinen Platin (IV) oksit, PtO2, potasyum hidroksit (KOH) çözeltilerinde ve konsantre asitlerde çözünebilen siyah bir tozdur. PtO2 ve daha az yaygın olan PtO'nun her ikisi de ısıtıldığında ayrışır. Platin (II,IV) oksit, Pt3O4, aşağıdaki reaksiyonda oluşur:
- 2 Pt2+ + Pt4+ + 4 O2- → Pt3O4 ⓘ
Diğer bileşikler
Paladyum asetatın aksine, platin (II) asetat ticari olarak mevcut değildir. Bir baz istendiğinde, halojenürler sodyum asetat ile birlikte kullanılmıştır. Platin(II) asetilasetonat kullanımı da rapor edilmiştir. ⓘ
Platinin -1 ila -2 arasında değişen negatif oksidasyon durumları sergilediği çeşitli baryum platinidler sentezlenmiştir. Bunlar arasında BaPt, Ba
3Pt
2, ve Ba
2Pt. Sezyum platinür, Cs
2Pt, koyu kırmızı şeffaf kristalli bir bileşiğin Pt2- içerdiği gösterilmiştir.
anyonlar. Platin ayrıca elektrokimyasal olarak indirgenmiş yüzeylerde negatif oksidasyon durumları sergiler. Platin tarafından sergilenen negatif oksidasyon durumları metalik elementler için olağandışıdır ve 6s orbitallerinin rölativistik stabilizasyonuna atfedilir. ⓘ
PtO2+ katyonunun bile elektrokimyasal olarak
4 içinde platinin +10 oksidasyon durumunda bulunduğu bileşikler elde edilebilir. ⓘ
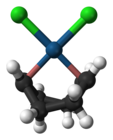
Bir etilen ligandı içeren Zeise tuzu, keşfedilen ilk organometalik bileşiklerden biridir. Dikloro(siklookta-1,5-dien)platin(II), kolayca yer değiştirebilen cod ligandları ("cod" 1,5-siklooktadienin kısaltmasıdır) içeren ticari olarak temin edilebilen bir olefin kompleksidir. Cod kompleksi ve halojenürler platin kimyası için uygun başlangıç noktalarıdır. ⓘ
Cisplatin veya cis-diamminedichloroplatinum(II), bir dizi kare düzlemli platin(II) içeren kemoterapi ilaçlarının ilkidir. Diğerleri arasında karboplatin ve oksaliplatin bulunmaktadır. Bu bileşikler DNA'yı çapraz bağlama yeteneğine sahiptir ve hücreleri alkilleyici kemoterapötik ajanlara benzer yollarla öldürür. (Sisplatinin yan etkileri arasında bulantı ve kusma, saç dökülmesi, kulak çınlaması, işitme kaybı ve nefrotoksisite yer alır). ⓘ
Yukarıdaki antitümör ajanlar gibi organoplatin bileşiklerinin yanı sıra çözünür inorganik platin kompleksleri de rutin olarak 195
Pt nükleer manyetik rezonans spektroskopisi. ⓘ
Sisplatin ⓘ
Tarih
Erken dönem kullanımlar
Arkeologlar, MÖ 1200 gibi erken bir tarihte eski Mısır mezarlarında kullanılan altının içinde platin izleri keşfetmişlerdir. Örneğin, Shepenupet II'nin mezarından çıkarılan küçük bir kutunun altın-platin hiyerogliflerle süslü olduğu görülmüştür. Bununla birlikte, erken Mısırlıların metal hakkındaki bilgilerinin kapsamı belirsizdir. Altınlarının içinde platin olduğunu fark etmemiş olmaları oldukça muhtemeldir. ⓘ
Metal, Kolomb öncesi Amerikalılar tarafından günümüz Esmeraldas, Ekvador yakınlarında beyaz altın-platin alaşımlı eserler üretmek için kullanılmıştır. Arkeologlar Güney Amerika'daki platin işleme geleneğini genellikle La Tolita Kültürü (yaklaşık MÖ 600 - MS 200) ile ilişkilendirmektedir, ancak bölgedeki platin eserlerin çoğu doğrudan arkeolojik kazılarla elde edilmek yerine eski eser ticareti yoluyla ikinci el olarak satın alındığından kesin tarih ve yer belirlemek zordur. Metali işlemek için altın ve platin tozlarını sinterleme yoluyla birleştirirlerdi. Elde edilen altın-platin alaşımı daha sonra aletlerle şekillendirilebilecek kadar yumuşak olurdu. Bu tür nesnelerde kullanılan platin saf bir element değil, platin grubu metallerin az miktarda paladyum, rodyum ve iridyum ile doğal olarak oluşan bir karışımıydı. ⓘ
Avrupalıların keşfi
Platine Avrupa'da yapılan ilk atıf 1557 yılında İtalyan hümanist Julius Caesar Scaliger'in yazılarında, Darién ve Meksika arasında bulunan ve "ne ateşin ne de herhangi bir İspanyol ustalığının henüz sıvılaştıramadığı" bilinmeyen asil bir metalin tanımı olarak karşımıza çıkar. İspanyollar platinle ilk karşılaşmalarından itibaren bu metali genellikle altının içindeki bir tür safsızlık olarak görmüş ve öyle muamele etmişlerdir. Genellikle basitçe çöpe atılırdı ve altının platin safsızlığıyla karıştırılmasını yasaklayan resmi bir kararname vardı. ⓘ

1735 yılında Antonio de Ulloa ve Jorge Juan y Santacilia, İspanyollar sekiz yıl boyunca Kolombiya ve Peru'da seyahat ederken Amerikan yerlilerinin platin madeni çıkardığını gördüler. Ulloa ve Juan beyazımsı metal külçelerin bulunduğu madenleri buldular ve İspanya'ya götürdüler. Antonio de Ulloa İspanya'ya döndü ve İspanya'daki ilk mineraloji laboratuvarını kurdu ve 1748 yılında platini sistematik olarak inceleyen ilk kişi oldu. Keşif gezisine ilişkin tarihsel anlatımı, platinin ne ayrılabilir ne de kalsine edilebilir olduğuna dair bir tanımlama içeriyordu. Ulloa ayrıca platin madenlerinin keşfini de öngörmüştür. 1748'de raporunu yayınladıktan sonra Ulloa yeni metali araştırmaya devam etmedi. 1758 yılında Huancavelica'daki cıva madenciliği faaliyetlerini denetlemek üzere gönderildi. ⓘ
1741'de İngiliz metalürji uzmanı Charles Wood, Jamaika'da Kolombiya platininden çeşitli örnekler buldu ve bunları daha fazla araştırması için William Brownrigg'e gönderdi. ⓘ
Brownrigg, Wood tarafından kendisine gönderilen platini inceledikten sonra 1750 yılında Royal Society'ye metal hakkında ayrıntılı bir açıklama sunmuş ve daha önce bilinen minerallerin hiçbirinde platinden bahsedilmediğini belirtmiştir. Brownrigg ayrıca platinin son derece yüksek erime noktasına ve boraksa karşı refrakterliğine dikkat çekti. Avrupa'daki diğer kimyagerler de kısa süre içinde platin üzerinde çalışmaya başladılar: Andreas Sigismund Marggraf, Torbern Bergman, Jöns Jakob Berzelius, William Lewis ve Pierre Macquer. Henrik Scheffer 1752'de "beyaz altın" olarak adlandırdığı metalin ayrıntılı bir bilimsel tanımını yayınladı ve arsenik yardımıyla platin cevherini eritmeyi nasıl başardığını anlattı. Scheffer platini altından daha az esnek, ancak korozyona karşı benzer dirençte olarak tanımlamıştır. ⓘ
İşlenebilirlik araçları
Carl von Sickingen 1772 yılında platini kapsamlı bir şekilde araştırdı. Altınla alaşım yaparak, alaşımı sıcak aqua regia'da çözerek, platini amonyum klorürle çöktürerek, amonyum kloroplatinatı tutuşturarak ve elde edilen ince bölünmüş platini çekiçleyerek dövülebilir platin yapmayı başardı. Franz Karl Achard 1784 yılında ilk platin potayı yaptı. Platini arsenikle eriterek ve daha sonra arseniği uçurarak çalıştı. ⓘ
Diğer platin ailesi üyeleri henüz keşfedilmediği için (platin listedeki ilk üyeydi), Scheffer ve Sickingen, saf demirden biraz daha fazla olan sertliği nedeniyle platinin nispeten esnek olmayan bir malzeme olacağı, hatta zaman zaman kırılgan olacağı gibi yanlış bir varsayımda bulundular, oysa aslında sünekliği ve işlenebilirliği altınınkine yakındı. Varsayımlarının önüne geçemediler çünkü denedikleri platin, platin alaşımını bozan osmiyum ve iridyum gibi çok az miktarda platin ailesi elementleriyle yüksek oranda kirlenmişti. "Plyoxen" adı verilen bu saf olmayan platin kalıntısını altınla alaşımlamak, o zamanlar esnek bir bileşik elde etmek için tek çözümdü, ancak günümüzde çok saf platin mevcuttur ve birçok yumuşak metalinkine benzer kristal yapısı nedeniyle saf platinden çok kolay bir şekilde son derece uzun teller çekilebilir. ⓘ
1786 yılında İspanya Kralı Charles III, Pierre-François Chabaneau'ya platin araştırmalarına yardımcı olması için bir kütüphane ve laboratuvar sağladı. Chabaneau cevherden altın, cıva, kurşun, bakır ve demir de dahil olmak üzere çeşitli safsızlıkları çıkarmayı başardı. Bu onu tek bir metalle çalıştığına inandırdı, ancak gerçekte cevher hala henüz keşfedilmemiş platin grubu metalleri içeriyordu. Bu durum deneylerinde tutarsız sonuçlara yol açtı. Platin zaman zaman yumuşak görünüyordu ama iridyumla alaşımlandığında çok daha kırılgan oluyordu. Bazen metal tamamen yanmazdı, ancak osmiyum ile alaşımlandığında uçuyordu. Birkaç ay sonra Chabaneau, sünger formunu beyaz-sıcak haldeyken çekiçleyip sıkıştırarak 23 kilogram saf, dövülebilir platin üretmeyi başardı. Chabeneau platinin eriyebilirliğinin ondan yapılan nesnelere değer katacağını fark etti ve Joaquín Cabezas ile birlikte platin külçeler ve mutfak eşyaları üreten bir iş kurdu. Bu, İspanya'da "platin çağı" olarak bilinen dönemi başlattı. ⓘ
Üretim


Platin, platin grubu metallerin geri kalanıyla birlikte, ticari olarak nikel ve bakır madenciliği ve işlenmesinden bir yan ürün olarak elde edilir. Bakırın elektro-rafinasyonu sırasında gümüş, altın ve platin grubu metaller gibi soy metaller ile selenyum ve tellür "anot çamuru" olarak hücrenin dibine çöker ve bu da platin grubu metallerin çıkarılması için başlangıç noktasını oluşturur. ⓘ
Saf platin plaser yataklarında veya diğer cevherlerde bulunursa, çeşitli safsızlık çıkarma yöntemleriyle bunlardan izole edilir. Platin, safsızlıklarının çoğundan önemli ölçüde daha yoğun olduğundan, daha hafif safsızlıklar bir sıvı içinde basitçe yüzdürülerek uzaklaştırılabilir. Platin paramanyetiktir, oysa nikel ve demirin her ikisi de ferromanyetiktir. Bu nedenle bu iki safsızlık, karışımın üzerinde bir elektromıknatıs çalıştırılarak giderilir. Platin diğer birçok maddeden daha yüksek bir erime noktasına sahip olduğundan, birçok safsızlık platini eritmeden yakılabilir veya eritilebilir. Son olarak, platin hidroklorik ve sülfürik asitlere karşı dirençlidir, oysa diğer maddeler bu asitler tarafından kolayca saldırıya uğrar. Metal safsızlıkları, karışımın iki asitten birinde karıştırılması ve kalan platinin geri kazanılmasıyla giderilebilir. ⓘ
Platin, altın ve diğer platin grubu metalleri içeren ham platinin saflaştırılması için uygun bir yöntem, içinde paladyum, altın ve platinin çözündüğü, osmiyum, iridyum, rutenyum ve rodyumun ise reaksiyona girmeden kaldığı aqua regia ile işlemektir. Altın, demir (II) klorür ilavesiyle çöktürülür ve altın süzüldükten sonra platin, amonyum klorür ilavesiyle amonyum kloroplatinat olarak çöktürülür. Amonyum kloroplatinat ısıtılarak platine dönüştürülebilir. Çökelmemiş hekzakloroplatinat (IV) elementel çinko ile indirgenebilir ve benzer bir yöntem laboratuvar artıklarından küçük ölçekli platin geri kazanımı için uygundur. Platin madenciliği ve rafine edilmesinin çevresel etkileri vardır. ⓘ
Uygulamalar

2014 yılında satılan 218 ton platinin 98 tonu araç emisyon kontrol cihazları (%45), 74,7 tonu mücevherat (%34), 20,0 tonu kimyasal üretim ve petrol rafinasyonu (%9,2) ve 5,85 tonu sabit disk sürücüleri gibi elektrik uygulamaları (%2,7) için kullanılmıştır. Kalan 28,9 ton ise tıp ve biyotıp, cam yapım ekipmanları, yatırım, elektrotlar, antikanser ilaçlar, oksijen sensörleri, bujiler ve türbin motorları gibi çeşitli diğer küçük uygulamalara gitti. ⓘ
Katalizör
Platinin en yaygın kullanımı, genellikle platin siyahı olarak kimyasal reaksiyonlarda katalizör olarak kullanılmasıdır. Hidrojenin tutuşmasını katalize etmek için platin tozunun kullanıldığı 19. yüzyılın başlarından beri katalizör olarak kullanılmaktadır. En önemli uygulaması otomobillerde egzozdan çıkan düşük konsantrasyonlardaki yanmamış hidrokarbonların karbondioksit ve su buharına tamamen yanmasını sağlayan katalitik konvertördür. Platin ayrıca petrol endüstrisinde bir dizi ayrı işlemde katalizör olarak kullanılır, ancak özellikle aromatik bileşikler açısından zengin hale gelen daha yüksek oktanlı benzine düz akışlı naftaların katalitik reformasyonunda kullanılır. Adams katalizörü olarak da bilinen PtO2, özellikle bitkisel yağlar için bir hidrojenasyon katalizörü olarak kullanılır. Platin ayrıca hidrojen peroksitin su ve oksijene ayrışmasını güçlü bir şekilde katalize eder ve yakıt hücrelerinde oksijenin indirgenmesi için bir katalizör olarak kullanılır. ⓘ
Standart

1889'dan 1960'a kadar metre, uluslararası prototip metre olarak bilinen platin-iridyum (90:10) alaşımlı bir çubuğun uzunluğu olarak tanımlanmıştır. Bir önceki çubuk 1799 yılında platinden yapılmıştı. Mayıs 2019'a kadar kilogram, 1879'da yapılan aynı platin-iridyum alaşımından bir silindir olan kilogramın uluslararası prototipinin kütlesi olarak tanımlanıyordu. ⓘ
Standart Platin Direnç Termometresi (SPRT), sıcaklık ölçümleri için uluslararası kalibrasyon standardı olan 1990 Uluslararası Sıcaklık Ölçeğini (ITS-90) tanımlamak için kullanılan dört termometre türünden biridir. Termometredeki direnç teli saf platinden yapılmıştır (NIST, telleri ağırlıkça %99,999 kimyasal saflığa sahip platin çubuk stokundan üretmiştir). Laboratuvar kullanımlarına ek olarak, Platin Direnç Termometresinin (PRT) birçok endüstriyel uygulaması da vardır, endüstriyel standartlar arasında ASTM E1137 ve IEC 60751 bulunmaktadır. ⓘ
Standart hidrojen elektrodu da korozyon direnci ve diğer özellikleri nedeniyle platinleştirilmiş platin elektrot kullanır. ⓘ
Bir yatırım olarak
Platin değerli bir metal emtiadır; külçeleri XPT ISO para birimi koduna sahiptir. Sikkeler, çubuklar ve külçeler alınıp satılır veya toplanır. Platin, inertliği nedeniyle genellikle %90-95 alaşım olarak mücevherlerde kullanılır. Bu amaçla prestiji ve doğal külçe değeri için kullanılır. Mücevher ticareti yayınları, platin ürünlerin değerini artırmak amacıyla kuyumculara küçük yüzey çiziklerini (patina olarak adlandırdıkları) arzu edilen bir özellik olarak sunmalarını tavsiye etmektedir. ⓘ
Saatçilikte Vacheron Constantin, Patek Philippe, Rolex, Breitling ve diğer şirketler sınırlı sayıda üretilen saat serilerini üretmek için platin kullanmaktadır. Saat yapımcıları platinin eşsiz özelliklerini takdir etmektedir, çünkü platin ne kararır ne de aşınır (altına göre ikinci kalite). ⓘ
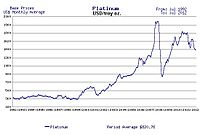
Sürekli ekonomik istikrar ve büyüme dönemlerinde platin fiyatı altın fiyatının iki katına kadar çıkma eğilimi gösterirken, ekonomik belirsizlik dönemlerinde platin fiyatı azalan endüstriyel talep nedeniyle düşme eğilimi göstererek altın fiyatının altına inmektedir. Altın güvenli bir liman olarak görüldüğünden, ekonominin durgun olduğu dönemlerde altın fiyatları daha istikrarlıdır. Altın endüstriyel uygulamalarda, özellikle iletken olarak kullanılması nedeniyle elektronikte de kullanılsa da, talebi endüstriyel kullanımlardan kaynaklanmamaktadır. 18. yüzyılda platinin nadir bulunması, Fransa Kralı XV. Louis'nin onu krallara layık tek metal ilan etmesine neden olmuştur. ⓘ
1992-2012 yılları arasında troy ons başına ABD doları cinsinden ortalama platin fiyatı ⓘ
Diğer kullanımlar
Laboratuvar kaplarının, bozunmaya dayanıklı gereçlerin, tellerin ve ısıluçların yapımında, kuyumculukta, diş hekimliğinde ve elektrik kontaklarında kullanılır. Platin-kobalt alaşımları güçlü manyetik özellik gösterir. Platin rezistans telleri, çok yüksek sıcaklıklarda çalışan elektrikli fırınların yapımında kullanılır. Arabalarda hava kirliliğini önleyici donanımların yapımında, füzelerin uç konilerinin ve jet motorlarının ağızlıklarının kaplamasında, büyük gemilerin, denizaltı boru hatlarının ve çelik desteklerin katodik koruma sistemlerinde de platinden yararlanılır. Sülfürik asit eldesinde ve petrol ürünlerinin işlenmesinde katalizör olarak platin kullanılmaktadır. Platin dirençli termometreler, elektrolizde kullanılan elektrotlarda da yer alıyor. ⓘ
Platin bileşiklerininse daha da yaygın kullanım alanları bulunur. Örneğin sisplatin, karboplatin ve okzaliplatinin DNA yapısı arasına girme özelliklerinden dolayı kanser tedavisinde kemoterapi sırasında kullanılabiliyor. Hekza kloroplatin asitse fotoğrafçılık, aynalar, mürekkep, porselen renklendirmesi, çinkonun aşındırılmasında kullanılmaktadır. ⓘ
Pazarlamada prestij sembolü
Platinin nadir bulunan bir metal olması, reklamcıların onu ayrıcalık ve zenginlikle ilişkilendirmesine neden olmuştur. "Platin" banka ve kredi kartları "altın" kartlardan daha fazla ayrıcalığa sahiptir. "Platin ödüller", "altın", "gümüş" ve "bronz "un üzerinde, ancak elmasın altında yer alan, mümkün olan en yüksek ikinci ödüldür. Örneğin, Amerika Birleşik Devletleri'nde 1 milyondan fazla satan bir müzik albümü "platin" olarak değerlendirilirken, 10 milyondan fazla satan bir albüm "elmas" olarak sertifikalandırılır. Karıştırıcılar ve araçlar gibi gümüşi beyaz renge sahip bazı ürünler "platin" olarak tanımlanır. Platin, kullanımı altın veya gümüş kadar yaygın olmasa da değerli bir metal olarak kabul edilir. Ana Kraliçe Elizabeth'in Kral VI George'un eşi olarak taç giyme töreni için üretilen tacının çerçevesi platinden yapılmıştır. Bu özel metalden yapılan ilk İngiliz tacıdır. ⓘ
Sağlık sorunları
Hastalık Kontrol ve Önleme Merkezlerine göre, platin tuzlarına kısa süreli maruziyet gözlerde, burunda ve boğazda tahrişe neden olabilir ve uzun süreli maruziyet hem solunum hem de cilt alerjilerine neden olabilir. Mevcut OSHA standardı, 8 saatlik bir çalışma vardiyası boyunca ortalama metreküp hava başına 2 mikrogramdır. Ulusal Mesleki Güvenlik ve Sağlık Enstitüsü platin için tavsiye edilen maruz kalma sınırını (REL) 8 saatlik bir iş gününde 1 mg/m3 olarak belirlemiştir. ⓘ
Platin, çeşitli tıbbi implantların (meme implantları, eklem replasman protezleri, yapay bel diskleri, vasküler erişim portları, vb) silikon kauçuk ve jel bileşenlerinin üretiminde bir katalizör olduğundan, platinin vücuda girme ve olumsuz etkilere neden olma olasılığı araştırılmaya değer bulunmuştur. Gıda ve İlaç İdaresi ve diğer kurumlar konuyu incelemiş ve in vivo toksisiteye işaret eden herhangi bir kanıt bulamamıştır. Kimyasal olarak sınırlandırılmamış platin FDA tarafından "sahte bir kanser 'tedavisi'" olarak tanımlanmıştır. Yanlış anlaşılma, metalin adını cisplatin gibi platin bazlı kemoterapi ilaçları için uygunsuz bir şekilde argo terim olarak kullanan sağlık çalışanları tarafından yaratılmaktadır. Bunlar platin bileşikleridir, metalin kendisi değil. ⓘ
Önlemler
Platin reaktif bir metal olmadığından herhangi bir sağlık problemi yaratmaz. Bazı platin kompleksleri (cis-platin), anti-tümör aktivitelerinden dolayı kemoterapi alanında kullanılmakta iseler de böbreklerde geri dönüşümü olmayan tahribata yol açarlar. ⓘ