Çinko
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Çinko | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Görünüş | gümüş-gri | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Standart atom ağırlığı Ar°(Zn) |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Periyodik tabloda çinko | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atom numarası (Z) | 30 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grup | Grup 12 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dönem | dönem 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | d-blok | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektron konfigürasyonu | [[[Argon|Ar]]] 3d10 4s2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kabuk başına elektron | 2, 8, 18, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fiziksel özellikler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| STP'de Faz | katı | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Erime noktası | 692,68 K (419,53 °C, 787,15 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kaynama noktası | 1180 K (907 °C, 1665 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Yoğunluk (r.t.'ye yakın) | 7,14 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| sıvı olduğunda (m.p.'de) | 6,57 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Füzyon ısısı | 7,32 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Buharlaşma ısısı | 115 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar ısı kapasitesi | 25.470 J/(mol-K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Buhar basıncı
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomik özellikler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oksidasyon durumları | -2, 0, +1, +2 (amfoterik bir oksit) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegatiflik | Pauling ölçeği: 1.65 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| İyonlaşma enerjileri |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomik yarıçap | ampi̇ri̇k: 134 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalent yarıçap | 122±4 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waals yarıçapı | 139 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Çinkonun spektral çizgileri | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Diğer özellikler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Doğal oluşum | ilkel | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristal yapı | altıgen yakın paketlenmiş (hcp) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ses hızı ince çubuk | 3850 m/s (r.t.'de) (yuvarlanmış) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termal genleşme | 30,2 µm/(m⋅K) (25 °C'de) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termal iletkenlik | 116 W/(m⋅K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektriksel direnç | 59,0 nΩ⋅m (20 °C'de) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Manyetik sipariş | diamanyetik | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar manyetik duyarlılık | -11,4×10-6 cm3/mol (298 K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Young modülü | 108 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kayma modülü | 43 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Yığın modülü | 70 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Poisson oranı | 0.25 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohs sertliği | 2.5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brinell sertliği | 327-412 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS Numarası | 7440-66-6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tarih | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Keşif | Hintli metalürjistler (MÖ 1000'den önce) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| İlk izolasyon | Andreas Sigismund Marggraf (1746) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tarafından benzersiz bir metal olarak tanınmıştır | Rasaratna Samuccaya (1300) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Çinkonun ana izotopları | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Çinko, sembolü Zn ve atom numarası 30 olan kimyasal bir elementtir. Çinko oda sıcaklığında hafif kırılgan bir metaldir ve oksidasyon giderildiğinde gümüşi grimsi bir görünüme sahiptir. Periyodik tablonun 12. grubundaki (IIB) ilk elementtir. Bazı açılardan çinko kimyasal olarak magnezyuma benzer: her iki element de yalnızca bir normal oksidasyon durumu (+2) sergiler ve Zn2+ ve Mg2+ iyonları benzer boyuttadır. Çinko, yerkabuğunda en bol bulunan 24. elementtir ve beş kararlı izotopa sahiptir. En yaygın çinko cevheri, bir çinko sülfür minerali olan sfalerittir (çinko blende). En büyük işlenebilir lodlar Avustralya, Asya ve Amerika Birleşik Devletleri'ndedir. Çinko, cevherin köpük flotasyonu, kavurma ve elektrik kullanılarak son ekstraksiyon (elektrowinning) ile rafine edilir. ⓘ
ÇeĢitli oranlarda bakır ve çinko alaĢımı olan pirinç, MÖ üçüncü bin yılın baĢlarında Ege bölgesinde ve günümüzde Irak, BirleĢik Arap Emirlikleri, Kalmıkya, Türkmenistan ve Gürcistan'ı kapsayan bölgede kullanılmıĢtır. MÖ ikinci binyılda ise günümüzde Batı Hindistan, Özbekistan, İran, Suriye, Irak ve İsrail'i kapsayan bölgelerde kullanılmıştır. Antik Romalılar ve Yunanlılar tarafından bilinmesine rağmen çinko metali Hindistan'da 12. yüzyıla kadar büyük ölçekte üretilmemiştir. Rajasthan madenleri M.Ö. 6. yüzyıla kadar uzanan çinko üretimine dair kesin kanıtlar sunmaktadır. Bugüne kadar saf çinkoya dair en eski kanıtlar, saf çinko elde etmek için damıtma işleminin kullanıldığı MS 9. yüzyılın başlarında Rajasthan'daki Zawar'dan gelmektedir. Simyacılar çinkoyu havada yakarak "filozof yünü" ya da "beyaz kar" dedikleri şeyi oluşturmuşlardır. ⓘ
Element muhtemelen simyacı Paracelsus tarafından Almanca Zinke (çatal, diş) kelimesinden esinlenerek adlandırılmıştır. Alman kimyager Andreas Sigismund Marggraf 1746 yılında saf metalik çinkoyu keşfetmesiyle tanınır. Luigi Galvani ve Alessandro Volta'nın çalışmaları 1800 yılında çinkonun elektrokimyasal özelliklerini ortaya çıkarmıştır. Demirin korozyona dayanıklı çinko kaplaması (sıcak daldırma galvanizleme) çinko için başlıca uygulamadır. Diğer uygulamalar elektrikli bataryalar, küçük yapısal olmayan dökümler ve pirinç gibi alaşımlardır. Çinko karbonat ve çinko glukonat (besin takviyesi olarak), çinko klorür (deodorantlarda), çinko piritiyon (kepek önleyici şampuanlarda), çinko sülfür (ışıldayan boyalarda) ve organik laboratuvarda dimetil çinko veya dietil çinko gibi çeşitli çinko bileşikleri yaygın olarak kullanılmaktadır. ⓘ
Çinko, doğum öncesi ve sonrası gelişim için gerekli olan temel bir mineraldir. Çinko eksikliği gelişmekte olan dünyada yaklaşık iki milyar insanı etkilemekte ve birçok hastalıkla ilişkilendirilmektedir. Çocuklarda eksikliği büyüme geriliğine, cinsel olgunlaşmanın gecikmesine, enfeksiyona yatkınlığa ve ishale neden olur. Reaktif merkezinde çinko atomu bulunan enzimler, insanlardaki alkol dehidrojenaz gibi biyokimyada yaygındır. Fazla çinko tüketimi ataksi, uyuşukluk ve bakır eksikliğine neden olabilir. ⓘ
Çinko (Latince: Zinkum, İngilizce: Zinc, Almanca: Zink), eski kaynaklarda Tutya (Osmanlıca: توتيا), mavimsi açık gri renkte, kırılgan bir metal. Elementlerin periyodik tablosunda geçiş elementleri grubunda yer alır. Düşük kaynama sıcaklığı dikkat çekicidir. Bu değer özellikle pirometalurjik metal üretiminde çok belirleyici bir etmendir. Dökülmüş halde sert ve kırılgandır. 120 °C'de şekillendirilebilir. Elektrokimyasal potansiyel dizisinde demirden daha negatif değerdedir. Böylece çinko anot olarak katodik korozyon korumada önemli bir kullanım bulur. Galvanizleme bu tür uygulamalardan biridir. ⓘ
Özellikleri
Fiziksel özellikler
Çinko mavimsi-beyaz, parlak, diyamanyetik bir metaldir, ancak metalin en yaygın ticari kaliteleri mat bir yüzeye sahiptir. Demirden biraz daha az yoğundur ve her atomun kendi düzleminde altı en yakın komşuya (265,9 pm'de) ve 290,6 pm'lik daha büyük bir mesafede altı diğerine sahip olduğu çarpıtılmış bir altıgen yakın paketleme biçimine sahip altıgen bir kristal yapıya sahiptir. Metal çoğu sıcaklıkta sert ve kırılgandır ancak 100 ila 150 °C arasında dövülebilir hale gelir. 210 °C'nin üzerinde metal tekrar kırılgan hale gelir ve dövülerek toz haline getirilebilir. Çinko iyi bir elektrik iletkenidir. Bir metal için çinko nispeten düşük erime (419,5 °C) ve kaynama noktalarına (907 °C) sahiptir. Erime noktası, cıva ve kadmiyum dışında tüm d-blok metalleri arasında en düşük olanıdır; bu nedenle çinko, kadmiyum ve cıva, diğer d-blok metalleri gibi geçiş metalleri olarak kabul edilmez. ⓘ
Pirinç de dahil olmak üzere birçok alaşım çinko içerir. Çinko ile ikili alaşımlar oluşturduğu uzun zamandır bilinen diğer metaller alüminyum, antimon, bizmut, altın, demir, kurşun, cıva, gümüş, kalay, magnezyum, kobalt, nikel, tellür ve sodyumdur. Ne çinko ne de zirkonyum ferromanyetik olmamasına rağmen, alaşımları ZrZn
2, 35 K'nin altında ferromanyetizma sergiler. ⓘ
Oluşum
Çinko yerkabuğunun yaklaşık 75 ppm'ini (%0,0075) oluşturur ve bu da onu en bol bulunan 24. element yapar. Çinkonun tipik arka plan konsantrasyonları atmosferde 1 μg/m3'ü; toprakta 300 mg/kg'ı; bitki örtüsünde 100 mg/kg'ı; tatlı suda 20 μg/L'yi ve deniz suyunda 5 μg/L'yi geçmez. Element normalde cevherlerde bakır ve kurşun gibi diğer baz metallerle birlikte bulunur. Çinko bir kalkofildir, yani elementin minerallerde hafif kalkojen oksijen veya halojenler gibi kalkojen olmayan elektronegatif elementlerden ziyade kükürt ve diğer ağır kalkojenlerle birlikte bulunma olasılığı daha yüksektir. Sülfürler, Dünya'nın erken atmosferinin indirgeyici koşulları altında kabuk katılaştıkça oluşmuştur. Bir çinko sülfür formu olan sfalerit, konsantresi %60-62 çinko içerdiğinden en çok çıkarılan çinko içeren cevherdir. ⓘ
Çinko için diğer kaynak mineraller arasında smithsonit (çinko karbonat), hemimorfit (çinko silikat), wurtzit (başka bir çinko sülfür) ve bazen hidrozinkit (bazik çinko karbonat) bulunur. Wurtzite haricinde, tüm bu diğer mineraller ilkel çinko sülfürlerin ayrışmasıyla oluşmuştur. ⓘ
Tanımlanmış dünya çinko kaynakları toplamı yaklaşık 1,9-2,8 milyar tondur. En büyük rezervler İran'da olmak üzere Avustralya, Kanada ve Amerika Birleşik Devletleri'nde büyük yataklar bulunmaktadır. Çinko için en son rezerv tahmini (mevcut madencilik ve üretim uygulamalarıyla ilgili belirlenmiş minimum fiziksel kriterleri karşılayan) 2009 yılında yapılmış ve yaklaşık 480 Mt olarak hesaplanmıştır. Çinko rezervleri ise, jeolojik olarak tanımlanmış ve geri kazanım için uygunluğu ekonomik olarak (konum, tenör, kalite ve miktar) belirlenmiş cevher kütleleridir. Arama ve maden geliştirme devam eden bir süreç olduğundan, çinko rezervlerinin miktarı sabit bir sayı değildir ve çinko cevheri arzının sürdürülebilirliği, günümüz çinko madenlerinin toplam maden ömrünün tahmin edilmesiyle değerlendirilemez. Bu kavram, rafine çinko üretiminin 1990 ve 2010 yılları arasında %80 artmasına rağmen çinko rezerv ömrünün değişmediğini gösteren Amerika Birleşik Devletleri Jeolojik Araştırmalar Kurumu (USGS) verileriyle de desteklenmektedir. Tarih boyunca 2002 yılına kadar yaklaşık 346 milyon ton çıkarılmıştır ve bilim adamları yaklaşık 109-305 milyon tonun kullanımda olduğunu tahmin etmektedir. ⓘ

İzotoplar
Doğada beş kararlı çinko izotopu bulunur ve 64Zn en bol bulunan izotoptur (%49,17 doğal bolluk). Doğada bulunan diğer izotoplar 66
Zn (%27,73), %67
Zn (%4,04), %68
Zn (%18,45) ve %70
Zn (%0,61). ⓘ
Birkaç düzine radyoizotop karakterize edilmiştir. 65
Yarılanma ömrü 243,66 gün olan Zn en az aktif radyoizotoptur ve onu 72
Yarılanma ömrü 46,5 saat olan Zn. Çinkonun 10 nükleer izomeri vardır. 69mZn, 13,76 saat ile en uzun yarı ömre sahiptir. m üst simgesi, yarı kararlı bir izotopu gösterir. Yarı kararlı bir izotopun çekirdeği uyarılmış bir durumdadır ve gama ışını şeklinde bir foton yayarak temel duruma dönecektir. 61
Zn üç uyarılmış metastabil duruma sahiptir ve 73
Zn'de iki tane vardır. İzotoplar 65
Zn, 71
Zn, 77
Zn ve 78
Zn'nin her biri yalnızca bir uyarılmış metastabil duruma sahiptir. ⓘ
Kütle numarası 66'dan düşük olan bir çinko radyoizotopunun en yaygın bozunma modu elektron yakalamadır. Elektron yakalamadan kaynaklanan bozunma ürünü bir bakır izotopudur. ⓘ
- n
30Zn
+
e-
→ n
29Cu ⓘ
Kütle numarası 66'dan büyük olan bir çinko radyoizotopunun en yaygın bozunma modu, bir galyum izotopu üreten beta bozunmasıdır (β-).
- n
30Zn
→ n
31Ga
+
e-
+
ν
e ⓘ
Bileşikler ve kimya
Reaktivite
Çinko, [Ar]3d104s2 elektron konfigürasyonuna sahiptir ve periyodik tablonun 12. grubunun bir üyesidir. Orta derecede reaktif bir metal ve güçlü bir indirgeyici maddedir. Saf metalin yüzeyi hızla kararır ve sonunda bazik çinko karbonattan koruyucu bir pasifleştirici tabaka oluşturur, Zn
5(OH)
6(CO3)
2, atmosferik karbondioksit ile reaksiyona girerek. ⓘ
Çinko havada parlak mavimsi-yeşil bir alevle yanar ve çinko oksit dumanları çıkarır. Çinko asitlerle, alkalilerle ve diğer metal olmayan maddelerle kolayca reaksiyona girer. Son derece saf çinko oda sıcaklığında asitlerle sadece yavaş reaksiyona girer. Hidroklorik veya sülfürik asit gibi güçlü asitler pasifleştirici tabakayı kaldırabilir ve asitle sonraki reaksiyon hidrojen gazı açığa çıkarır. ⓘ
Çinkonun kimyasına +2 oksidasyon durumu hakimdir. Bu oksidasyon durumundaki bileşikler oluştuğunda, dış kabuk elektronları kaybolur ve [Ar]3d10 elektronik konfigürasyonuna sahip çıplak bir çinko iyonu verir. Sulu çözeltide bir oktahedral kompleks, [Zn(H
2O)6]2+
baskın türdür. Çinkonun 285 °C'nin üzerindeki sıcaklıklarda çinko klorür ile birlikte uçması, Zn
2Cl
2, +1 oksidasyon durumuna sahip bir çinko bileşiği. Çinkonun +1 veya +2 dışındaki pozitif oksidasyon durumlarında hiçbir bileşiği bilinmemektedir. Hesaplamalar, +4 oksidasyon durumuna sahip bir çinko bileşiğinin var olma ihtimalinin düşük olduğunu göstermektedir. Zn(III)'ün güçlü elektronegatif trianyonların varlığında var olabileceği tahmin edilmektedir; ancak bu olasılıkla ilgili bazı şüpheler vardır. Ancak 2021'de ZnBeB11(CN)12 formülüyle +3 oksidasyon durumuna sahip daha fazla kanıt içeren başka bir bileşik rapor edildi. ⓘ
Çinko kimyası, geç birinci sıra geçiş metalleri olan nikel ve bakırın kimyasına benzer, ancak dolu bir d-kabuğuna sahiptir ve bileşikler diyamanyetik ve çoğunlukla renksizdir. Çinko ve magnezyumun iyonik yarıçapları neredeyse aynıdır. Bu nedenle bazı eşdeğer tuzlar aynı kristal yapıya sahiptir ve iyonik yarıçapın belirleyici bir faktör olduğu diğer durumlarda çinkonun kimyası magnezyumunkiyle çok fazla ortak noktaya sahiptir. Diğer açılardan, geç birinci sıra geçiş metalleri ile çok az benzerlik vardır. Çinko, N- ve S- donörleri ile daha yüksek derecede kovalent bağlar ve çok daha kararlı kompleksler oluşturma eğilimindedir. Çinko kompleksleri çoğunlukla 4- veya 6- koordinatlıdır, ancak 5-koordinatlı kompleksler de bilinmektedir. ⓘ
Çinko(I) bileşikleri
Çinko(I) bileşikleri nadirdir ve düşük oksidasyon durumunu stabilize etmek için hacimli ligandlara ihtiyaç duyarlar. Çoğu çinko(I) bileşiği, cıva(I) bileşiklerinde bulunan [Hg2]2+ dimerik katyonuna benzeyen resmi olarak [Zn2]2+ çekirdeği içerir. İyonun diyamanyetik doğası dimerik yapısını doğrulamaktadır. Zn-Zn bağı içeren ilk çinko(I) bileşiği, (η5-C5Me5)2Zn2, aynı zamanda ilk dimetallosendir. Zn2]2+ iyonu hızla çinko metali ve çinko(II)'ye ayrışır ve sadece erimiş ZnCl2 içindeki metalik çinko çözeltisinin soğutulmasıyla sarı diamanyetik bir camda elde edilmiştir. ⓘ
Çinko(II) bileşikleri


Çinkonun ikili bileşikleri, metaloidlerin çoğu ve soy gazlar hariç tüm ametaller için bilinmektedir. ZnO oksit, nötr sulu çözeltilerde neredeyse çözünmeyen beyaz bir tozdur, ancak amfoteriktir, hem güçlü bazik hem de asidik çözeltilerde çözünür. Diğer kalkojenitler (ZnS, ZnSe ve ZnTe) elektronik ve optikte çeşitli uygulamalara sahiptir. Piktojenitler (Zn
3N
2, Zn
3P
2, Zn
3As
2 ve Zn
3Sb
2), peroksit (ZnO
2), hidrür (ZnH
2) ve karbür (ZnC
2) de bilinmektedir. Dört halojenürden ZnF
2 en iyonik karaktere sahipken, diğerleri (ZnCl
2, ZnBr
2 ve ZnI
2) nispeten düşük erime noktalarına sahiptir ve daha kovalent karaktere sahip oldukları kabul edilir. ⓘ
Zn2+ içeren zayıf bazik çözeltilerde
iyonları, hidroksit Zn(OH)
2 beyaz bir çökelti olarak oluşur. Daha güçlü alkali çözeltilerde, bu hidroksit çözünerek çinkoatlar ([Zn(OH)4]2-
). Nitrat Zn(NO3)
2, klorat Zn(ClO3)
2, sülfat ZnSO
4, fosfat Zn
3(PO4)
2, molibdat ZnMoO
4, siyanür Zn(CN)
2, arsenit Zn(AsO2)
2, arsenat Zn(AsO4)
2-8H
2O ve kromat ZnCrO
4 (birkaç renkli çinko bileşiğinden biri) çinkonun diğer yaygın inorganik bileşiklerine birkaç örnektir. ⓘ
Organozinc bileşikleri, çinko-karbon kovalent bağları içerenlerdir. Dietil çinko ((C
2H5)
2Zn) sentetik kimyada bir reaktiftir. İlk olarak 1848 yılında çinko ve etil iyodür reaksiyonundan rapor edilmiştir ve bir metal-karbon sigma bağı içerdiği bilinen ilk bileşiktir. ⓘ
Çinko için test
Kobaltisiyanid kağıdı (Rinnmann'ın Zn testi) çinko için kimyasal bir indikatör olarak kullanılabilir. 4 g K3Co(CN)6 ve 1 g KClO3 100 ml suda çözülür. Kağıt çözeltiye daldırılır ve 100 °C'de kurutulur. Numuneden bir damla kuru kağıdın üzerine damlatılır ve ısıtılır. Yeşil bir disk çinko varlığını gösterir. ⓘ
Tarih
Eski kullanım
MS 300 ila 500 yılları arasında yazıldığı düşünülen Charaka Samhita, oksitlendiğinde çinko oksit olduğu düşünülen pushpanjan üreten bir metalden bahseder. Hindistan'da Udaipur yakınlarındaki Zawar'da bulunan çinko madenleri Mauryan döneminden beri (M.Ö. 322 ve 187) aktiftir. Ancak burada metalik çinkonun eritilmesi MS 12. yüzyıl civarında başlamış gibi görünmektedir. Bir tahmine göre bu bölgede 12. ve 16. yüzyıllar arasında yaklaşık bir milyon ton metalik çinko ve çinko oksit üretilmiştir. Bir başka tahmine göre ise bu dönemde toplam 60.000 ton metalik çinko üretilmiştir. Yaklaşık olarak MS 13. yüzyılda yazılmış olan Rasaratna Samuccaya, iki tür çinko içeren cevherden bahseder: biri metal çıkarımı için, diğeri ise tıbbi amaçlar için kullanılır. ⓘ

Antik çağlarda saf olmayan çinko kullanımına dair çeşitli izole örnekler keşfedilmiştir. Çinko cevherleri, çinkonun ayrı bir element olarak keşfedilmesinden binlerce yıl önce çinko-bakır alaşımı pirinç yapımında kullanılmıştır. MÖ 14. ila 10. yüzyıllara ait Judean pirinci %23 çinko içermektedir. ⓘ
Pirinç üretme bilgisi M.Ö. 7. yüzyılda Antik Yunan'a yayılmış, ancak çok az çeşit üretilmiştir. Kurşun, demir, antimon ve diğer metallerin geri kalanını oluşturduğu %80-90 çinko içeren alaşımlardan yapılmış 2.500 yıllık süs eşyaları bulunmuştur. Bir Daçya arkeolojik alanında %87,5 çinko içeren muhtemelen tarih öncesi bir heykelcik bulunmuştur. ⓘ
Bilinen en eski haplar çinko karbonatlar olan hidrozinkit ve smithsonitten yapılmıştır. Bu haplar göz ağrısı için kullanılmış ve M.Ö. 140 yılında batan Relitto del Pozzino adlı Roma gemisinde bulunmuştur. ⓘ
Pirinç üretimi Romalılar tarafından yaklaşık MÖ 30'da biliniyordu. Toz halindeki kalamin (çinko silikat veya karbonat), odun kömürü ve bakırı bir potada ısıtarak pirinç yapıyorlardı. Elde edilen kalamin pirinci daha sonra silah yapımında kullanılmak üzere dökülüyor ya da dövülerek şekillendiriliyordu. Hıristiyanlık döneminde Romalılar tarafından basılan bazı sikkeler muhtemelen kalamin pirincinden yapılmıştır. ⓘ
MÖ 1. yüzyılda yazan Strabon (ancak MÖ 4. yüzyıl tarihçisi Theopompus'un artık kayıp olan bir eserinden alıntı yaparak) bakırla karıştırıldığında pirinç yapan "sahte gümüş damlalarından" bahseder. Bu, sülfürlü cevherlerin eritilmesinin bir yan ürünü olan küçük miktarlardaki çinkoya atıfta bulunuyor olabilir. Eritme fırınlarındaki bu tür kalıntılarda bulunan çinko, değersiz olduğu düşünüldüğünden genellikle atılırdı. ⓘ
Berne çinko tableti, Roma Galya'sına tarihlenen ve çoğunlukla çinko olan bir alaşımdan yapılmış bir adak levhasıdır. ⓘ
İlk çalışmalar ve isimlendirme
Çinko, Hindu kralı Madanapala'ya (Taka hanedanından) atfedilen ve yaklaşık 1374 yılında yazılan tıp sözlüğünde Yasada veya Jasada adı altında belirgin bir metal olarak tanınmıştır. Kalaminin yün ve diğer organik maddelerle indirgenmesi yoluyla saf olmayan çinkonun eritilmesi ve ekstraksiyonu 13. yüzyılda Hindistan'da gerçekleştirilmiştir. Çinliler bu tekniği 17. yüzyıla kadar öğrenememişlerdir. ⓘ
Simyacılar çinko metalini havada yakmış ve ortaya çıkan çinko oksidi bir kondansatörde toplamışlardır. Bazı simyacılar bu çinko okside Latince "filozof yünü" anlamına gelen lana philosophica adını verdiler, çünkü yün tutamlar halinde toplanıyordu, diğerleri ise beyaz kara benzediğini düşündüler ve nix album adını verdiler. ⓘ
Metalin adı muhtemelen ilk olarak 16. yüzyılda Liber Mineralium II adlı kitabında metalden "zincum" veya "zinken" olarak bahseden İsviçre doğumlu Alman simyacı Paracelsus tarafından belgelenmiştir. Kelime muhtemelen Almanca zinke'den türetilmiştir ve "diş benzeri, sivri veya pürüzlü" anlamına geldiği varsayılmaktadır (metalik çinko kristalleri iğneye benzer bir görünüme sahiptir). Zink, kalay anlamına gelen Almanca zinn ile ilişkisi nedeniyle "kalay benzeri" anlamına da gelebilir. Bir başka olasılık da kelimenin Farsça taş anlamına gelen سنگ seng kelimesinden türetilmiş olmasıdır. Metal ayrıca Hint kalayı, tutanego, kalamin ve spinter olarak da adlandırılmıştır. ⓘ
Alman metalürji uzmanı Andreas Libavius, 1596 yılında Portekizlilerden ele geçirilen bir yük gemisinden Malabar'ın "kalay" adını verdiği metalden bir miktar aldı. Libavius, çinko olabileceği düşünülen numunenin özelliklerini tanımlamıştır. Çinko, 17. yüzyılda ve 18. yüzyılın başlarında Doğu'dan Avrupa'ya düzenli olarak ithal ediliyordu, ancak zaman zaman çok pahalıydı. ⓘ
İzolasyon

Metalik çinko Hindistan'da MS 1300 yılında, Batı'dakinden çok daha önce izole edilmiştir. Avrupa'da izole edilmeden önce, yaklaşık MS 1600 yılında Hindistan'dan ithal edilmiştir. Avrupa'daki teknolojik bilgileri veren çağdaş bir kaynak olan Postlewayt'in Evrensel Sözlüğü 1751'den önce çinkodan bahsetmemiştir, ancak element o zamandan önce incelenmiştir. ⓘ
Flaman metalürjist ve simyacı P. M. de Respour 1668 yılında çinko oksitten metalik çinko elde ettiğini bildirmiştir. Étienne François Geoffroy, 18. yüzyılın başlarında çinko oksidin eritilmekte olan çinko cevherinin üzerine yerleştirilen demir çubuklar üzerinde sarı kristaller halinde nasıl yoğunlaştığını tarif etmiştir. İngiltere'de John Lane'in 1726'daki iflasından önce muhtemelen Landore'da çinko eritme deneyleri yaptığı söylenmektedir. ⓘ
1738'de Büyük Britanya'da William Champion, dikey retort tarzı bir izabe fırınında kalaminden çinko elde etmek için bir işlemin patentini almıştır. Tekniği Rajasthan'daki Zawar çinko madenlerinde kullanılan tekniğe benziyordu, ancak Doğu'yu ziyaret ettiğine dair bir kanıt yoktu. Champion'ın süreci 1851'e kadar kullanıldı. ⓘ
İsveçli kimyager Anton von Swab dört yıl önce kalaminden çinko damıtmış olsa da, Alman kimyager Andreas Marggraf normalde saf metalik çinkoyu keşfetmesiyle tanınır. Marggraf, 1746 yılında yaptığı deneyde kalamin ve odun kömürü karışımını bakır içermeyen kapalı bir kapta ısıtarak bir metal elde etti. Bu prosedür 1752'de ticari olarak pratik hale geldi. ⓘ
Daha sonraki çalışmalar

William Champion'ın kardeşi John, 1758 yılında çinko sülfürü kalsine ederek imbik işleminde kullanılabilecek bir okside dönüştüren bir işlemin patentini almıştır. Bundan önce çinko üretmek için sadece kalamin kullanılabiliyordu. 1798 yılında Johann Christian Ruberg ilk yatay imbik izabe fırınını inşa ederek eritme sürecini geliştirdi. Jean-Jacques Daniel Dony, Belçika'da daha da fazla çinko işleyen farklı bir yatay çinko izabe tesisi inşa etti. İtalyan doktor Luigi Galvani 1780 yılında, yeni kesilmiş bir kurbağanın omuriliğini pirinç bir kancayla tutturulmuş demir bir raya bağlamanın kurbağanın bacağının seğirmesine neden olduğunu keşfetti. Yanlışlıkla sinirlerin ve kasların elektrik üretme yeteneğini keşfettiğini düşündü ve bu etkiye "hayvan elektriği" adını verdi. Galvanik hücre ve galvanizleme süreci Luigi Galvani'nin adıyla anılmış ve keşifleri elektrik pilleri, galvanizleme ve katodik korumanın önünü açmıştır. ⓘ
Galvani'nin arkadaşı Alessandro Volta, bu etkiyi araştırmaya devam etti ve 1800 yılında Voltaik kazığı icat etti. Volta'nın kazığı, her biri bir elektrolitle birbirine bağlanmış bir bakır ve bir çinko plakadan oluşan basitleştirilmiş galvanik hücreler yığınından oluşuyordu. Bu birimlerin seri olarak istiflenmesiyle, Voltaik yığın (ya da "pil") bir bütün olarak daha yüksek bir gerilime sahip oluyor ve bu da tek hücrelerden daha kolay kullanılabiliyordu. Elektrik üretilir çünkü iki metal plaka arasındaki Volta potansiyeli elektronların çinkodan bakıra akmasına ve çinkoyu aşındırmasına neden olur. ⓘ
Çinkonun manyetik olmayan karakteri ve çözeltide renk vermemesi, biyokimya ve beslenme açısından öneminin keşfedilmesini geciktirmiştir. Bu durum 1940 yılında kandaki karbondioksiti temizleyen bir enzim olan karbonik anhidrazın aktif bölgesinde çinko bulunduğu gösterilince değişti. Sindirim enzimi karboksipeptidaz 1955 yılında bilinen ikinci çinko içeren enzim olmuştur. ⓘ
Üretim
Madencilik ve işleme
| Rütbe | Ülke | Ton |
|---|---|---|
| 1 | Çin | 4,210,000 |
| 2 | Peru | 1,400,000 |
| 3 | Avustralya | 1,330,000 |
| 5 | Birleşik Devletler | 753,000 |
| 4 | Hindistan | 720,000 |
| 6 | Meksika | 677,000 |

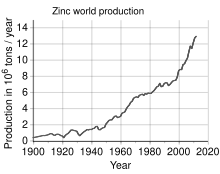
Çinko, yıllık yaklaşık 13 milyon tonluk üretimiyle demir, alüminyum ve bakırın ardından en yaygın kullanılan dördüncü metaldir. Dünyanın en büyük çinko üreticisi Avustralyalı OZ Minerals ve Belçikalı Umicore'un birleşmesinden oluşan Nyrstar'dır. Dünyadaki çinkonun yaklaşık %70'i madencilikten, kalan %30'u ise ikincil çinkonun geri dönüşümünden elde edilmektedir. Ticari olarak saf çinko, genellikle SHG olarak kısaltılan Özel Yüksek Sınıf olarak bilinir ve %99,995 oranında saftır. ⓘ
Dünya çapında yeni çinkonun %95'i sfaleritin (ZnS) neredeyse her zaman bakır, kurşun ve demir sülfürleriyle karıştığı sülfidik cevher yataklarından çıkarılmaktadır. Çinko madenleri dünyanın dört bir yanına dağılmış olup, başlıca bölgeler Çin, Avustralya ve Peru'dur. Çin 2014 yılında küresel çinko üretiminin %38'ini gerçekleştirmiştir. ⓘ
Çinko metali ekstraktif metalürji kullanılarak üretilir. Cevher ince öğütülür, daha sonra mineralleri gangdan ayırmak için (hidrofobiklik özelliğine göre) köpük flotasyonuna tabi tutulur ve yaklaşık %50 çinko, %32 kükürt, %13 demir ve %5 SiO içeren bir çinko sülfür cevheri konsantresi elde edilir.
2. ⓘ
Kavurma, çinko sülfür konsantresini çinko okside dönüştürür:
- Ayrıştırılamadı (sözdizim hatası): {\displaystyle \ce{2ZnS + 3O2 ->[t^o] 2ZnO + 2SO2 <span title="Kaynak: İngilizce Vikipedi, Bölüm "Mining and processing"" class="plainlinks">[https://en.wikipedia.org/wiki/Zinc#Mining_and_processing <span style="color:#dddddd">ⓘ</span>]</span>}}
Sülfür dioksit, liç işlemi için gerekli olan sülfürik asit üretimi için kullanılır. Çinko üretimi için çinko karbonat, çinko silikat veya çinko-spinel (Namibya'daki Skorpion Yatağı gibi) yatakları kullanılıyorsa, kavurma işlemi ihmal edilebilir. ⓘ
Daha ileri işlemler için iki temel yöntem kullanılır: pirometalurji veya elektrowinning. Pirometalurji, çinko oksidi karbon veya karbon monoksit ile 950 °C'de (1.740 °F) metale indirger ve bu sıcaklıklarda uçucu olmayan diğer metallerden ayırmak için çinko buharı olarak damıtılır. Çinko buharı bir yoğunlaştırıcıda toplanır. Aşağıdaki denklemler bu süreci açıklamaktadır:
- Ayrıştırılamadı (sözdizim hatası): {\displaystyle \ce{ZnO + CO ->[950^oC] Zn + CO2 <span title="Kaynak: İngilizce Vikipedi, Bölüm "Mining and processing"" class="plainlinks">[https://en.wikipedia.org/wiki/Zinc#Mining_and_processing <span style="color:#dddddd">ⓘ</span>]</span>}}
Elektrowinning işleminde, çinko cevher konsantresinden sülfürik asit ile süzülür ve safsızlıklar çökeltilir:
- Ayrıştırılamadı (sözdizim hatası): {\displaystyle \ce{ZnO + H2SO4 -> ZnSO4 + H2O <span title="Kaynak: İngilizce Vikipedi, Bölüm "Mining and processing"" class="plainlinks">[https://en.wikipedia.org/wiki/Zinc#Mining_and_processing <span style="color:#dddddd">ⓘ</span>]</span>}}
Son olarak, çinko elektroliz yoluyla indirgenir. ⓘ
- Ayrıştırılamadı (sözdizim hatası): {\displaystyle \ce{2ZnSO4 + 2H2O -> 2Zn + O2 + 2H2SO4 <span title="Kaynak: İngilizce Vikipedi, Bölüm "Mining and processing"" class="plainlinks">[https://en.wikipedia.org/wiki/Zinc#Mining_and_processing <span style="color:#dddddd">ⓘ</span>]</span>}}
Sülfürik asit yeniden üretilir ve liç adımına geri dönüştürülür. ⓘ
Galvanizli hammadde bir elektrik ark fırınına beslendiğinde, çinko, ağırlıklı olarak Waelz işlemi (2014 itibariyle %90) olmak üzere bir dizi işlemle tozdan geri kazanılır. ⓘ
Çevresel etki
Sülfidik çinko cevherlerinin rafine edilmesi büyük miktarlarda sülfür dioksit ve kadmiyum buharı üretir. İzabe cürufu ve diğer kalıntılar önemli miktarlarda metal içerir. Belçika'nın La Calamine ve Plombières kasabalarında 1806 ve 1882 yılları arasında yaklaşık 1,1 milyon ton metalik çinko ve 130 bin ton kurşun çıkarılmış ve eritilmiştir. Geçmişteki madencilik faaliyetlerinin çöplükleri çinko ve kadmiyum sızdırmakta ve Geul Nehri'nin tortuları önemsiz miktarlarda metal içermektedir. Yaklaşık iki bin yıl önce, madencilik ve eritme işlemlerinden kaynaklanan çinko emisyonları yılda toplam 10 bin tondu. Çinko emisyonları 1850'den itibaren 10 kat arttıktan sonra 1980'lerde yılda 3,4 milyon tonla zirve yapmış ve 1990'larda 2,7 milyon tona düşmüştür. 2005 yılında Kuzey Kutbu troposferinde yapılan bir çalışma buradaki konsantrasyonların düşüşü yansıtmadığını ortaya koymuştur. İnsan kaynaklı ve doğal emisyonlar 20'ye 1 oranında gerçekleşmektedir. ⓘ
Sanayi ve maden bölgelerinden akan nehirlerdeki çinko 20 ppm kadar yüksek olabilir. Etkili kanalizasyon arıtımı bunu büyük ölçüde azaltır; örneğin Ren Nehri boyunca yapılan arıtma çinko seviyelerini 50 ppb'ye kadar düşürmüştür. Çinkonun 2 ppm kadar düşük konsantrasyonları balıkların kanlarında taşıyabilecekleri oksijen miktarını olumsuz etkilemektedir. ⓘ
Madencilik, arıtma veya çinko içeren çamurla gübreleme nedeniyle çinko ile kirlenmiş topraklar, kilogram kuru toprak başına birkaç gram çinko içerebilir. Toprakta 500 ppm'i aşan çinko seviyeleri, bitkilerin demir ve manganez gibi diğer temel metalleri absorbe etme yeteneğini engeller. Bazı toprak örneklerinde 2000 ppm ila 180.000 ppm (%18) çinko seviyeleri kaydedilmiştir. ⓘ
Uygulamalar
Başlıca çinko uygulamaları şunlardır (sayılar ABD için verilmiştir)
Korozyon önleyici ve aküler

Çinko en yaygın olarak korozyon önleyici madde olarak kullanılır ve galvanizleme (demir veya çeliğin kaplanması) en bilinen şeklidir. Amerika Birleşik Devletleri'nde 2009 yılında çinko metalinin %55'i veya 893.000 tonu galvanizleme için kullanılmıştır. ⓘ
Çinko demir veya çelikten daha reaktiftir ve bu nedenle tamamen korozyona uğrayana kadar neredeyse tüm yerel oksidasyonu çekecektir. Oksit ve karbonattan oluşan koruyucu bir yüzey tabakası (Zn
5(OH)
6(CO
3)
2) çinko korozyona uğradıkça oluşur. Bu koruma çinko tabakası çizildikten sonra bile devam eder ancak çinko korozyona uğradıkça zamanla bozulur. Çinko elektrokimyasal olarak veya sıcak daldırma galvanizleme veya püskürtme yoluyla erimiş çinko olarak uygulanır. Galvanizleme zincir bağlantı çitlerinde, korkuluklarda, asma köprülerde, aydınlatma direklerinde, metal çatılarda, ısı eşanjörlerinde ve araba gövdelerinde kullanılır. ⓘ
Çinkonun göreceli reaktivitesi ve oksidasyonu kendine çekme yeteneği, onu katodik korumada (CP) etkili bir kurban anot haline getirir. Örneğin, gömülü bir boru hattının katodik koruması, çinkodan yapılmış anotların boruya bağlanmasıyla sağlanabilir. Çinko, elektrik akımını çelik boru hattına geçirirken yavaşça korozyona uğrayarak anot (negatif uç) görevi görür. Çinko ayrıca deniz suyuna maruz kalan metalleri katodik olarak korumak için de kullanılır. Bir geminin demir dümenine takılan bir çinko disk, dümen sağlam kalırken yavaşça korozyona uğrayacaktır. Benzer şekilde, bir pervaneye veya geminin omurgası için metal koruyucu muhafazaya takılan bir çinko tapa geçici koruma sağlar. ⓘ
Standart elektrot potansiyeli (SEP) -0,76 volt olan çinko, piller için anot malzemesi olarak kullanılır. (Lityum pillerdeki anotlar için daha reaktif lityum (SEP -3.04 V) kullanılır). Alkalin pillerde bu şekilde toz çinko kullanılır ve çinko-karbon pillerin kasası (aynı zamanda anot görevi görür) levha çinkodan oluşturulur. Çinko, çinko-hava pilinin/yakıt hücresinin anotu veya yakıtı olarak kullanılır. Çinko-seryum redoks akış pili de çinko bazlı bir negatif yarı hücreye dayanır. ⓘ
Alaşımlar
Yaygın olarak kullanılan bir çinko alaşımı, pirinç türüne bağlı olarak bakırın %3 ila %45 çinko ile alaşım haline getirildiği pirinçtir. Pirinç genellikle bakırdan daha sünek ve daha güçlüdür ve üstün korozyon direncine sahiptir. Bu özellikler onu iletişim ekipmanları, donanım, müzik aletleri ve su vanalarında kullanışlı hale getirir. ⓘ

Yaygın olarak kullanılan diğer çinko alaşımları arasında nikel gümüş, daktilo metali, yumuşak ve alüminyum lehim ve ticari bronz bulunmaktadır. Çinko ayrıca çağdaş boru organlarında borulardaki geleneksel kurşun/kalay alaşımının yerine kullanılmaktadır. 85-88 çinko, %4-10 bakır ve %2-8 alüminyum alaşımları bazı makine yataklarında sınırlı kullanım alanı bulmaktadır. Çinko 1982'den beri Amerikan bir sentlik madeni paralarının (pennies) ana metalidir. Çinko çekirdek, bakır madeni para görünümü vermek için ince bir bakır tabakası ile kaplanmıştır. 1994 yılında Amerika Birleşik Devletleri'nde 13,6 milyar peni üretmek için 33.200 ton (36.600 kısa ton) çinko kullanılmıştır. ⓘ
Az miktarda bakır, alüminyum ve magnezyum içeren çinko alaşımları, özellikle otomotiv, elektrik ve donanım endüstrilerinde kalıp dökümün yanı sıra spin dökümde de kullanışlıdır. Bu alaşımlar Zamak adı altında pazarlanmaktadır. Buna bir örnek çinko alüminyumdur. Alaşımın düşük viskozitesi ile birlikte düşük erime noktası, küçük ve karmaşık şekillerin üretimini mümkün kılar. Düşük çalışma sıcaklığı, döküm ürünlerin hızlı soğumasını ve montaj için hızlı üretim yapılmasını sağlar. Prestal markası altında pazarlanan bir başka alaşımın %78 çinko ve %22 alüminyum içerdiği ve neredeyse çelik kadar güçlü ancak plastik kadar yumuşak olduğu bildirilmektedir. Alaşımın bu süper esnekliği, seramik ve çimentodan yapılmış kalıp dökümleri kullanılarak kalıplanmasına olanak sağlamaktadır. ⓘ
Az miktarda kurşun eklenmiş benzer alaşımlar soğuk haddelenerek levha haline getirilebilir. 96 çinko ve %4 alüminyumdan oluşan bir alaşım, demirli metal kalıpların çok pahalı olacağı düşük üretimli uygulamalar için damgalama kalıpları yapmak için kullanılır. Bina cepheleri, çatı kaplamaları ve derin çekme, rulo şekillendirme veya bükme ile şekillendirilen diğer sac metal uygulamaları için titanyum ve bakır içeren çinko alaşımları kullanılır. Alaşımsız çinko bu üretim süreçleri için çok kırılgandır. ⓘ
Yoğun, ucuz ve kolay işlenen bir malzeme olarak çinko, kurşunun yerine kullanılır. Kurşunla ilgili endişelerin ardından çinko, balıkçılıktan lastik balanslarına ve volanlara kadar çeşitli uygulamalar için ağırlıklarda görülmektedir. ⓘ
Kadmiyum çinko tellürid (CZT), bir dizi küçük algılama cihazına bölünebilen yarı iletken bir alaşımdır. Bu cihazlar entegre bir devreye benzer ve gelen gama ışını fotonlarının enerjisini tespit edebilir. Emici bir maskenin arkasındayken, CZT sensör dizisi ışınların yönünü belirleyebilir. ⓘ
Diğer endüstriyel kullanımlar

2009'da Amerika Birleşik Devletleri'ndeki tüm çinko üretiminin yaklaşık dörtte biri, çeşitli endüstriyel olarak kullanılan çinko bileşiklerinde tüketilmiştir. Çinko oksit boyalarda beyaz pigment olarak ve kauçuk üretiminde ısıyı dağıtmak için katalizör olarak yaygın bir şekilde kullanılmaktadır. Çinko oksit, kauçuk polimerleri ve plastikleri ultraviyole radyasyondan (UV) korumak için kullanılır. Çinko oksidin yarı iletken özellikleri onu varistörlerde ve fotokopi ürünlerinde kullanışlı hale getirir. Çinko oksit döngüsü, hidrojen üretimi için çinko ve çinko oksit bazlı iki aşamalı bir termokimyasal süreçtir. ⓘ
Çinko klorür genellikle keresteye yangın geciktirici olarak ve bazen de ahşap koruyucu olarak eklenir. Diğer kimyasalların üretiminde kullanılır. Çinko metil (Zn(CH3)
2) bir dizi organik sentezde kullanılır. Çinko sülfür (ZnS), saatlerin ibrelerinde, X-ışını ve televizyon ekranlarında ve parlak boyalarda olduğu gibi ışıldayan pigmentlerde kullanılır. ZnS kristalleri, spektrumun orta kızılötesi kısmında çalışan lazerlerde kullanılır. Çinko sülfat, boya ve pigmentlerde kullanılan bir kimyasaldır. Çinko piritiyon zehirli boyalarda kullanılır. ⓘ
Çinko tozu bazen model roketlerde itici gaz olarak kullanılır. Sıkıştırılmış %70 çinko ve %30 sülfür tozu karışımı ateşlendiğinde şiddetli bir kimyasal reaksiyon meydana gelir. Bu, büyük miktarlarda sıcak gaz, ısı ve ışıkla birlikte çinko sülfür üretir. ⓘ
Çinko sac, çinko çubuklar yapmak için kullanılır. ⓘ
64
Çinkonun en bol bulunan izotopu olan Zn, nötron aktivasyonuna çok duyarlıdır ve yüksek derecede radyoaktif 65
Yarılanma ömrü 244 gün olan ve yoğun gama radyasyonu üreten Zn. Bu nedenle, nükleer reaktörlerde korozyon önleyici madde olarak kullanılan çinko oksitin %64'ü tükenmiştir.
Kullanmadan önce Zn, buna tükenmiş çinko oksit denir. Aynı nedenle, çinko nükleer silahlar için bir tuzlama malzemesi olarak önerilmiştir (kobalt daha iyi bilinen bir başka tuzlama malzemesidir). İzotopik olarak zenginleştirilmiş 64
Zn, patlayan bir termonükleer silahtan kaynaklanan yoğun yüksek enerjili nötron akısı tarafından ışınlanarak büyük miktarda 65
Zn, silahın serpintisinin radyoaktivitesini önemli ölçüde artırır. Böyle bir silahın şimdiye kadar inşa edildiği, test edildiği ya da kullanıldığı bilinmemektedir. ⓘ
65
Zn, çinko içeren alaşımların nasıl aşındığını veya çinkonun organizmalardaki yolunu ve rolünü incelemek için bir izleyici olarak kullanılır. ⓘ
Çinko ditiyokarbamat kompleksleri tarımsal fungisitler olarak kullanılır; bunlar arasında Zineb, Metiram, Propineb ve Ziram bulunur. Çinko naftenat ahşap koruyucu olarak kullanılır. ZDDP formundaki çinko, motor yağındaki metal parçalar için aşınma önleyici katkı maddesi olarak kullanılır. ⓘ
Organik kimya

Organozinc kimyası, fiziksel özellikleri, sentezi ve kimyasal reaksiyonları tanımlayan, karbon-çinko bağları içeren bileşiklerin bilimidir. Birçok organozinc bileşiği önemlidir. Önemli uygulamalar arasında şunlar bulunmaktadır
- Bir oksalat esterinin (ROCOCOOR) bir alkil halojenür R'X, çinko ve hidroklorik asit ile reaksiyona girerek α-hidroksikarboksilik esterler RR'COHCOOR oluşturduğu Frankland-Duppa Reaksiyonu
- Olumsuz tarafı, organozinkler Grignardlardan çok daha az nükleofiliktir ve pahalı ve kullanımı zordur. Ticari olarak temin edilebilen diorganozinc bileşikleri dimetilzinc, dietilzinc ve difenilzincdir. Bir çalışmada, aktif organozinc bileşiği çok daha ucuz organobromin öncüllerinden elde edilmiştir. ⓘ
Çinko, asimetrik sentez de dahil olmak üzere organik sentezlerde katalizör olarak birçok kullanım alanı bulmuştur, değerli metal komplekslerine ucuz ve kolay temin edilebilir bir alternatiftir. Kiral çinko katalizörlerle elde edilen sonuçlar (verim ve enantiyomerik fazlalık) paladyum, rutenyum, iridyum ve diğerleriyle elde edilenlerle karşılaştırılabilir ve çinko tercih edilen bir metal katalizör haline gelir. ⓘ
Besin takviyesi

Tek tabletlik, reçetesiz satılan, günlük vitamin ve mineral takviyelerinin çoğunda çinko; çinko oksit, çinko asetat, çinko glukonat veya çinko amino asit şelatı gibi formlarda bulunur. ⓘ
Genel olarak çinko takviyesi, çinko eksikliği riskinin yüksek olduğu yerlerde (düşük ve orta gelirli ülkeler gibi) önleyici bir tedbir olarak önerilmektedir. Çinko sülfat yaygın olarak kullanılan bir çinko formu olmasına rağmen, çinko sitrat, glukonat ve pikolinat da geçerli seçenekler olabilir. Bu formlar çinko oksitten daha iyi emilir. ⓘ
Gastroenterit
Çinko, gelişmekte olan ülkelerdeki çocuklarda ishal tedavisinin ucuz ve etkili bir parçasıdır. Çinko ishal sırasında vücutta tükenir ve 10 ila 14 günlük bir tedavi ile çinkonun yenilenmesi ishal ataklarının süresini ve şiddetini azaltabilir ve ayrıca üç ay kadar uzun bir süre boyunca gelecek atakları önleyebilir. Gastroenterit, muhtemelen gastrointestinal sistemdeki iyonların doğrudan antimikrobiyal etkisi veya çinkonun emilmesi ve bağışıklık hücrelerinden (tüm granülositler çinko salgılar) yeniden salınması veya her ikisi yoluyla çinko alımıyla güçlü bir şekilde zayıflatılır. ⓘ
Kilo alımı
Çinko eksikliği iştah kaybına yol açabilir. Anoreksiya tedavisinde çinko kullanımı 1979'dan beri savunulmaktadır. En az 15 klinik çalışma çinkonun anoreksiyada kilo alımını iyileştirdiğini göstermiştir. 1994 yılında yapılan bir çalışma, çinkonun anoreksiya nervoza tedavisinde vücut kütlesi artış oranını iki katına çıkardığını göstermiştir. Tirozin, triptofan ve tiamin gibi diğer besin maddelerinin eksikliği bu "yetersiz beslenmeye bağlı malnütrisyon" olgusuna katkıda bulunabilir. Birçok ülkede çinko takviyesi ve bunun çocukların büyümesi üzerindeki etkilerine ilişkin 33 prospektif müdahale çalışmasının meta analizi, tek başına çinko takviyesinin doğrusal büyüme ve vücut ağırlığı artışı üzerinde istatistiksel olarak anlamlı bir etkiye sahip olduğunu göstermiş, bu da mevcut olabilecek diğer eksikliklerin büyüme geriliğinden sorumlu olmadığını ortaya koymuştur. ⓘ
Diğer
Bir Cochrane incelemesi, çinko takviyesi alan kişilerin yaşa bağlı maküler dejenerasyona ilerleme olasılığının daha düşük olabileceğini belirtmiştir. Çinko takviyesi, daha önce etkilenen bebekler için ölümcül olan çinko emilimini etkileyen genetik bir bozukluk olan akrodermatitis enteropathica için etkili bir tedavidir. Çinko eksikliği majör depresif bozukluk (MDB) ile ilişkilendirilmiştir ve çinko takviyeleri etkili bir tedavi olabilir. ⓘ
Topikal kullanım
Topikal çinko preparatları, genellikle çinko oksit formunda cilt üzerinde kullanılanları içerir. Çinko preparatları yazın güneş yanıklarına ve kışın rüzgar yanıklarına karşı koruma sağlayabilir. Her bez değişiminde bebeğin bez bölgesine (perine) ince bir şekilde uygulandığında pişiğe karşı koruma sağlayabilir. ⓘ
Şelatlı çinko ağız kokusunu önlemek için diş macunlarında ve gargaralarda kullanılır; çinko sitrat diş taşı (tartar) birikimini azaltmaya yardımcı olur. ⓘ
Çinko piritiyon kepeği önlemek için şampuanlarda yaygın olarak bulunur. ⓘ
Topikal çinkonun genital uçuklarda etkili bir şekilde tedavi ettiği ve remisyonu uzattığı da gösterilmiştir. ⓘ
Biyolojik rolü
Çinko, insanlar ve diğer hayvanlar, bitkiler ve mikroorganizmalar için temel bir eser elementtir. Çinko 300'den fazla enzimin ve 1000 transkripsiyon faktörünün işlevi için gereklidir ve metallothioneinlerde depolanır ve aktarılır. Demirden sonra insanlarda en çok bulunan ikinci eser metaldir ve tüm enzim sınıflarında bulunan tek metaldir. ⓘ
Proteinlerde çinko iyonları genellikle aspartik asit, glutamik asit, sistein ve histidin amino asit yan zincirlerine koordine olur. Proteinlerdeki bu çinko bağlanmasının (diğer geçiş metallerinde olduğu gibi) teorik ve hesaplamalı açıklaması zordur. ⓘ
Kabaca 2-4 gram çinko insan vücuduna dağılmıştır. Çinkonun çoğu beyin, kas, kemik, böbrek ve karaciğerde bulunurken, en yüksek konsantrasyonlar prostat ve gözün bazı kısımlarında bulunur. Meni özellikle prostat bezi fonksiyonu ve üreme organı büyümesinde önemli bir faktör olan çinko açısından zengindir. ⓘ
Vücudun çinko homeostazı esas olarak bağırsak tarafından kontrol edilir. Burada, ZIP4 ve özellikle TRPM7, doğum sonrası hayatta kalma için gerekli olan bağırsak çinko alımıyla ilişkilendirilmiştir. ⓘ
İnsanlarda çinkonun biyolojik rolleri her yerde mevcuttur. "Çok çeşitli organik ligandlar" ile etkileşime girer ve RNA ve DNA metabolizmasında, sinyal iletiminde ve gen ifadesinde rol oynar. Ayrıca apoptozu da düzenler. 2015 yılında yapılan bir inceleme, insan proteinlerinin yaklaşık %10'unun (~3000) çinko bağladığını, buna ek olarak yüzlerce proteinin de çinko taşıdığını ve çinko trafiği yaptığını göstermiştir; Arabidopsis thaliana bitkisinde yapılan benzer bir in silico çalışmada çinko ile ilişkili 2367 protein bulunmuştur. ⓘ
Beyinde çinko, glutamaterjik nöronlar tarafından spesifik sinaptik veziküllerde depolanır ve nöronal uyarılabilirliği modüle edebilir. Sinaptik plastisitede ve dolayısıyla öğrenmede kilit bir rol oynar. Çinko homeostazı, merkezi sinir sisteminin işlevsel düzenlenmesinde de kritik bir rol oynar. Merkezi sinir sisteminde aşırı sinaptik çinko konsantrasyonlarıyla sonuçlanan çinko homeostazının düzensizliğinin mitokondriyal oksidatif stres (örneğin kompleks I, kompleks III ve α-ketoglutarat dehidrojenaz dahil elektron taşıma zincirinde yer alan bazı enzimleri bozarak), kalsiyum homeostazının düzensizliği, glutamaterjik nöronal eksitotoksisite ve intranöronal sinyal iletimine müdahale yoluyla nörotoksisiteyi indüklediğine inanılmaktadır. L- ve D-histidin beyin çinko alımını kolaylaştırır. SLC30A3, serebral çinko homeostazında rol oynayan birincil çinko taşıyıcısıdır. ⓘ
Enzimler


Çinko etkili bir Lewis asididir, bu da onu hidroksilasyon ve diğer enzimatik reaksiyonlarda yararlı bir katalitik ajan yapar. Metal ayrıca esnek bir koordinasyon geometrisine sahiptir, bu da onu kullanan proteinlerin biyolojik reaksiyonları gerçekleştirmek için konformasyonları hızla değiştirmesine izin verir. Çinko içeren enzimlere iki örnek karbonik anhidraz ve karboksipeptidazdır; bunlar karbondioksit (CO
2) sırasıyla proteinlerin düzenlenmesi ve sindirimi. ⓘ
Omurgalı kanında, karbonik anhidraz CO
2'yi bikarbonata dönüştürür ve aynı enzim bikarbonatı tekrar CO
2 akciğerlerden nefes vermek için. Bu enzim olmadan, bu dönüşüm normal kan pH'ı olan 7'de yaklaşık bir milyon kat daha yavaş gerçekleşir ya da pH'ın 10 veya daha fazla olması gerekirdi. Akraba olmayan β-karbonik anhidraz bitkilerde yaprak oluşumu, indol asetik asit (oksin) sentezi ve alkolik fermantasyon için gereklidir. ⓘ
Karboksipeptidaz, proteinlerin sindirimi sırasında peptit bağlantılarını keser. Terminal peptit ile çinkoya bağlı bir C=O grubu arasında bir koordinat kovalent bağ oluşur ve bu da karbona pozitif bir yük verir. Bu, enzim üzerinde çinkoya yakın bir hidrofobik cep oluşturmaya yardımcı olur ve bu da sindirilen proteinin polar olmayan kısmını çeker. ⓘ
Sinyalizasyon
Çinko, sinyal yollarını aktive edebilen bir haberci olarak kabul edilmiştir. Bu yolların birçoğu anormal kanser büyümesinde itici güç sağlar. ZIP taşıyıcıları aracılığıyla hedeflenebilirler. ⓘ
Diğer proteinler
Çinko, çinko parmaklarda, kıvrımlarda ve kümelerde tamamen yapısal bir rol oynar. Çinko parmaklar, DNA'nın replikasyonu ve transkripsiyonu sırasında DNA baz dizilerini tanıyan proteinler olan bazı transkripsiyon faktörlerinin parçalarını oluşturur. Dokuz veya on Zn2+'nin her biri
iyonları, transkripsiyon faktöründeki dört amino aside koordineli bir şekilde bağlanarak parmağın yapısının korunmasına yardımcı olur. ⓘ
Kan plazmasında çinko, albümin (%60, düşük afiniteli) ve transferrin (%10) tarafından bağlanır ve taşınır. Transferrin aynı zamanda demir de taşıdığından, aşırı demir çinko emilimini azaltır ve bunun tersi de geçerlidir. Bakır ile de benzer bir antagonizma mevcuttur. Kan plazmasındaki çinko konsantrasyonu, çinko alımından bağımsız olarak nispeten sabit kalır. Tükürük bezi, prostat, bağışıklık sistemi ve bağırsaktaki hücreler diğer hücrelerle iletişim kurmak için çinko sinyalini kullanır. ⓘ
Çinko, mikroorganizmaların içindeki metallothionein rezervlerinde veya hayvanların bağırsaklarında veya karaciğerinde tutulabilir. Bağırsak hücrelerindeki metallothionein, çinko emilimini %15-40 oranında ayarlayabilmektedir. Bununla birlikte, yetersiz veya aşırı çinko alımı zararlı olabilir; aşırı çinko özellikle bakır emilimini bozar çünkü metallothionein her iki metali de emer. ⓘ
İnsan dopamin taşıyıcısı, çinko bağlandığında dopamin geri alımını inhibe eden ve in vitro amfetamin kaynaklı dopamin akışını güçlendiren yüksek afiniteli bir hücre dışı çinko bağlama bölgesi içerir. İnsan serotonin taşıyıcısı ve norepinefrin taşıyıcısı çinko bağlama bölgeleri içermez. S100 veya NCS-1 gibi bazı EF-el kalsiyum bağlayıcı proteinler de çinko iyonlarını bağlayabilmektedir. ⓘ
Beslenme
Beslenme önerileri
ABD Tıp Enstitüsü (IOM) 2001 yılında çinko için Tahmini Ortalama Gereksinimleri (EAR'lar) ve Önerilen Diyet Miktarlarını (RDA'lar) güncellemiştir. Çinko için 14 yaş ve üzeri kadın ve erkekler için güncel EAR'lar sırasıyla 6.8 ve 9.4 mg/gün'dür. RDA'lar ise 8 ve 11 mg/gündür. RDA'lar, ortalama gereksinimlerden daha yüksek olan kişileri kapsayacak miktarları belirlemek için EAR'lardan daha yüksektir. Hamilelik için RDA 11 mg/gündür. Emzirme dönemi için RDA 12 mg/gün'dür. 12 aya kadar olan bebekler için RDA 3 mg/gün'dür. 1-13 yaş arası çocuklar için RDA yaşla birlikte 3 ila 8 mg/gün arasında artar. Güvenlik konusunda ise IOM, kanıtlar yeterli olduğunda vitamin ve mineraller için tolere edilebilir üst alım seviyeleri (UL'ler) belirlemektedir. Çinko için yetişkinlerde UL 40 mg/gündür (çocuklar için daha düşüktür). EAR'lar, RDA'lar, AI'lar ve UL'ler toplu olarak Diyet Referans Alımları (DRI'ler) olarak adlandırılır. ⓘ
Avrupa Gıda Güvenliği Otoritesi (EFSA), RDA yerine Popülasyon Referans Alımı (PRI) ve EAR yerine Ortalama Gereksinim kullanarak toplu bilgi setini Diyet Referans Değerleri olarak adlandırmaktadır. AI ve UL, Amerika Birleşik Devletleri'nde olduğu gibi tanımlanmıştır. 18 yaş ve üzeri kişiler için PRI hesaplamaları karmaşıktır, çünkü EFSA diyetin fitat içeriği arttıkça daha yüksek ve daha yüksek değerler belirlemiştir. Kadınlar için, fitat alımı 300 ila 1200 mg/gün arasında arttıkça PRI'lar 7,5 ila 12,7 mg/gün arasında artmaktadır; erkekler için bu aralık 9,4 ila 16,3 mg/gündür. Bu PRI'lar ABD RDA'larından daha yüksektir. EFSA aynı güvenlik sorusunu incelemiş ve UL değerini 25 mg/gün olarak belirlemiştir ki bu değer ABD değerinden çok daha düşüktür. ⓘ
ABD gıda ve besin takviyesi etiketleme amaçları için bir porsiyondaki miktar Günlük Değerin yüzdesi (%DV) olarak ifade edilir. Çinko etiketleme amaçları için Günlük Değerin %100'ü 15 mg idi, ancak 27 Mayıs 2016 tarihinde 11 mg olarak revize edilmiştir. Eski ve yeni yetişkin günlük değerlerinin bir tablosu Referans Günlük Alım adresinde verilmiştir. ⓘ
Diyetle alınan miktar

Et, balık, kabuklu deniz ürünleri, kümes hayvanları, yumurta ve süt ürünleri gibi hayvansal ürünler çinko içerir. Bitkilerdeki çinko konsantrasyonu topraktaki seviyeye göre değişir. Toprakta yeterli çinko bulunduğunda, en fazla çinko içeren gıda bitkileri buğday (rüşeym ve kepek) ve susam, haşhaş, yonca, kereviz ve hardal gibi çeşitli tohumlardır. Çinko ayrıca fasulye, fındık, badem, tam tahıllar, kabak çekirdeği, ayçiçeği çekirdeği ve frenk üzümünde de bulunur. ⓘ
Diğer kaynaklar arasında zenginleştirilmiş gıdalar ve çeşitli formlardaki diyet takviyeleri yer alır. 1998 yılında yapılan bir inceleme, Amerika Birleşik Devletleri'nde en yaygın takviyelerden biri olan çinko oksit ve çinko karbonatın neredeyse çözünmez olduğu ve vücutta zayıf bir şekilde emildiği sonucuna varmıştır. Bu derlemede, çinko oksit ve çinko karbonat tüketen deneklerde, çinko asetat ve sülfat tuzları alanlara göre daha düşük plazma çinko konsantrasyonları bulan çalışmalara atıfta bulunulmuştur. Bununla birlikte, 2003 yılında yapılan bir inceleme, zenginleştirme için, daha pahalı formlar kadar kolay emilen ucuz ve istikrarlı bir kaynak olarak tahılları (çinko oksit içeren) tavsiye etmiştir. 2005 yılında yapılan bir çalışmada, oksit ve sülfat da dahil olmak üzere çeşitli çinko bileşiklerinin, mısır ekmeğine takviye olarak eklendiğinde emilim açısından istatistiksel olarak anlamlı farklılıklar göstermediği bulunmuştur. ⓘ
Eksiklik
Gelişmekte olan dünyada yaklaşık iki milyar insanda çinko eksikliği bulunmaktadır. Risk altındaki gruplar arasında gelişmekte olan ülkelerdeki çocuklar ve kronik hastalığı olan yaşlılar yer almaktadır. Çocuklarda enfeksiyon ve ishalin artmasına neden olur ve dünya çapında yılda yaklaşık 800.000 çocuğun ölümüne katkıda bulunur. Dünya Sağlık Örgütü, şiddetli yetersiz beslenme ve ishal için çinko takviyesini savunmaktadır. Çinko takviyesi, özellikle düşük doğum ağırlıklı veya bodur büyüme gösteren çocuklarda hastalıkların önlenmesine ve ölümlerin azaltılmasına yardımcı olmaktadır. Bununla birlikte, çinko takviyeleri tek başına uygulanmamalıdır, çünkü gelişmekte olan dünyadaki birçok kişide çeşitli eksiklikler vardır ve çinko diğer mikro besinlerle etkileşim halindedir. Çinko eksikliği genellikle yetersiz diyet alımından kaynaklansa da, malabsorpsiyon, akrodermatitis enteropathica, kronik karaciğer hastalığı, kronik böbrek hastalığı, orak hücre hastalığı, diyabet, malignite ve diğer kronik hastalıklarla ilişkili olabilir. ⓘ
Amerika Birleşik Devletleri'nde, federal bir gıda tüketimi araştırması, 19 yaş üstü kadın ve erkeklerde ortalama tüketimin sırasıyla 9,7 ve 14,2 mg/gün olduğunu belirlemiştir. Kadınların %17'si, erkeklerin ise %11'i EAR değerinden daha az tüketmiştir. EAR'ın altındaki yüzdeler yaşla birlikte artmıştır. Araştırmanın en son yayınlanan güncellemesi (NHANES 2013-2014) daha düşük ortalamalar bildirmiştir - 9,3 ve 13,2 mg/gün - yine alım yaşla birlikte azalmaktadır. ⓘ
Hafif çinko eksikliğinin belirtileri çeşitlidir. Klinik sonuçlar arasında depresif büyüme, ishal, iktidarsızlık ve cinsel olgunlaşmada gecikme, alopesi, göz ve cilt lezyonları, iştah bozukluğu, bilişsel değişim, bağışıklık fonksiyonlarında bozulma, karbonhidrat kullanımında kusurlar ve üreme teratogenezi yer almaktadır. Çinko eksikliği bağışıklığı baskılar, ancak aşırı çinko da baskılar. ⓘ
Bazı endişelere rağmen, batılı vejetaryenler ve veganlar et yiyenlerden daha fazla açık çinko eksikliğinden muzdarip değildir. Başlıca bitkisel çinko kaynakları arasında pişmiş kuru fasulye, deniz sebzeleri, güçlendirilmiş tahıllar, soya gıdaları, fındık, bezelye ve tohumlar yer alır. Bununla birlikte, birçok tam tahıl ve lifte bulunan fitatlar çinko emilimini engelleyebilir ve marjinal çinko alımının etkileri tam olarak anlaşılamamıştır. Tohumlarda ve tahıl kepeğinde bulunan çinko şelatör fitat, çinko emilim bozukluğuna katkıda bulunabilir. Bazı kanıtlar, bazı vejetaryenler gibi diyetinde fitat oranı yüksek olan kişilerde ABD RDA'sından (yetişkin kadınlar için 8 mg/gün; yetişkin erkekler için 11 mg/gün) daha fazlasına ihtiyaç duyulabileceğini göstermektedir. Avrupa Gıda Güvenliği Otoritesi (EFSA) kılavuzları, diyetle fitat alımının daha fazla olduğu durumlarda daha yüksek çinko alımını önererek bunu telafi etmeye çalışmaktadır. Bu hususlar, yeterli çinko biyobelirteçlerinin azlığına karşı dengelenmelidir ve en yaygın kullanılan gösterge olan plazma çinkosunun duyarlılığı ve özgüllüğü zayıftır. ⓘ
Toprak iyileştirme
Calluna, Erica ve Vaccinium türleri çinko-metalli topraklarda yetişebilir, çünkü ericoid mikorizal mantarların etkisiyle toksik iyonların translokasyonu engellenir. ⓘ
Tarım
Çinko eksikliği, mahsul bitkilerinde en yaygın mikro besin eksikliği olarak görünmektedir; özellikle yüksek pH'lı topraklarda yaygındır. Çinko eksikliği olan topraklar Türkiye ve Hindistan'ın yaklaşık yarısında, Çin'in üçte birinde ve Batı Avustralya'nın çoğunda ekili arazilerdir. Bu bölgelerde çinko gübrelemesine karşı önemli tepkiler bildirilmiştir. Çinko eksikliği olan topraklarda yetişen bitkiler hastalıklara karşı daha hassastır. Çinko toprağa öncelikle kayaların ayrışması yoluyla eklenir, ancak insanlar fosil yakıt yanması, maden atıkları, fosfatlı gübreler, pestisit (çinko fosfit), kireçtaşı, gübre, kanalizasyon çamuru ve galvanizli yüzeylerden gelen parçacıklar yoluyla çinko eklemiştir. Çinko toksisitesi çok daha az yaygın olmasına rağmen, fazla çinko bitkiler için toksiktir. ⓘ
Önlemler
Toksisite
Çinko sağlık için temel bir gereksinim olmasına rağmen, fazla çinko zararlı olabilir. Aşırı çinko emilimi bakır ve demir emilimini baskılar. Çözeltideki serbest çinko iyonu bitkiler, omurgasızlar ve hatta omurgalı balıklar için oldukça toksiktir. Serbest İyon Aktivite Modeli literatürde iyi bir şekilde oluşturulmuştur ve serbest iyonun sadece mikromolar miktarlarının bazı organizmaları öldürdüğünü göstermektedir. Yakın tarihli bir örnek, 6 mikromolar'ın sudaki tüm Daphnia'ların %93'ünü öldürdüğünü göstermiştir. ⓘ
Serbest çinko iyonu, aşındırıcı olma noktasına kadar güçlü bir Lewis asididir. Mide asidi, metalik çinkonun kolayca çözünerek korozif çinko klorür verdiği hidroklorik asit içerir. 1982 sonrası bir Amerikan sentinin (%97,5 çinko) yutulması, asidik midede çinko iyonunun yüksek çözünürlüğü nedeniyle mide zarında hasara neden olabilir. ⓘ
Kanıtlar, günde 100-300 mg çinko alan kişilerin indüklenmiş bakır eksikliği yaşayabileceğini göstermektedir. 2007 yılında yapılan bir çalışmada, günde 80 mg alan yaşlı erkeklerin, plasebo alanlara kıyasla idrar komplikasyonları nedeniyle daha sık hastaneye kaldırıldığı gözlemlenmiştir. 100-300 mg seviyeleri bakır ve demir kullanımını engelleyebilir veya kolesterolü olumsuz etkileyebilir. Toprakta 500 ppm'i aşan çinko, demir ve manganez gibi diğer temel metallerin bitki tarafından emilimini engeller. Çinko titremesi veya "çinko üşümesi" olarak adlandırılan bir durum, galvanizli malzemelerin lehimlenmesi veya kaynaklanması sırasında çinko dumanının solunmasıyla ortaya çıkabilir. Çinko, gram başına 17 ila 38 mg çinko içerebilen protez kreminin yaygın bir bileşenidir. Bu ürünlerin aşırı kullanımından kaynaklanan sakatlıklar ve hatta ölümler iddia edilmiştir. ⓘ
ABD Gıda ve İlaç Dairesi (FDA) çinkonun burundaki sinir reseptörlerine zarar vererek anosmiye neden olduğunu belirtmektedir. Anosmi raporları 1930'larda çocuk felci enfeksiyonlarını önlemek için başarısız bir girişimde çinko preparatları kullanıldığında da gözlemlenmiştir. 16 Haziran 2009 tarihinde FDA, çinko bazlı burun içi soğuk algınlığı ürünlerinin mağaza raflarından kaldırılmasını emretmiştir. FDA, koku alma bozukluğu olan kişilerin sızan gaz veya dumanı algılayamaması ve yiyecekleri yemeden önce bozulup bozulmadığını anlayamaması nedeniyle koku kaybının hayati tehlike yaratabileceğini söyledi. ⓘ
Son araştırmalar, topikal antimikrobiyal çinko piritionun, kültürlenmiş insan keratinositleri ve melanositlerinde PARP'a bağlı enerji krizinin indüksiyonu ile genomik bütünlüğü bozabilecek güçlü bir ısı şoku tepkisi indükleyicisi olduğunu göstermektedir. ⓘ
Zehirlenme
1982 yılında ABD Darphanesi bakırla kaplanmış ancak esas olarak çinko içeren madeni paralar basmaya başladı. Çinko madeni paralar ölümcül olabilen çinko toksikozu riski oluşturmaktadır. Rapor edilen bir vakada 425 adet çinkonun (1 kg'dan fazla çinko) kronik olarak yutulması gastrointestinal bakteriyel ve fungal sepsis nedeniyle ölümle sonuçlanmıştır. Ancak 12 gram çinko alan bir başka hastada sadece uyuşukluk ve ataksi (kas hareketlerinin koordinasyonunda büyük eksiklik) görülmüştür. Çinko madeni paraların yutulmasıyla çinko zehirlenmesi yaşayan başka vakalar da bildirilmiştir. ⓘ
Kuruşlar ve diğer küçük madeni paralar bazen köpekler tarafından yutulur ve yabancı cisimlerin veteriner tarafından çıkarılmasını gerektirir. Bazı madeni paraların çinko içeriği, köpeklerde şiddetli hemolitik anemi ve karaciğer veya böbrek hasarı yoluyla genellikle ölümcül olan çinko toksisitesine neden olabilir; kusma ve ishal olası semptomlardır. Çinko papağanlarda oldukça toksiktir ve zehirlenme genellikle ölümcül olabilir. Galvanizli kutularda saklanan meyve sularının tüketimi, çinko ile toplu papağan zehirlenmelerine neden olmuştur. ⓘ
Bulunuşu
Çinko, yerkabuğunda en çok bulunan elementler arasında 23. sıradadır. En çok kullanılan cevheri sfalerit (ZnS) olup %40-50 çinko ve yaklaşık %10 demir içerir. Çinkonun ayrıştırıldığı diğer mineraller smitsonit (çinko karbonat), hemimorfit (çinko silikat) ve franklinit ((Fe,Mn,Zn)(Fe,Mn)2O4) dir. ⓘ




![{\displaystyle {\ce {ZnO + C ->[950^oC] Zn + CO}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1592f63fc0ae67a24850c33381264f5ca6bd1f55)
