Uranyum
 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Uranyum | ||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Telaffuz | /jʊˈreɪniəm/ (yuu-RAY-nee-əm) | |||||||||||||||||||||||||||||||||||||||||||||||||
| Görünüş | gümüşi gri metalik; havada korozyona uğrayarak siyah oksit tabakasına dönüşür | |||||||||||||||||||||||||||||||||||||||||||||||||
| Standart atom ağırlığı Ar°(U) |
| |||||||||||||||||||||||||||||||||||||||||||||||||
| Periyodik tabloda Uranyum | ||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||
| Atom numarası (Z) | 92 | |||||||||||||||||||||||||||||||||||||||||||||||||
| Grup | grup n/a | |||||||||||||||||||||||||||||||||||||||||||||||||
| Dönem | dönem 7 | |||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | f-blok | |||||||||||||||||||||||||||||||||||||||||||||||||
| Elektron konfigürasyonu | [[[Radon|Rn]]] 5f3 6d1 7s2 | |||||||||||||||||||||||||||||||||||||||||||||||||
| Kabuk başına elektron | 2, 8, 18, 32, 21, 9, 2 | |||||||||||||||||||||||||||||||||||||||||||||||||
| Fiziksel özellikler | ||||||||||||||||||||||||||||||||||||||||||||||||||
| STP'de Faz | katı | |||||||||||||||||||||||||||||||||||||||||||||||||
| Erime noktası | 1405,3 K (1132,2 °C, 2070 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||
| Kaynama noktası | 4404 K (4131 °C, 7468 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||
| Yoğunluk (r.t.'ye yakın) | 19,1 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||
| sıvı olduğunda (m.p.'de) | 17,3 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||
| Füzyon ısısı | 9,14 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||
| Buharlaşma ısısı | 417,1 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||
| Molar ısı kapasitesi | 27,665 J/(mol-K) | |||||||||||||||||||||||||||||||||||||||||||||||||
Buhar basıncı
| ||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomik özellikler | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Oksidasyon durumları | +1, +2, +3, +4, +5, +6 (amfoterik bir oksit) | |||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegatiflik | Pauling ölçeği: 1.38 | |||||||||||||||||||||||||||||||||||||||||||||||||
| İyonlaşma enerjileri |
| |||||||||||||||||||||||||||||||||||||||||||||||||
| Atomik yarıçap | ampi̇ri̇k: 156 pm | |||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalent yarıçap | 196±7 pm | |||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waals yarıçapı | 186 pm | |||||||||||||||||||||||||||||||||||||||||||||||||
| Uranyumun spektral çizgileri | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Diğer özellikler | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Doğal oluşum | ilkel | |||||||||||||||||||||||||||||||||||||||||||||||||
| Kristal yapı | ortorombik | |||||||||||||||||||||||||||||||||||||||||||||||||
| Ses hızı ince çubuk | 3155 m/s (20 °C'de) | |||||||||||||||||||||||||||||||||||||||||||||||||
| Termal genleşme | 13,9 µm/(m⋅K) (25 °C'de) | |||||||||||||||||||||||||||||||||||||||||||||||||
| Termal iletkenlik | 27,5 W/(m⋅K) | |||||||||||||||||||||||||||||||||||||||||||||||||
| Elektriksel direnç | 0,280 µΩ⋅m (0 °C'de) | |||||||||||||||||||||||||||||||||||||||||||||||||
| Manyetik sipariş | paramanyetik | |||||||||||||||||||||||||||||||||||||||||||||||||
| Young modülü | 208 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||
| Kayma modülü | 111 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||
| Yığın modülü | 100 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||
| Poisson oranı | 0.23 | |||||||||||||||||||||||||||||||||||||||||||||||||
| Vickers sertliği | 1960-2500 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||
| Brinell sertliği | 2350-3850 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||
| CAS Numarası | 7440-61-1 | |||||||||||||||||||||||||||||||||||||||||||||||||
| Tarih | ||||||||||||||||||||||||||||||||||||||||||||||||||
| İsimlendirme | Uranüs gezegeninden sonra, adını Yunan gök tanrısı Uranüs'ten almıştır | |||||||||||||||||||||||||||||||||||||||||||||||||
| Keşif | Martin Heinrich Klaproth (1789) | |||||||||||||||||||||||||||||||||||||||||||||||||
| İlk izolasyon | Eugène-Melchior Péligot (1841) | |||||||||||||||||||||||||||||||||||||||||||||||||
| Uranyumun ana izotopları | ||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||
Uranyum, sembolü U ve atom numarası 92 olan kimyasal bir elementtir. Periyodik tablonun aktinit serisinde yer alan gümüşi-gri renkli bir metaldir. Bir uranyum atomunun 92 protonu ve 92 elektronu vardır, bunların 6'sı değerlik elektronudur. Uranyum zayıf radyoaktiftir çünkü uranyumun tüm izotopları kararsızdır; doğal olarak oluşan izotoplarının yarı ömürleri 159.200 yıl ile 4,5 milyar yıl arasında değişmektedir. Doğal uranyumdaki en yaygın izotoplar uranyum-238 (146 nötrona sahiptir ve Dünya'daki uranyumun %99'undan fazlasını oluşturur) ve uranyum-235'tir (143 nötrona sahiptir). Uranyum, ilkel olarak oluşan elementler arasında en yüksek atom ağırlığına sahiptir. Yoğunluğu kurşundan yaklaşık %70 daha yüksek, altın veya tungstenden ise biraz daha düşüktür. Toprak, kaya ve suda milyonda birkaç parça gibi düşük konsantrasyonlarda doğal olarak bulunur ve ticari olarak uraninit gibi uranyum içeren minerallerden çıkarılır. ⓘ
Doğada uranyum, uranyum-238 (%99,2739-99,2752), uranyum-235 (%0,7198-0,7202) ve çok az miktarda uranyum-234 (%0,0050-0,0059) olarak bulunur. Uranyum bir alfa parçacığı yayarak yavaşça bozunur. Uranyum-238'in yarı ömrü yaklaşık 4,47 milyar yıl ve uranyum-235'in yarı ömrü 704 milyon yıldır, bu da onları Dünya'nın yaşını belirlemede yararlı kılar. ⓘ
Uranyumun pek çok çağdaş kullanımı, onun eşsiz nükleer özelliklerinden faydalanmaktadır. Uranyum-235 doğal olarak oluşan tek bölünebilir izotoptur, bu da nükleer enerji santrallerinde ve nükleer silahlarda yaygın olarak kullanılmasını sağlar. Ancak doğada çok az miktarda bulunduğu için uranyumun zenginleştirilmesi gerekir, böylece yeterli miktarda uranyum-235 bulunur. Uranyum-238 hızlı nötronlar tarafından parçalanabilir ve verimlidir, yani bir nükleer reaktörde bölünebilir plütonyum-239'a dönüştürülebilir. Bir başka bölünebilir izotop olan uranyum-233, doğal toryumdan üretilebilir ve nükleer teknolojide gelecekte endüstriyel kullanım için incelenmektedir. Uranyum-238'in hızlı nötronlarla kendiliğinden bölünme ve hatta uyarılmış bölünme için küçük bir olasılığı vardır; uranyum-235 ve daha az derecede uranyum-233 yavaş nötronlar için çok daha yüksek bir bölünme kesitine sahiptir. Yeterli konsantrasyonda, bu izotoplar sürekli bir nükleer zincir reaksiyonu sağlar. Bu, nükleer güç reaktörlerinde ısı üretir ve nükleer silahlar için bölünebilir malzeme üretir. Kurutulmuş uranyum (238U) kinetik enerji delicilerinde ve zırh kaplamalarında kullanılır. Uranyum, uranyum camında renklendirici olarak kullanılır ve limon sarısından yeşile kadar renkler üretir. Uranyum camı ultraviyole ışıkta yeşil renkte floresan verir. Erken dönem fotoğrafçılıkta renklendirme ve gölgelendirme için de kullanılmıştır. ⓘ
Uranyumun 1789 yılında pitchblende mineralinde keşfedilmesi, yeni elemente yakın zamanda keşfedilen Uranüs gezegeninin adını veren Martin Heinrich Klaproth'a atfedilir. Eugène-Melchior Péligot metali izole eden ilk kişiydi ve radyoaktif özellikleri 1896 yılında Henri Becquerel tarafından keşfedildi. Otto Hahn, Lise Meitner, Enrico Fermi ve J. Robert Oppenheimer gibi diğerlerinin 1934'te başlayan araştırmaları, nükleer enerji endüstrisinde ve savaşta kullanılan ilk nükleer silah olan Little Boy'da yakıt olarak kullanılmasına yol açtı. Soğuk Savaş sırasında Amerika Birleşik Devletleri ve Sovyetler Birliği arasındaki silahlanma yarışı, uranyum metali ve uranyum türevi plütonyum-239 kullanan on binlerce nükleer silah üretti. Bu silahların güvenliği yakından takip edilmektedir. Yaklaşık 2000 yılından bu yana, Soğuk Savaş dönemi bombalarının sökülmesiyle elde edilen plütonyum nükleer reaktörlerde yakıt olarak kullanılmaktadır. Bu nükleer reaktörlerin geliştirilmesi ve yaygınlaştırılması, CO2 içermeyen güçlü enerji kaynakları olmaları nedeniyle küresel bazda devam etmektedir. ⓘ
Uranyum, cama katıldığı zaman ilginç sarı-yeşil bir renk verir. yüksek radyoaktif elementtir. Yüksek yoğunluğa sahiptir. Çelikten daha yumuşaktır. Kurşundan %65 daha yoğundur. 3 tane allotropu vardır. Kolayca yükseltgenir ve ısıtıldığında yanar. Klor, kükürt ve azotla az ya da çok kolay bileşir; karbonla uranyum karbürü (UC2), uranyum karbür de suyla bozularak hidrojen ve hidrokarbonları verir. Uranyum metali, hidroklorik asit ve sülfürik asit içinde kolayca çözünerek dört değerli uranyum tuzlarını oluşturur; nitrik asit içinde dinginleşir. ⓘ
- Alfa (ortorombik) 667.7 °C nin üzerinde kararlıdır.
- Beta (tetragonal) 667.7 - 774.8 °C arasında kararlıdır.
- Gama (kübik) 774.8 °C dan erime noktası arasında kararlı (bu sıcaklıkta dövülebilir ve yumuşak formda) ⓘ
Uranyum mineralleri, uraninit, autinit, tobernit, koffinittir. Minerallerde bulunan uranyum kimyasal reaksiyonlar sonucunda uranyum okside veya diğer formlarına dönüştürülür. Metal olarak uranyum, KUF5 ve UF4 bileşiklerinin elektrolizi ile elde edilir. ⓘ
Çok saf uranyum ise halojenlerinin termal yanması ile elde edilir. ⓘ
Özellikleri

Rafine edildiğinde uranyum gümüşi beyaz, zayıf radyoaktif bir metaldir. Mohs sertliği 6'dır, camı çizmek için yeterlidir ve yaklaşık olarak titanyum, rodyum, manganez ve niyobyumunkine eşittir. Dövülebilir, sünek, hafif paramanyetik, güçlü elektropozitif ve zayıf bir elektrik iletkenidir. Uranyum metali 19,1 g/cm3 gibi çok yüksek bir yoğunluğa sahiptir, kurşundan (11,3 g/cm3) daha yoğundur, ancak tungsten ve altından (19,3 g/cm3) biraz daha az yoğundur. ⓘ
Uranyum metali neredeyse tüm metal olmayan elementlerle (asal gazlar hariç) ve bunların bileşikleriyle reaksiyona girer ve reaktivite sıcaklıkla artar. Hidroklorik ve nitrik asitler uranyumu çözer, ancak hidroklorik asit dışındaki oksitleyici olmayan asitler elemente çok yavaş saldırır. İnce bölündüğünde soğuk suyla tepkimeye girebilir; havada uranyum metali koyu bir uranyum oksit tabakasıyla kaplanır. Cevherlerdeki uranyum kimyasal olarak çıkarılır ve uranyum dioksite veya endüstride kullanılabilen diğer kimyasal formlara dönüştürülür. ⓘ
Uranyum-235 bölünebilir olduğu tespit edilen ilk izotoptur. Doğal olarak oluşan diğer izotoplar parçalanabilir, ancak bölünebilir değildir. Yavaş nötronlarla bombardıman edildiğinde, uranyum-235 izotopu çoğu zaman iki küçük çekirdeğe bölünerek nükleer bağlanma enerjisi ve daha fazla nötron açığa çıkarır. Bu nötronların çok fazlası diğer uranyum-235 çekirdekleri tarafından emilirse, bir ısı patlaması veya (özel durumlarda) bir patlamayla sonuçlanan bir nükleer zincirleme reaksiyon meydana gelir. Bir nükleer reaktörde böyle bir zincirleme reaksiyon, serbest nötronların bir kısmını emen bir nötron zehiri tarafından yavaşlatılır ve kontrol edilir. Bu tür nötron emici malzemeler genellikle reaktör kontrol çubuklarının bir parçasıdır (bu reaktör kontrol sürecinin açıklaması için nükleer reaktör fiziğine bakınız). ⓘ
Bir atom bombası yapmak için 15 lb (6.8 kg) kadar az miktarda uranyum-235 kullanılabilir. Hiroşima üzerinde patlatılan ve Little Boy adı verilen nükleer silah uranyum fisyonuna dayanıyordu. Ancak, ilk nükleer bomba (Trinity'de kullanılan Gadget) ve Nagazaki üzerinde patlatılan bombanın (Fat Man) her ikisi de plütonyum bombasıydı. ⓘ
Uranyum metalinin üç allotropik formu vardır:
- α (ortorombik) 668 °C'ye (1,234 °F) kadar kararlıdır. Ortorombik, uzay grubu No. 63, Cmcm, kafes parametreleri a= 285.4 pm, b = 587 pm, c = 495.5 pm.
- β (tetragonal) 668 ila 775 °C (1,234 ila 1,427 °F) arasında kararlıdır. Tetragonal, uzay grubu P42/mnm, P42nm veya P4n2, kafes parametreleri a = 565,6 pm, b = c = 1075,9 pm.
- γ (gövde merkezli kübik) 775 °C'den (1,427 °F) erime noktasına kadar - bu en dövülebilir ve sünek durumdur. Gövde merkezli kübik, kafes parametresi a = 352,4 pm. ⓘ
Uygulamalar
Askeri

Askeri sektörde uranyumun başlıca kullanım alanı yüksek yoğunluklu delicilerdir. Bu mühimmat, %1-2 oranında titanyum veya molibden gibi diğer elementlerle alaşımlanmış seyreltilmiş uranyumdan (DU) oluşur. Yüksek darbe hızında, merminin yoğunluğu, sertliği ve piroforikliği ağır zırhlı hedeflerin imha edilmesini sağlar. Tank zırhı ve diğer çıkarılabilir araç zırhları da seyreltilmiş uranyum plakalarla sertleştirilebilir. Basra Körfezi ve Balkanlar'daki savaşlar sırasında ABD, İngiltere ve diğer ülkeler tarafından bu tür mühimmatların kullanılması toprakta kalan uranyum bileşikleriyle ilgili soruları gündeme getirdikten sonra seyreltilmiş uranyum kullanımı siyasi ve çevresel açıdan tartışmalı hale geldi (bkz. Körfez Savaşı sendromu). ⓘ
Kurşunsuz uranyum ayrıca radyoaktif maddelerin depolanması ve taşınmasında kullanılan bazı konteynerlerde koruyucu malzeme olarak da kullanılmaktadır. Metalin kendisi radyoaktif olsa da, yüksek yoğunluğu radyum gibi güçlü kaynaklardan gelen radyasyonu durdurmada kurşundan daha etkili olmasını sağlar. Seyreltilmiş uranyumun diğer kullanım alanları arasında uçak kontrol yüzeyleri için karşı ağırlıklar, füze yeniden giriş araçları için balast ve kalkan malzemesi bulunmaktadır. Yüksek yoğunluğu nedeniyle bu malzeme atalet yönlendirme sistemlerinde ve jiroskopik pusulalarda bulunur. Seyreltilmiş uranyum, kolay işlenebilmesi ve dökülebilmesinin yanı sıra nispeten düşük maliyeti nedeniyle benzer yoğunluktaki metallere tercih edilmektedir. Tüketilmiş uranyuma maruz kalmanın ana riski radyoaktiviteden ziyade uranyum oksitten kaynaklanan kimyasal zehirlenmedir (uranyum sadece zayıf bir alfa yayıcıdır). ⓘ
Dünya Savaşı'nın sonraki aşamalarında, tüm Soğuk Savaş boyunca ve daha az ölçüde sonrasında, uranyum-235 nükleer silah üretmek için bölünebilir patlayıcı madde olarak kullanılmıştır. Başlangıçta iki ana fisyon bombası türü üretilmiştir: uranyum-235 kullanan nispeten basit bir cihaz ve uranyum-238'den türetilen plütonyum-239 kullanan daha karmaşık bir mekanizma. Daha sonra, trityum ve döteryum karışımının nükleer füzyona uğramasını sağlamak için plütonyum bazlı bir cihaz kullanan çok daha karmaşık ve çok daha güçlü bir fisyon/füzyon bombası (termonükleer silah) türü inşa edilmiştir. Bu tür bombalar fisil olmayan (zenginleştirilmemiş) uranyum bir kılıfla kaplanır ve güçlerinin yarısından fazlasını nükleer füzyon sürecinden kaynaklanan hızlı nötronların bu malzemeyi parçalamasından elde ederler. ⓘ
Sivil

Uranyumun sivil sektördeki ana kullanımı nükleer enerji santrallerine yakıt sağlamaktır. Bir kilogram uranyum-235, tam fisyon varsayıldığında teorik olarak yaklaşık 20 terajoule (2×1013 joule) enerji üretebilir; 1,5 milyon kilogram (1.500 ton) kömür kadar enerji. ⓘ
Ticari nükleer enerji santralleri tipik olarak yaklaşık %3 uranyum-235 oranında zenginleştirilmiş yakıt kullanmaktadır. CANDU ve Magnox tasarımları zenginleştirilmemiş uranyum yakıtı kullanabilen tek ticari reaktörlerdir. Birleşik Devletler Donanması reaktörleri için kullanılan yakıt tipik olarak uranyum-235 bakımından yüksek oranda zenginleştirilmiştir (kesin değerler sınıflandırılmıştır). Bir ıslah reaktöründe uranyum-238 de aşağıdaki reaksiyon yoluyla plütonyuma dönüştürülebilir:
- 238
92U
+ n → 239
92U
+ γ 239
93Np
239
94Pu ⓘ

Radyoaktivitenin keşfinden önce (ve bazen sonra) uranyum, öncelikle uranyum camı ve Fiestaware gibi sarı cam ve çömlek sırları için küçük miktarlarda kullanılıyordu. ⓘ
Marie Curie tarafından uranyum cevherinde (pitchblende) radyumun keşfedilmesi ve izole edilmesi, saat ve uçak kadranları için karanlıkta parlayan boyalar yapmak için kullanılan radyumu çıkarmak için uranyum madenciliğinin gelişmesine yol açtı. Bir gram radyum çıkarmak için üç ton uranyum gerektiğinden, bu durum atık ürün olarak muazzam miktarda uranyum bıraktı. Bu atık ürün sır endüstrisine yönlendirildi ve uranyum sırları çok ucuz ve bol hale geldi. Çömlek sırlarının yanı sıra, yeşil, sarı, leylak rengi, siyah, mavi, kırmızı ve diğer renklerde üretilebilen yaygın banyo ve mutfak karoları da dahil olmak üzere, uranyum karo sırları kullanımın büyük bir kısmını oluşturuyordu. ⓘ


Uranyum ayrıca fotoğraf kimyasallarında (özellikle toner olarak uranyum nitrat), sahne aydınlatma ampulleri için lamba filamentlerinde, protezlerin görünümünü iyileştirmek için ve deri ve ahşap endüstrilerinde leke ve boyalar için kullanılmıştır. Uranyum tuzları ipek veya yün mordanlarıdır. Uranil asetat ve uranil format, transmisyon elektron mikroskobunda, ultra ince kesitlerde biyolojik örneklerin kontrastını artırmak ve virüslerin, izole hücre organellerinin ve makromoleküllerin negatif boyanmasında elektron yoğun "lekeler" olarak kullanılır. ⓘ
Uranyumun radyoaktivitesinin keşfi, elementin ek bilimsel ve pratik kullanımlarını başlatmıştır. Uranyum-238 izotopunun uzun yarı ömrü (4,47×109 yıl), onu en eski magmatik kayaçların yaşını tahmin etmede ve uranyum-toryum tarihleme, uranyum-kurşun tarihleme ve uranyum-uranyum tarihleme dahil olmak üzere diğer radyometrik tarihleme türlerinde kullanım için çok uygun hale getirir. Uranyum metali, yüksek enerjili X-ışınlarının yapımında X-ışını hedefleri için kullanılır. ⓘ
Tarih
Keşif öncesi kullanım
Uranyumun doğal oksit formunda kullanımı, Roma İmparatorluğu'nda seramik sırlarına sarı bir renk katmak için kullanıldığı en az MS 79 yılına kadar uzanmaktadır. 1 uranyum oksit içeren sarı cam, 1912 yılında Oxford Üniversitesi'nden R. T. Gunther tarafından İtalya'nın Napoli Körfezi'ndeki Posillipo Burnu'nda bir Roma villasında bulunmuştur. Orta Çağ'ın sonlarından itibaren zift, Bohemya, Joachimsthal'daki (günümüzde Çek Cumhuriyeti'nde Jáchymov) Habsburg gümüş madenlerinden çıkarılmış ve yerel cam yapım endüstrisinde renklendirici olarak kullanılmıştır. 19. yüzyılın başlarında dünyanın bilinen tek uranyum cevheri kaynakları bu madenlerdi. Soğuk Savaş sona erdikten ve SDAG Wismut kapatıldıktan sonra Alman tarafında Cevher Dağları'nda uranyum madenciliği durduruldu. Çek tarafında ise 2007'deki uranyum fiyat balonu sırasında madenciliği yeniden başlatma girişimleri oldu, ancak uranyum fiyatlarındaki düşüşün ardından bunlardan hızla vazgeçildi. ⓘ
Keşif
Elementin keşfi Alman kimyager Martin Heinrich Klaproth'a atfedilir. Klaproth, 1789 yılında Berlin'deki deneysel laboratuvarında çalışırken, zifti nitrik asitte çözüp çözeltiyi sodyum hidroksitle nötralize ederek sarı bir bileşiği (muhtemelen sodyum diuranat) çökeltmeyi başardı. Klaproth sarı maddenin henüz keşfedilmemiş bir elementin oksidi olduğunu varsaydı ve yeni keşfedilen metalin kendisi olduğunu düşündüğü siyah bir toz elde etmek için kömürle ısıttı (aslında bu toz uranyumun bir oksidiydi). Yeni keşfettiği elemente, sekiz yıl önce William Herschel tarafından keşfedilmiş olan Uranüs gezegeninin (adını ilk Yunan gök tanrısından almıştır) adını verdi. ⓘ
1841 yılında Paris'teki Conservatoire National des Arts et Métiers'de (Sanat ve İmalat Merkez Okulu) Analitik Kimya Profesörü olan Eugène-Melchior Péligot, uranyum tetraklorürü potasyum ile ısıtarak ilk uranyum metali örneğini izole etti. ⓘ
Henri Becquerel 1896 yılında uranyum kullanarak radyoaktiviteyi keşfetti. Becquerel bu keşfi Paris'te bir çekmecede pozlanmamış bir fotoğraf plakasının üzerine bir uranyum tuzu örneği, K2UO2(SO4)2 (potasyum uranil sülfat) bırakarak ve plakanın "buğulandığını" fark ederek yaptı. Uranyum tarafından yayılan bir tür görünmez ışığın veya ışınların plakayı açığa çıkardığını tespit etti. ⓘ
Birinci Dünya Savaşı sırasında Merkezi Güçler topçu silahı namluları ve yüksek hızlı takım çelikleri yapmak için molibden sıkıntısı çektiklerinde, aynı fiziksel özelliklerin çoğunu sunan ferrouranyum alaşımlarını rutin olarak ikame ettiler. Bu uygulama 1916'da duyulduğunda ABD hükümeti önde gelen birkaç üniversiteden uranyumun bu kullanımlarını araştırmalarını istedi ve bu formüllerle yapılan aletler on yıllar boyunca kullanılmaya devam etti, ancak Manhattan Projesi ve Soğuk Savaş fisyon araştırmaları ve silah geliştirme için uranyuma büyük bir talep oluşturduğunda sona erdi. ⓘ
Fisyon araştırmaları

Enrico Fermi liderliğindeki bir ekip 1934 yılında uranyumu nötronlarla bombalamanın beta ışınları (üretilen elementlerden elektronlar veya pozitronlar; bkz. beta parçacığı) yaydığını gözlemledi. Fisyon ürünleri ilk başta, Roma Fakültesi Dekanı Orso Mario Corbino'nun sırasıyla ausonium ve hesperium olarak adlandırdığı 93 ve 94 atom numaralı yeni elementlerle karıştırıldı. Uranyumun daha hafif elementlere bölünme (parçalanma) ve bağlanma enerjisini serbest bırakma yeteneğinin keşfine yol açan deneyler Otto Hahn ve Fritz Strassmann tarafından Hahn'ın Berlin'deki laboratuvarında yürütüldü. Lise Meitner ve yeğeni fizikçi Otto Robert Frisch, Şubat 1939'da fiziksel açıklamayı yayınladılar ve sürece "nükleer fisyon" adını verdiler. Kısa bir süre sonra Fermi, uranyum fisyonunun bir fisyon reaksiyonunu sürdürmeye yetecek kadar nötron açığa çıkarabileceği hipotezini ortaya attı. Bu hipotezin doğrulanması 1939'da gerçekleşti ve daha sonraki çalışmalar, nadir bulunan uranyum izotopu uranyum-235'in her fisyonunda ortalama 2,5 nötronun açığa çıktığını ortaya koydu. Fermi, Alfred O. C. Nier'i bölünebilir bileşenin belirlenmesi için uranyum izotoplarını ayırmaya teşvik etti ve 29 Şubat 1940'ta Nier, Minnesota Üniversitesi'nde inşa ettiği bir aleti kullanarak Tate Laboratuvarı'nda dünyanın ilk uranyum-235 örneğini ayırdı. Columbia Üniversitesi'nin siklotronuna postalandıktan sonra, John Dunning 1 Mart'ta numunenin izole edilmiş bölünebilir malzeme olduğunu doğruladı. Daha sonraki çalışmalar, çok daha yaygın olan uranyum-238 izotopunun, uranyum-235 gibi termal nötronlar tarafından bölünebilir olan plütonyuma dönüştürülebileceğini ortaya koydu. Bu keşifler çok sayıda ülkenin nükleer silah ve nükleer enerji geliştirme çalışmalarına başlamasına yol açtı. Fisyonun Almanya'da keşfedilmiş olmasına rağmen, Uranverein ("uranyum kulübü") Almanya'nın nükleer güç ve/veya silah araştırmasına yönelik savaş zamanı projesi, sınırlı kaynaklar, iç çekişmeler, bu alanda önde gelen bazı bilim adamlarının sürgüne gönderilmesi ya da hiç katılmaması ve mevcut grafit örneklerindeki safsızlıkların hesaba katılmaması gibi bazı önemli hatalar nedeniyle sekteye uğradı ve bu da grafitin nötron moderatörü olarak gerçekte olduğundan daha az uygun görünmesine neden oldu. Almanya'nın doğal uranyum/ağır su reaktörü inşa etme girişimleri, Amerikalılar Almanya'nın savaş zamanındaki son reaktör deneyinin yapıldığı Haigerloch'a ulaştığında kritik seviyeye ulaşmaya yaklaşmamıştı. ⓘ
2 Aralık 1942'de Manhattan Projesi'nin bir parçası olarak Enrico Fermi liderliğindeki bir başka ekip ilk yapay kendi kendine devam eden nükleer zincir reaksiyonu olan Chicago Pile-1'i başlatmayı başardı. Zenginleştirilmiş uranyum-235 kullanan bir başlangıç planından, henüz yeterli miktarda bulunamadığı için vazgeçildi. Chicago Üniversitesi'ndeki Stagg Field tribünlerinin altındaki bir laboratuarda çalışan ekip, 400 kısa ton (360 metrik ton) grafit, 58 kısa ton (53 metrik ton) uranyum oksit ve altı kısa ton (5,5 metrik ton) uranyum metalini bir araya getirerek böyle bir reaksiyon için gereken koşulları yarattı; bunların büyük bir kısmı Westinghouse Lamp Plant tarafından geçici bir üretim sürecinde sağlandı. ⓘ
Nükleer silahlar
Dünya Savaşı sırasında Amerika Birleşik Devletleri tarafından iki ana tip atom bombası geliştirilmiştir: bölünebilir malzemesi yüksek oranda zenginleştirilmiş uranyum olan uranyum tabanlı bir cihaz (kod adı "Little Boy") ve plütonyumu uranyum-238'den türetilen plütonyum tabanlı bir cihaz (bkz. Trinity testi ve "Fat Man"). Uranyum bazlı Little Boy cihazı, 6 Ağustos 1945'te Japon şehri Hiroşima üzerinde patlatıldığında savaşta kullanılan ilk nükleer silah oldu. Yaklaşık 12.500 ton TNT'ye eşdeğer bir güçle patlayan bombanın yarattığı patlama ve termal dalga yaklaşık 50.000 binayı yerle bir etmiş ve yaklaşık 75.000 kişinin ölümüne yol açmıştır (bkz. Hiroşima ve Nagazaki'ye atom bombası atılması). Başlangıçta uranyumun nispeten nadir olduğu ve bilinen tüm uranyum stoklarının satın alınmasıyla nükleer yayılmanın önlenebileceği düşünülüyordu, ancak on yıl içinde dünyanın birçok yerinde büyük uranyum yatakları keşfedildi. ⓘ
Reaktörler

Oak Ridge, Tennessee'deki Oak Ridge Ulusal Laboratuvarı'nda (ORNL) bulunan ve daha önce Clinton Kazığı ve X-10 Kazığı olarak bilinen X-10 Grafit Reaktörü, dünyanın ikinci yapay nükleer reaktörüdür (Enrico Fermi'nin Chicago Kazığı'ndan sonra) ve sürekli çalışma için tasarlanan ve inşa edilen ilk reaktördür. Arco, Idaho yakınlarındaki Atom Enerjisi Komisyonu'nun Ulusal Reaktör Test İstasyonu'nda bulunan Argonne Ulusal Laboratuarı'nın Deneysel Islah Reaktörü I, 20 Aralık 1951'de elektrik üreten ilk nükleer reaktör oldu. Başlangıçta reaktör dört adet 150 watt'lık ampulü yakıyordu, ancak yapılan iyileştirmeler sonunda reaktörün tüm tesise güç sağlaması mümkün oldu (daha sonra Arco kasabası, Argonne Ulusal Laboratuarı tarafından tasarlanan ve işletilen bir başka reaktör olan BORAX-III'ün ürettiği nükleer enerjiden tüm elektriğini alan dünyadaki ilk kasaba oldu). Dünyanın ilk ticari ölçekli nükleer enerji santrali olan Sovyetler Birliği'ndeki Obninsk, 27 Haziran 1954 tarihinde AM-1 reaktörü ile üretime başlamıştır. Diğer ilk nükleer enerji santralleri 17 Ekim 1956'da üretime başlayan İngiltere'deki Calder Hall ve 26 Mayıs 1958'de üretime başlayan Pennsylvania'daki Shippingport Atomik Enerji Santrali'dir. Nükleer enerji ilk kez 1954 yılında bir denizaltı olan USS Nautilus tarafından itici güç olarak kullanılmıştır. ⓘ
Tarih öncesi doğal olarak oluşan fisyon
1972 yılında Fransız fizikçi Francis Perrin, Batı Afrika, Gabon'daki Oklo madeninde üç ayrı cevher yatağında, topluca Oklo Fosil Reaktörleri olarak bilinen on beş eski ve artık aktif olmayan doğal nükleer fisyon reaktörü keşfetti. Cevher yatağı 1,7 milyar yaşında; o zamanlar uranyum-235, Dünya'daki toplam uranyumun yaklaşık %3'ünü oluşturuyordu. Bu oran, diğer destekleyici koşulların mevcut olması halinde, sürekli bir nükleer fisyon zincir reaksiyonunun gerçekleşmesine izin verecek kadar yüksektir. Çevredeki tortunun nükleer atık ürünlerini tutma kapasitesi, ABD federal hükümeti tarafından kullanılmış nükleer yakıtın Yucca Dağı nükleer atık deposunda depolanmasının fizibilitesini destekleyen bir kanıt olarak gösterilmiştir. ⓘ
Kirlenme ve Soğuk Savaş mirası

Sovyetler Birliği ve Amerika Birleşik Devletleri tarafından 1950'lerde ve 1960'ların başında ve Fransa tarafından 1970'lerde ve 1980'lerde yapılan yer üstü nükleer denemeler, uranyum yavru izotoplarından kaynaklanan önemli miktarda serpintiyi dünyaya yaymıştır. Çeşitli nükleer kazalar nedeniyle ilave serpinti ve kirlilik meydana gelmiştir. ⓘ
Uranyum madencilerinde kanser görülme sıklığı daha yüksektir. Örneğin Navajo uranyum madencileri arasında akciğer kanseri riskinin fazla olduğu belgelenmiş ve meslekleriyle ilişkilendirilmiştir. ABD'de 1990 yılında yürürlüğe giren Radyasyona Maruz Kalma Tazminat Yasası, kanser veya diğer solunum rahatsızlıkları teşhisi konan uranyum madencilerine 100.000 dolar "şefkat ödemesi" yapılmasını zorunlu kılmıştır. ⓘ
Sovyetler Birliği ve Amerika Birleşik Devletleri arasındaki Soğuk Savaş sırasında devasa uranyum stokları biriktirilmiş ve zenginleştirilmiş uranyum ve uranyumdan yapılan plütonyum kullanılarak on binlerce nükleer silah üretilmiştir. Sovyetler Birliği'nin 1991 yılında dağılmasından bu yana, tahminen 600 short ton (540 metrik ton) yüksek derecede zenginleştirilmiş silah sınıfı uranyum (40,000 nükleer savaş başlığı yapmaya yetecek kadar) Rusya Federasyonu ve diğer bazı eski Sovyet devletlerinde genellikle yetersiz korunan tesislerde depolanmıştır. Asya, Avrupa ve Güney Amerika'da polis 1993'ten 2005'e kadar en az 16 kez, çoğu eski Sovyet kaynaklarından gelen kaçak bomba sınıfı uranyum ya da plütonyum sevkiyatlarını yakalamıştır. 1993'ten 2005'e kadar Amerika Birleşik Devletleri federal hükümeti tarafından işletilen Malzeme Koruma, Kontrol ve Muhasebe Programı, Rusya'daki uranyum ve plütonyum stoklarının korunmasına yardımcı olmak için yaklaşık 550 milyon ABD doları harcamıştır. Bu para, araştırma ve depolama tesislerinde iyileştirmeler ve güvenlik geliştirmeleri için kullanıldı. Scientific American'ın Şubat 2006'da yayınladığı bir habere göre bazı tesislerde güvenlik, ciddi şekilde bakımsız durumda olan zincir bağlantı çitlerden ibaretti. Makalede yer alan bir röportaja göre, bir tesis iyileştirme projesinden önce zenginleştirilmiş (silah sınıfı) uranyum örneklerini bir süpürge dolabında saklıyordu; bir diğeri ise nükleer savaş başlığı stokunu bir ayakkabı kutusunda saklanan dizin kartları kullanarak takip ediyordu. ⓘ
Oluşum
Köken
Demirden daha yüksek atom ağırlığına sahip tüm elementlerle birlikte uranyum, doğal olarak yalnızca süpernovalarda ve nötron yıldızı birleşmelerinde r-süreciyle (hızlı nötron yakalama) oluşur. İlkel toryum ve uranyum sadece r-sürecinde üretilir, çünkü s-süreci (yavaş nötron yakalama) çok yavaştır ve bizmuttan sonraki kararsızlık boşluğunu geçemez. Mevcut iki ilkel uranyum izotopu olan 235U ve 238U'nun yanı sıra, r-süreci ayrıca daha kısa bir yarı ömre sahip olan ve bu nedenle uzun zamandan beri tamamen 232Th'ye bozunmuş olan soyu tükenmiş bir radyonüklid olan 236U'yu da önemli miktarlarda üretmiştir. Uranyum-236'nın kendisi 244Pu'nun bozunmasıyla zenginleşmiştir, bu da toryumun beklenenden daha yüksek ve uranyumun beklenenden daha düşük bolluğunu açıklamaktadır. Uranyumun doğal bolluğu, soyu tükenmiş 242Pu (yarı ömrü 0,375 milyon yıl) ve 247Cm'nin (yarı ömrü 16 milyon yıl) bozunmasıyla desteklenerek sırasıyla 238U ve 235U üretilmiş olsa da, bu ebeveynlerin daha kısa yarı ömürleri ve toryumun ebeveynleri olan 236U ve 244Pu'dan daha düşük üretimleri nedeniyle bu neredeyse ihmal edilebilir bir ölçüde gerçekleşmiştir: Güneş Sistemi'nin oluşumundaki 247Cm:235U oranı (7,0±1,6)×10-5 idi. ⓘ
Biyotik ve abiyotik


Uranyum, tüm kaya, toprak ve suda düşük seviyelerde bulunabilen doğal olarak oluşan bir elementtir. Uranyum, yerkabuğundaki bolluk sırasına göre 51. elementtir. Uranyum aynı zamanda Dünya'da önemli miktarlarda doğal olarak bulunan en yüksek numaralı elementtir ve neredeyse her zaman diğer elementlerle birlikte bulunur. Dünya'nın mantosundaki uranyum, toryum ve potasyum-40'ın bozunmasının, Dünya'nın dış çekirdeğini sıvı halde tutan ve manto konveksiyonunu yönlendiren ana ısı kaynağı olduğu düşünülmektedir, bu da plaka tektoniğini yönlendirir. ⓘ
Uranyumun yerkabuğundaki ortalama konsantrasyonu (referansa bağlı olarak) milyonda 2 ila 4 parça ya da gümüşten yaklaşık 40 kat daha fazladır. Yüzeyden 25 km (15 mil) aşağıya kadar olan Dünya kabuğunun 1017 kg (2×1017 lb) uranyum içerdiği hesaplanırken, okyanuslar 1013 kg (2×1013 lb) içerebilir. Topraktaki uranyum konsantrasyonu milyonda 0,7 ila 11 parça (fosfatlı gübre kullanımı nedeniyle tarım arazisi toprağında milyonda 15 parçaya kadar) arasında değişmektedir ve deniz suyundaki konsantrasyonu milyarda 3 parçadır. ⓘ
Uranyum, antimon, kalay, kadmiyum, cıva veya gümüşten daha bol bulunur ve arsenik veya molibden kadar bol miktarda bulunur. Uranyum, uraninit (en yaygın uranyum cevheri), karnotit, autunit, uranofan, torbernit ve coffinit dahil olmak üzere yüzlerce mineralde bulunur. Fosfat kayası yatakları gibi bazı maddelerde ve uranyum açısından zengin cevherlerdeki linyit ve monazit kumları gibi minerallerde önemli uranyum konsantrasyonları meydana gelir (ticari olarak %0,1 kadar az uranyum içeren kaynaklardan geri kazanılır). ⓘ
Shewanella putrefaciens, Geobacter metallireducens ve Burkholderia fungorum'un bazı türleri gibi bazı bakteriler büyümek için uranyum kullanır ve U(VI)'yı U(IV)'e dönüştürür. Son araştırmalar, bu yolun bir ara U(V) pentavalent durumu aracılığıyla çözünür U(VI)'nın indirgenmesini içerdiğini göstermektedir.
Liken Trapelia involuta gibi diğer organizmalar veya Citrobacter bakterisi gibi mikroorganizmalar, çevrelerindeki seviyenin 300 katına kadar uranyum konsantrasyonlarını absorbe edebilir. Citrobacter türleri gliserol fosfat (veya diğer benzer organik fosfatlar) verildiğinde uranil iyonlarını emer. Bir gün sonra, bir gram bakteri dokuz gram uranil fosfat kristali ile kaplanabilir; bu da bu organizmaların uranyumla kirlenmiş suyu arındırmak için biyoremediasyonda kullanılabileceği ihtimalini doğurmaktadır. Proteobakteri Geobacter'in de yeraltı suyundaki uranyumu biyoremediate ettiği gösterilmiştir. Mikorizal mantar Glomus intraradices, simbiyotik bitkisinin köklerindeki uranyum içeriğini artırır. ⓘ
Doğada, uranyum (VI) alkali pH'da yüksek oranda çözünür karbonat kompleksleri oluşturur. Bu durum, uranyumun nükleer atıklardan yeraltı sularına ve toprağa geçişinde ve bulunabilirliğinde artışa yol açarak sağlık tehlikelerine neden olmaktadır. Bununla birlikte, alkali pH'da aşırı karbonat varlığında uranyumu fosfat olarak çökeltmek zordur. Sphingomonas sp. suşu BSAR-1'in yüksek aktiviteli bir alkalin fosfataz (PhoK) eksprese ettiği bulunmuş ve bu enzim, uranyumun alkalin çözeltilerden uranil fosfat türleri olarak biyopresipitasyonu için uygulanmıştır. Çökeltme yeteneği, PhoK proteininin E. coli'de aşırı eksprese edilmesiyle geliştirilmiştir. ⓘ
Bitkiler topraktan bir miktar uranyum emer. Bitkilerdeki uranyumun kuru ağırlık konsantrasyonları milyarda 5 ila 60 parça arasında değişir ve yanmış odundan elde edilen kül milyonda 4 parçaya kadar konsantrasyonlara sahip olabilir. Gıda bitkilerindeki uranyumun kuru ağırlık konsantrasyonları tipik olarak daha düşüktür ve insanların yediği gıdalar yoluyla günde bir ila iki mikrogram alınır. ⓘ
Üretim ve madencilik

2013'te dünya çapında U3O8 (sarı kek) üretimi 70.015 tona ulaşmış olup bunun 22.451 tonu (%32) Kazakistan'da çıkarılmıştır. Diğer önemli uranyum madenciliği ülkeleri Kanada (9,331 t), Avustralya (6,350 t), Nijer (4,518 t), Namibya (4,323 t) ve Rusya'dır (3,135 t). ⓘ
Uranyum cevheri çeşitli şekillerde çıkarılır: açık ocak, yeraltı, yerinde liç ve sondaj kuyusu madenciliği (bkz. uranyum madenciliği). Çıkarılan düşük dereceli uranyum cevheri tipik olarak %0,01 ila %0,25 uranyum oksit içerir. Metali cevherinden çıkarmak için kapsamlı önlemler alınmalıdır. Kanada, Saskatchewan'daki Athabasca Havzası yataklarında bulunan yüksek dereceli cevherler ortalama %23'e kadar uranyum oksit içerebilir. Uranyum cevheri kırılarak ince bir toz haline getirilir ve ardından bir asit veya alkali ile liç edilir. Sızıntı suyu çökeltme, çözücü ekstraksiyonu ve iyon değişimi işlemlerinden birine tabi tutulur. Elde edilen ve sarı kek olarak adlandırılan karışım en az %75 uranyum oksit U3O8 içerir. Sarı kek daha sonra rafine edilmeden ve dönüştürülmeden önce öğütme işleminden kaynaklanan safsızlıkları gidermek için kalsine edilir. ⓘ
Ticari sınıf uranyum, uranyum halojenürlerin alkali veya toprak alkali metallerle indirgenmesi yoluyla üretilebilir. Uranyum metali ayrıca KUF'un elektrolizi yoluyla da hazırlanabilir
5 veya
UF
4, erimiş kalsiyum klorür (CaCl
2) ve sodyum klorür (NaCl) çözeltisi. Çok saf uranyum, uranyum halojenürlerin sıcak bir filament üzerinde termal ayrışması yoluyla üretilir. ⓘ
Sarı kek, saf uranyum elde etmek için daha da rafine edilen konsantre bir uranyum oksit karışımıdır. ⓘ
Kaynaklar ve rezervler
Uranyumun 5,5 milyon tonunun, uranyumun lb'si başına 59 ABD dolarından ekonomik olarak uygulanabilir cevher rezervlerinde bulunduğu tahmin edilmektedir. 35 milyon ton ise mineral kaynakları (nihai ekonomik çıkarma için makul beklentiler) olarak sınıflandırılmaktadır. Fiyatlar Mayıs 2003'te yaklaşık 10 $/lb iken Temmuz 2007'de 138 $/lb'ye yükselmiştir. Bu durum arama harcamalarında büyük bir artışa neden olmuştur. 2005 yılında dünya çapında 200 milyon ABD doları harcanmış olup, bu rakam bir önceki yıla göre %54 artış göstermiştir. Bu eğilim, arama harcamalarının 2004 yılına kıyasla %250'nin üzerinde bir artışla 774 milyon doların üzerine çıktığı 2006 yılında da devam etmiştir. OECD Nükleer Enerji Ajansı, 2007 yılı arama rakamlarının 2006 yılı rakamlarını yakalayacağını belirtmiştir. ⓘ
Avustralya dünyanın bilinen uranyum cevheri rezervlerinin %31'ine ve Güney Avustralya'daki Olympic Dam Madeninde bulunan dünyanın en büyük tek uranyum yatağına sahiptir. Orta Afrika Cumhuriyeti'ndeki Mbomou vilayetinin bir alt vilayeti olan Bakouma'da önemli bir uranyum rezervi bulunmaktadır. ⓘ
Megatondan Megawatt'a Programı gibi bazı nükleer yakıtlar sökülmekte olan nükleer silahlardan elde edilmektedir. ⓘ
Deniz suyunda 4.6 milyar ton uranyumun çözünmüş halde bulunduğu tahmin edilmektedir (1980'lerde Japon bilim adamları iyon değiştiriciler kullanarak deniz suyundan uranyum çıkarmanın teknik olarak mümkün olduğunu göstermişlerdir). Deniz suyundan uranyum çıkarmak için deneyler yapılmıştır, ancak suda bulunan karbonat nedeniyle verim düşük olmuştur. 2012 yılında ORNL araştırmacıları, Pasifik Kuzeybatı Ulusal Laboratuvarı'ndaki araştırmacılar tarafından doğrulanan sonuçlara göre, katı veya gaz moleküllerinin, atomların veya iyonların yüzeyde tutulmasını sağlayan ve ayrıca toksik metalleri sudan etkili bir şekilde uzaklaştıran HiCap adlı yeni bir emici malzemenin başarıyla geliştirildiğini duyurdu. ⓘ
Malzemeler
2005 yılında on yedi ülke konsantre uranyum oksit üretmiştir: Kanada (dünya üretiminin %27.9'u), Avustralya (%22.8), Kazakistan (%10.5), Rusya (%8.0), Namibya (%7.5), Nijer (%7.4), Özbekistan (%5.5), Amerika Birleşik Devletleri (%2.5), Arjantin (%2.1), Ukrayna (%1.9) ve Çin (%1.7). 2008 yılında Kazakistan'ın üretimini arttıracağı ve 2009 yılında 12.826 tonluk üretimle dünyanın en büyük uranyum üreticisi olacağı tahmin ediliyordu. 11.100 tonluk Kanada ve 9.430 tonluk Avustralya ile karşılaştırıldığında bu tahminler doğru çıktı. 2019 yılında Kazakistan dünya arzının %42'sini madenlerden üreterek en büyük uranyum payına sahip olurken, onu Kanada (%13) ve Avustralya (%12), Namibya (%10), Özbekistan (%6), Nijer (%5), Rusya (%5), Çin (%3), Ukrayna (%1,5), ABD (%0,12), Hindistan (%0,6), İran (%0,13) ve toplam 54752 ton madenlerden dünya üretimi takip etmektedir. Bununla birlikte, 2019 yılında uranyumun sadece üretimin %43'ünü (54752 ton) oluşturan cevherlerin geleneksel yeraltı madenciliği ile çıkarılmadığı, mineralli kayanın topraktan çıkarıldığı, parçalandığı ve aranan mineralleri çıkarmak için işlendiği, aynı zamanda yerinde liç yöntemleriyle (ISL) dünya üretiminin %57'sinin (64.566 ton) çıkarıldığı belirtilmelidir. ⓘ
1960'ların sonlarında BM jeologları Somali'de büyük uranyum yatakları ve diğer nadir mineral rezervleri keşfetti. Bu keşif türünün en büyüğüydü ve endüstri uzmanları bu yatakların o zamanlar bilinen 800.000 tonluk dünya uranyum rezervlerinin %25'inden fazlasını oluşturduğunu tahmin ediyordu. ⓘ
Mevcut nihai arzın en azından önümüzdeki 85 yıl için yeterli olduğuna inanılmaktadır, ancak bazı çalışmalar yirminci yüzyılın sonlarındaki yetersiz yatırımın 21. yüzyılda arz sorunları yaratabileceğini göstermektedir. Uranyum yataklarının log-normal dağılım gösterdiği görülmektedir. Cevher tenöründeki her on katlık düşüş için geri kazanılabilir uranyum miktarında 300 katlık bir artış söz konusudur. Başka bir deyişle, az miktarda yüksek dereceli cevher ve orantılı olarak çok daha fazla düşük dereceli cevher mevcuttur. ⓘ
Bileşikler

Oksidasyon durumları ve oksitler
Oksitler
Birçok büyük değirmende üretilen kalsine uranyum sarı keki, en çok oksitlenenden en az oksitlenene kadar çeşitli şekillerde uranyum oksidasyon türlerinin dağılımını içerir. Bir kalsinatörde kısa kalma süresine sahip partiküller genellikle uzun kalma süresine sahip olanlardan veya baca yıkayıcıda geri kazanılan partiküllerden daha az oksitlenmiş olacaktır. Uranyum içeriği genellikle U
3O
8, Manhattan Projesi günlerinden kalma, U
3O
8 analitik kimya raporlama standardı olarak kullanılmıştır. ⓘ
Uranyum-oksijen sistemindeki faz ilişkileri karmaşıktır. Uranyumun en önemli oksidasyon durumları uranyum(IV) ve uranyum(VI)'dır ve bunlara karşılık gelen iki oksit sırasıyla uranyum dioksit (UO
2) ve uranyum trioksit (UO
3). Uranyum monoksit (UO) gibi diğer uranyum oksitler, diuranyum pentoksit (U
2O
5) ve uranyum peroksit (UO
4-2H
2O) da mevcuttur. ⓘ
Uranyum oksidin en yaygın formları triüranyum oktoksittir (U
3O
8) ve UO
2. Her iki oksit formu da suda düşük çözünürlüğe sahip katı maddelerdir ve çok çeşitli çevresel koşullarda nispeten kararlıdır. Triuranyum oktoksit (koşullara bağlı olarak) uranyumun en kararlı bileşiğidir ve doğada en yaygın olarak bulunan formdur. Uranyum dioksit, uranyumun nükleer reaktör yakıtı olarak en yaygın kullanıldığı formdur. Ortam sıcaklıklarında, UO
2 kademeli olarak U'ya dönüşecektir
3O
8. Uranyum oksitler kararlılıkları nedeniyle genellikle depolama veya bertaraf için tercih edilen kimyasal form olarak kabul edilir. ⓘ
Sulu kimya

Uranyumun birçok oksidasyon durumunun tuzları suda çözünür ve sulu çözeltilerde incelenebilir. En yaygın iyonik formlar U3+
(kahverengi-kırmızı), U4+
(yeşil), UO+
2 (kararsız) ve UO2+
2 (sarı), sırasıyla U(III), U(IV), U(V) ve U(VI) için. UO ve US gibi birkaç katı ve yarı metalik bileşik uranyum(II) resmi oksidasyon durumu için mevcuttur, ancak bu durum için çözeltide basit iyonların var olduğu bilinmemektedir. U3+ iyonları
sudan hidrojen açığa çıkarır ve bu nedenle oldukça kararsız olarak kabul edilirler. UO2+
2 iyonu uranyum (VI) durumunu temsil eder ve uranil karbonat, uranil klorür ve uranil sülfat gibi bileşikler oluşturduğu bilinmektedir. UO2+
2 ayrıca çeşitli organik şelatlama maddeleriyle kompleksler oluşturur, bunlardan en sık karşılaşılanı uranil asetattır. ⓘ
Uranyumun uranil tuzları ve poliatomik iyon uranyum-oksit katyonik formlarının aksine, uranatlar, poliatomik uranyum-oksit anyonu içeren tuzlar, genellikle suda çözünmezler. ⓘ
Karbonatlar
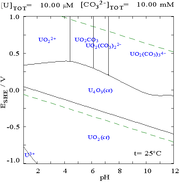
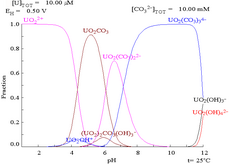
Karbonat anyonlarının uranyum(VI) ile etkileşimleri, ortam sudan karbonat içeren bir çözeltiye değiştirildiğinde Pourbaix diyagramının büyük ölçüde değişmesine neden olur. Karbonatların büyük çoğunluğu suda çözünmezken (öğrencilere genellikle alkali metaller dışındaki tüm karbonatların suda çözünmediği öğretilir), uranyum karbonatlar genellikle suda çözünür. Bunun nedeni, bir U(VI) katyonunun anyonik kompleksler oluşturmak için iki terminal oksit ve üç veya daha fazla karbonat bağlayabilmesidir. ⓘ
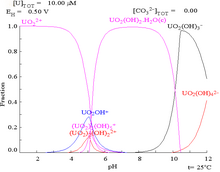
| Karmaşık olmayan sulu bir ortamda (örn. perklorik asit/sodyum hidroksit) uranyum. | Karbonat çözeltisi içinde uranyum |
| Karmaşık olmayan sulu bir ortamda (örneğin perklorik asit/sodyum hidroksit) uranyumun farklı kimyasal formlarının bağıl konsantrasyonları. | Sulu bir karbonat çözeltisinde uranyumun farklı kimyasal formlarının bağıl konsantrasyonları. |
pH'ın etkileri
Karbonat varlığında uranyum fraksiyon diyagramları bunu daha da açıklamaktadır: uranyum (VI) çözeltisinin pH'ı arttığında uranyum hidratlı uranyum oksit hidroksite dönüşür ve yüksek pH'larda anyonik bir hidroksit kompleksi haline gelir. ⓘ
Karbonat eklendiğinde, pH artırılırsa uranyum bir dizi karbonat kompleksine dönüşür. Bu reaksiyonların bir etkisi de uranyumun pH 6 ila 8 aralığında çözünürlüğünün artmasıdır ki bu da kullanılmış uranyum dioksit nükleer yakıtların uzun vadeli kararlılığı üzerinde doğrudan bir etkiye sahiptir. ⓘ
Hidrürler, karbürler ve nitrürler
250 ila 300 °C'ye (482 ila 572 °F) kadar ısıtılan uranyum metali hidrojenle tepkimeye girerek uranyum hidrür oluşturur. Daha yüksek sıcaklıklar bile hidrojeni geri dönüşümlü olarak uzaklaştıracaktır. Bu özellik, uranyum hidrürleri çeşitli uranyum karbür, nitrür ve halojenür bileşikleri ile birlikte reaktif uranyum tozu oluşturmak için uygun başlangıç malzemeleri haline getirir. Uranyum hidrürün iki kristal modifikasyonu mevcuttur: düşük sıcaklıklarda elde edilen bir α formu ve oluşum sıcaklığı 250 °C'nin üzerinde olduğunda oluşan bir β formu. ⓘ
Uranyum karbürler ve uranyum nitrürler, asitlerde çok az çözünen, suyla tepkimeye giren ve havada tutuşarak U
3O
8. Uranyum karbürleri arasında uranyum monokarbid (UC), uranyum dikarbid (UC
2) ve diuranyum trikarbid (U
2C
3). Hem UC hem de UC
2, erimiş uranyuma karbon eklenerek veya metal yüksek sıcaklıklarda karbon monoksite maruz bırakılarak oluşturulur. 1800 °C'nin altında kararlı olan U
2C
3, ısıtılmış bir UC ve UC
2 mekanik strese karşı dayanıklıdır. Metalin doğrudan azota maruz bırakılmasıyla elde edilen uranyum nitrürler arasında uranyum mononitrür (UN), uranyum dinitrür (UN
2) ve diuranyum trinitrür (U
2N
3). ⓘ
Halojenürler

Tüm uranyum florürler uranyum tetraflorür (UF
4); UF
4'ün kendisi uranyum dioksitin hidroflorinasyonu ile hazırlanır. UF'nin indirgenmesi
4 1000 °C'de hidrojen ile uranyum triflorür (UF
3). Doğru sıcaklık ve basınç koşulları altında, katı UF
4 ile gaz halindeki uranyum hekzaflorür (UF
6) U'nun ara florürlerini oluşturabilir
2F
9, U
4F
17, ve UF
5. ⓘ
Oda sıcaklığında, UF
6 yüksek buhar basıncına sahiptir, bu da onu nadir uranyum-235'i yaygın uranyum-238 izotopundan ayırmak için gaz difüzyon işleminde kullanışlı hale getirir. Bu bileşik uranyum dioksit ve uranyum hidrürden aşağıdaki işlemle hazırlanabilir:
- UO
2 + 4 HF → UF
4 + 2 H
2O (500 °C, endotermik) - UF
4 + F
2 → UF
6 (350 °C, endotermik) ⓘ
Elde edilen UF
Beyaz bir katı olan 6, oldukça reaktiftir (florlama yoluyla), kolayca süblimleşir (neredeyse ideal bir gaz gibi davranan bir buhar yayar) ve var olduğu bilinen en uçucu uranyum bileşiğidir. ⓘ
Uranyum tetraklorür (UCl) hazırlamanın bir yöntemi
4) klorun uranyum metali veya uranyum hidrür ile doğrudan birleştirilmesidir. UCl'nin indirgenmesi
4 hidrojen tarafından uranyum triklorür (UCl
3) yüksek uranyum klorürleri ise ilave klor ile reaksiyona sokularak hazırlanır. Tüm uranyum klorürler su ve hava ile reaksiyona girer. ⓘ
Uranyumun bromürleri ve iyodürleri, sırasıyla bromun ve iyodun uranyum ile doğrudan reaksiyonu veya UH
3 ile bu elementlerin asitleri arasında bir bağ vardır. Bilinen örnekler şunlardır: UBr
3, UBr
4, UI
3, ve UI
4. UI
5 hiç hazırlanmamıştır. Uranyum oksihalidler suda çözünür ve UO
2F
2, UOCl
2, UO
2Cl
2 ve UO
2Br
2. Bileşen halojenürün atom ağırlığı arttıkça oksihalojenürlerin kararlılığı azalır. ⓘ
İzotoplar
Doğal konsantrasyonlar
Doğal uranyum üç ana izotoptan oluşur: uranyum-238 (%99,28 doğal bolluk), uranyum-235 (%0,71) ve uranyum-234 (%0,0054). Bu izotopların üçü de radyoaktiftir ve alfa parçacıkları yayar, ancak bu izotopların üçünün de kendiliğinden fisyona uğrama olasılığı düşüktür. Ayrıca dört eser izotop daha vardır: 238U'nun kendiliğinden fisyona uğrayarak başka bir 238U atomu tarafından yakalanan nötronları serbest bırakmasıyla oluşan uranyum-239; 238U'nun bir nötron yakalayıp iki nötron daha yaymasıyla oluşan ve daha sonra neptünyum-237'ye bozunan uranyum-237; 235U'da nötron yakalanması nedeniyle ve plütonyum-244'ün bozunma ürünü olarak eser miktarda oluşan uranyum-236; ve son olarak, neptünyum-237'nin bozunma zincirinde oluşan uranyum-233. Ayrıca toryum-232'nin uranyum-232'yi üretecek çift beta bozunmasına uğraması beklenir, ancak bu henüz deneysel olarak gözlemlenmemiştir. Bilinen doğal örneklerde U-235'in U-238'e oranından tek önemli sapma, doğal nükleer fisyon reaktörlerinin U-235'in bir kısmını yaklaşık iki milyar yıl önce U-235'in U-238'e oranının insan yapımı hafif su reaktörlerindeki sürece benzer şekilde normal ("hafif") suyun nötron moderatörü olarak hareket etmesine izin veren düşük zenginleştirilmiş uranyuma daha yakın olduğu zaman tükettiği Oklo, Gabon'da meydana gelmiştir. Teorik olarak önceden tahmin edilen bu tür doğal fisyon reaktörlerinin varlığı, Fransa'da uranyum zenginleştirme sırasında U-235 konsantrasyonunun beklenen değerlerden hafif sapmasının keşfedilmesiyle kanıtlanmıştır. Herhangi bir kötü niyetli insan eylemini (U-235'in çalınması gibi) ekarte etmek için yapılan müteakip araştırmalar, yaygın fisyon ürünlerinin (ya da daha doğrusu bunların kararlı yavru nüklitlerinin) izotop oranlarının fisyon için beklenen değerlerle uyumlu olduğunu ancak bu elementlerin fisyondan türetilmemiş örnekleri için beklenen değerlerden saptığını tespit ederek teoriyi doğrulamıştır. ⓘ
Uranyum-238 uranyumun en kararlı izotopudur ve yarı ömrü yaklaşık 4,468×109 yıldır, yani kabaca Dünya'nın yaşı kadardır. Uranyum-235'in yarı ömrü yaklaşık 7,13×108 yıl ve uranyum-234'ün yarı ömrü yaklaşık 2,48×105 yıldır. Uranyum-238 genellikle bir alfa yayıcıdır (bazen kendiliğinden fisyona uğrar), 18 üyesi olan uranyum serisi boyunca çeşitli farklı bozunma yollarıyla kurşun-206'ya bozunur. ⓘ
Aktinyum serisi olarak adlandırılan 235U'nun bozunma zincirinin 15 üyesi vardır ve sonunda kurşun-207'ye bozunur. Bu bozunma serilerindeki sabit bozunma oranları, radyometrik tarihlendirmede ana ve yavru element oranlarının karşılaştırılmasını faydalı kılar. ⓘ
Uranyum serisinin (uranyum-238'in bozunma zinciri) bir üyesi olan uranyum-234, nispeten kısa ömürlü bir dizi izotop aracılığıyla kurşun-206'ya bozunur. ⓘ
Uranyum-233, genellikle bir nükleer reaktörde nötron bombardımanı ile toryum-232'den yapılır ve 233U da bölünebilirdir. Bozunma zinciri neptünyum serisinin bir parçasını oluşturur ve bizmut-209 ve talyum-205 ile son bulur. ⓘ
Uranyum-235 hem nükleer reaktörler hem de nükleer silahlar için önemlidir, çünkü Dünya'da doğada önemli miktarda bulunan ve bölünebilir olan tek uranyum izotopudur. Bu, termal nötronlar tarafından iki veya üç parçaya (fisyon ürünleri) bölünebileceği anlamına gelir. ⓘ
Uranyum-238 bölünebilir değildir, ancak verimli bir izotoptur, çünkü nötron aktivasyonundan sonra başka bir bölünebilir izotop olan plütonyum-239'a dönüştürülebilir. Gerçekten de 238U çekirdeği bir nötron soğurarak radyoaktif uranyum-239 izotopunu üretebilir. 239U beta emisyonu ile yine bir beta yayıcısı olan neptünyum-239'a bozunur ve bu da birkaç gün içinde plütonyum-239'a bozunur. 239Pu, 15 Temmuz 1945'te New Mexico'da "Trinity testinde" patlatılan ilk atom bombasında bölünebilir malzeme olarak kullanılmıştır. ⓘ
Zenginleştirme

Uranyum doğada uranyum-238 (%99,2742) ve uranyum-235 (%0,7204) olarak bulunur. İzotop ayrıştırma, gaz soğutmalı reaktörler ve basınçlı ağır su reaktörleri hariç, nükleer silahlar ve çoğu nükleer enerji santrali için bölünebilir uranyum-235'i yoğunlaştırır (zenginleştirir). Fisyona uğrayan bir uranyum-235 atomu tarafından salınan nötronların çoğu, nükleer zincir reaksiyonunu sürdürmek için diğer uranyum-235 atomlarına çarpmalıdır. Bunu başarmak için gereken uranyum-235 konsantrasyonu ve miktarı 'kritik kütle' olarak adlandırılır. ⓘ
'Zenginleştirilmiş' olarak kabul edilebilmesi için uranyum-235 fraksiyonunun %3 ile %5 arasında olması gerekir. Bu işlem, uranyum-235'ten arındırılmış ve buna bağlı olarak uranyum-238 oranı artmış, tükenmiş uranyum veya 'DU' olarak adlandırılan büyük miktarlarda uranyum üretir. 'Tükenmiş' olarak kabul edilebilmesi için uranyum-235 izotop konsantrasyonunun %0,3'ten fazla olmaması gerekir. Uranyumun fiyatı 2001'den bu yana arttığından, %0.35'ten fazla uranyum-235 içeren zenginleştirme artıkları yeniden zenginleştirme için değerlendirilmekte ve 2001'de 5 dolar olan seyreltilmiş uranyum hekzaflorür fiyatı Temmuz 2007'de kilogram başına 130 doların üzerine çıkmıştır. ⓘ
Gaz santrifüj işlemi, gaz halindeki uranyum hekzaflorürün (UF
6) yüksek hızlı santrifüjler kullanılarak 235UF6 ve 238UF6 arasındaki moleküler ağırlık farkı ile ayrılır, en ucuz ve önde gelen zenginleştirme işlemidir. Gaz difüzyon prosesi zenginleştirme için önde gelen yöntem olmuştur ve Manhattan Projesi'nde kullanılmıştır. Bu işlemde uranyum hekzaflorür bir gümüş-çinko zardan tekrar tekrar difüze edilir ve uranyumun farklı izotopları difüzyon hızına göre ayrılır (uranyum-238 daha ağır olduğu için uranyum-235'ten biraz daha yavaş difüze olur). Moleküler lazer izotop ayırma yöntemi, uranyum-235 ile florin arasındaki bağı koparmak için hassas enerjili bir lazer ışını kullanır. Böylece uranyum-238 florine bağlanır ve uranyum-235 metalinin çözeltiden çökelmesini sağlar. Alternatif bir lazer zenginleştirme yöntemi atomik buhar lazer izotop ayrıştırma (AVLIS) olarak bilinir ve boya lazerleri gibi görünür ayarlanabilir lazerler kullanır. Kullanılan bir diğer yöntem de sıvı termal difüzyondur. ⓘ
İnsan maruziyeti
Bir kişi havadaki tozu soluyarak ya da kirlenmiş su ve yiyecekleri yutarak uranyuma (ya da radon gibi radyoaktif kızlarına) maruz kalabilir. Havadaki uranyum miktarı genellikle çok azdır; ancak fosfatlı gübre işleyen fabrikalarda çalışan, nükleer silah üreten veya test eden devlet tesislerinin yakınında yaşayan, tükenmiş uranyum silahlarının kullanıldığı modern bir savaş alanının yakınında yaşayan veya çalışan ya da kömürle çalışan bir elektrik santralinin, uranyum cevheri çıkaran veya işleyen veya reaktör yakıtı için uranyum zenginleştiren tesislerin yakınında yaşayan veya çalışan kişiler uranyuma daha fazla maruz kalabilir. Uranyum yataklarının (doğal veya insan yapımı cüruf yatakları) üzerinde bulunan evler veya yapılarda radon gazına maruz kalma sıklığı artabilir. Mesleki Güvenlik ve Sağlık İdaresi (OSHA) işyerinde uranyum maruziyeti için izin verilen maruziyet sınırını 8 saatlik bir iş gününde 0,25 mg/m3 olarak belirlemiştir. Ulusal Mesleki Güvenlik ve Sağlık Enstitüsü (NIOSH) 8 saatlik bir iş gününde 0,2 mg/m3 tavsiye edilen maruz kalma sınırı (REL) ve 0,6 mg/m3 kısa vadeli bir sınır belirlemiştir. 10 mg/m3 seviyelerinde uranyum, yaşam ve sağlık için hemen tehlikelidir. ⓘ
Yutulan uranyumun çoğu sindirim sırasında atılır. Uranyumun oksit gibi çözünmeyen formları yutulduğunda sadece %0,5'i emilirken, daha çözünür olan uranil iyonunun emilimi %5'e kadar çıkabilir. Bununla birlikte, çözünür uranyum bileşikleri vücuttan hızla geçme eğilimindeyken, çözünmeyen uranyum bileşikleri, özellikle akciğerlere toz yoluyla solunduğunda, daha ciddi bir maruz kalma tehlikesi oluşturur. Kan dolaşımına girdikten sonra, emilen uranyum biyolojik olarak birikme eğilimindedir ve uranyumun fosfatlara olan afinitesi nedeniyle kemik dokusunda uzun yıllar kalır. Uranyum deri yoluyla emilmez ve uranyum tarafından salınan alfa parçacıkları deriye nüfuz edemez. ⓘ
Birleşen uranyum, kemik, karaciğer, böbrek ve üreme dokularında biriken uranil iyonlarına dönüşür. Uranyum çelik yüzeylerden ve akiferlerden arındırılabilir. ⓘ
Etkiler ve önlemler
Böbrek, beyin, karaciğer, kalp ve diğer sistemlerin normal işleyişi uranyum maruziyetinden etkilenebilir, çünkü uranyum zayıf radyoaktif olmasının yanı sıra toksik bir metaldir. Uranyum aynı zamanda bir üreme toksik maddesidir. Radyolojik etkiler genellikle lokaldir çünkü 238U bozunmasının birincil formu olan alfa radyasyonu çok kısa bir menzile sahiptir ve cilde nüfuz etmez. Solunan uranyumdan kaynaklanan alfa radyasyonunun maruz kalan nükleer işçilerde akciğer kanserine neden olduğu gösterilmiştir. Uranil (UO2+
2) uranyum trioksit veya uranil nitrat ve diğer altı değerlikli uranyum bileşikleri gibi iyonların laboratuvar hayvanlarında doğum kusurlarına ve bağışıklık sistemi hasarına neden olduğu gösterilmiştir. CDC, doğal veya tükenmiş uranyuma maruz kalmanın bir sonucu olarak insanlarda kanser görülmediğine dair bir çalışma yayınlamış olsa da, uranyum ve bozunma ürünlerine, özellikle de radona maruz kalmak yaygın olarak bilinen ve önemli sağlık tehditleridir. Stronsiyum-90, iyot-131 ve diğer fisyon ürünlerine maruz kalmanın uranyum maruziyeti ile ilgisi yoktur, ancak tıbbi prosedürlerden veya kullanılmış reaktör yakıtına veya nükleer silahlardan kaynaklanan serpintilere maruz kalmaktan kaynaklanabilir.
Yüksek konsantrasyonda uranyum hekzaflorüre kazara solunması halinde maruz kalınmasına rağmen
insan ölümleriyle sonuçlansa da, bu ölümler uranyumun kendisinden ziyade yüksek derecede zehirli hidroflorik asit ve uranil florür oluşumuyla ilişkilendirilmiştir. İnce bölünmüş uranyum metali yangın tehlikesi arz eder çünkü uranyum piroforiktir; küçük taneler oda sıcaklığında havada kendiliğinden tutuşur. ⓘ
Uranyum metali genellikle yeterli bir önlem olarak eldivenle taşınır. Uranyum konsantresi, insanların solumamasını veya yutmamasını sağlayacak şekilde ele alınır ve muhafaza edilir. ⓘ
| Vücut sistemi | İnsan çalışmaları | Hayvan çalışmaları | In vitro |
|---|---|---|---|
| Böbrek | Yüksek protein atılımı, idrar katalazı ve diürez seviyeleri | Proksimal kıvrımlı tübüllerde hasar, tübüler epitelden dökülen nekrotik hücreler, glomerüler değişiklikler (böbrek yetmezliği) | Çalışma yok |
| Beyin/CNS | Nörobilişsel testlerde performans azalması | Akut kolinerjik toksisite; Korteks, orta beyin ve vermiste doza bağlı birikim; Hipokampusta elektrofizyolojik değişiklikler | Çalışma yok |
| DNA | Kanser raporlarında artış | Artmış mutajenite (farelerde) ve tümör indüksiyonu | Mikronükleuslu çift çekirdekli hücreler, Hücre döngüsü kinetiği ve proliferasyonun inhibisyonu; Kardeş kromatid indüksiyonu, tümörijenik fenotip |
| Kemik/kas | Çalışma yok | Periodontal kemik oluşumunun engellenmesi; ve alveolar yara iyileşmesi | Çalışma yok |
| Üreme | Uranyum madencilerinin ilk doğan kız çocukları daha fazla | Orta ila şiddetli fokal tübüler atrofi; Leydig hücrelerinde vakuolizasyon | Çalışma yok |
| Akciğerler/solunum | Sağlık üzerinde herhangi bir olumsuz etki bildirilmemiştir | Şiddetli burun tıkanıklığı ve kanaması, akciğer lezyonları ve fibrozis, ödem ve şişlik, akciğer kanseri | Çalışma yok |
| Gastrointestinal | Kusma, ishal, albüminüri | Çalışma yok | Çalışma yok |
| Karaciğer | Maruz kalma dozunda etki görülmedi | Yağlı karaciğerler, fokal nekroz | Çalışma yok |
| Cilt | Maruziyet değerlendirme verisi mevcut değildir | Şişmiş vakuollü epidermal hücreler, kıl foliküllerinde ve yağ bezlerinde hasar | Çalışma yok |
| Gömülü DU parçalarını çevreleyen dokular | Yüksek uranyum idrar konsantrasyonları | Yüksek uranyum idrar konsantrasyonları, biyokimyasal ve nöropsikolojik testlerde bozulmalar | Çalışma yok |
| Bağışıklık sistemi | Kronik yorgunluk, döküntü, kulak ve göz enfeksiyonları, saç ve kilo kaybı, öksürük. Tek başına DU'dan ziyade kombine kimyasal maruziyete bağlı olabilir | Çalışma yok | Çalışma yok |
| Gözler | Çalışma yok | Konjonktivit, irritasyon iltihabı, ödem, konjonktival keselerde ülserasyon | Çalışma yok |
| Kan | Çalışma yok | RBC sayısında ve hemoglobin konsantrasyonunda azalma | Çalışma yok |
| Kardiyovasküler | Uranyum alımından kaynaklanan ve alımdan altı ay sonra sona eren miyokardit | Etkisi yok | Çalışma yok |