Kalay
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kalay | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Allotroplar | gümüşi beyaz, β (beta); gri, α (alfa) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Standart atom ağırlığı Ar°(Sn) |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Periyodik tabloda kalay | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atom numarası (Z) | 50 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grup | grup 14 (karbon grubu) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dönem | dönem 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | p-blok | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektron konfigürasyonu | [[[Kripton|Kr]]] 4d10 5s2 5p2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kabuk başına elektron | 2, 8, 18, 18, 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fiziksel özellikler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| STP'de Faz | katı | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Erime noktası | 505,08 K (231,93 °C, 449,47 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kaynama noktası | 2875 K (2602 °C, 4716 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Yoğunluk (r.t.'ye yakın) | beyaz, β: 7,265 g/cm3 gri, α: 5,769 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| sıvı olduğunda (m.p.'de) | 6,99 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Füzyon ısısı | beyaz, β: 7,03 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Buharlaşma ısısı | beyaz, β: 296,1 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar ısı kapasitesi | beyaz, β: 27,112 J/(mol-K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Buhar basıncı
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomik özellikler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oksidasyon durumları | -4, -3, -2, -1, 0, +1, +2, +3, +4 (amfoterik bir oksit) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegatiflik | Pauling ölçeği: 1.96 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| İyonlaşma enerjileri |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomik yarıçap | ampi̇ri̇k: 140 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalent yarıçap | 139±4 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waals yarıçapı | 217 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kalayın spektral çizgileri | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Diğer özellikler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Doğal oluşum | ilkel | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristal yapı | gövde merkezli tetragonal beyaz (β) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristal yapı | yüz merkezli elmas-kübik gri (α) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ses hızı ince çubuk | 2730 m/s (r.t.'de) (yuvarlanmış) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termal genleşme | 22,0 µm/(m⋅K) (25 °C'de) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termal iletkenlik | 66,8 W/(m⋅K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektriksel direnç | 115 nΩ⋅m (0 °C'de) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Manyetik sipariş | gri: diamanyetik beyaz (β): paramanyetik | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar manyetik duyarlılık | (beyaz) +3,1×10-6 cm3/mol (298 K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Young modülü | 50 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kayma modülü | 18 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Yığın modülü | 58 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Poisson oranı | 0.36 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohs sertliği | 1.5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brinell sertliği | 50-440 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS Numarası | 7440-31-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tarih | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Keşif | protohistorik, yaklaşık MÖ 35. yüzyıl | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sembol | "Sn": Latince stannum'dan | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kalayın ana izotopları | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Kalay, sembolü Sn (Latince: stannum) ve atom numarası 50 olan kimyasal bir elementtir. Kalay gümüşi renkli bir metaldir. ⓘ
Kalay az bir kuvvetle kesilebilecek kadar yumuşaktır ve bir kalay çubuğu elle az bir çabayla bükülebilir. Büküldüğünde, kalay kristallerindeki ikizlenmenin bir sonucu olarak "kalay ağlaması" olarak adlandırılan ses duyulabilir; bu özellik katı halde indiyum, kadmiyum, çinko ve cıva tarafından paylaşılır. ⓘ
Katılaştıktan sonra saf kalay, çoğu metale benzer ayna benzeri bir görünüm sunar. Çoğu kalay alaşımında (kalay gibi) metal donuk gri bir renkle katılaşır. ⓘ
Kalay, periyodik element tablosunun 14. grubunda yer alan bir geçiş sonrası metalidir. Esas olarak stannik oksit içeren kasiterit mineralinden elde edilir, SnO
2. Kalay, 14. gruptaki komşuları germanyum ve kurşun ile kimyasal benzerlik gösterir ve +2 ve biraz daha kararlı olan +4 olmak üzere iki ana oksidasyon durumuna sahiptir. Kalay, Dünya'da en çok bulunan 49. elementtir ve 10 kararlı izotopu ile periyodik tablodaki en fazla sayıda kararlı izotopa sahiptir, sihirli proton sayısı sayesinde. ⓘ
İki ana allotropa sahiptir: oda sıcaklığında, kararlı allotrop gümüşi beyaz, dövülebilir bir metal olan β-kalaydır; düşük sıcaklıklarda elmas kübik yapıya sahip daha az yoğun gri α-kalaydır. Metalik kalay havada ve suda kolayca oksitlenmez. ⓘ
Büyük ölçekte kullanılan ilk kalay alaşımı, MÖ 3000 gibi erken bir tarihte 1⁄8 kalay ve 7⁄8 bakırdan yapılan bronzdu. MÖ 600'den sonra saf metalik kalay üretilmiştir. 85-90 kalay alaşımı olan ve geri kalanı genellikle bakır, antimon, bizmut ve bazen kurşun ve gümüşten oluşan kalay, Bronz Çağı'ndan beri sofra takımları için kullanılmıştır. Modern zamanlarda kalay, başta tipik olarak %60 veya daha fazla kalay içeren kalay / kurşun yumuşak lehimler olmak üzere birçok alaşımda ve optoelektronik uygulamalarda şeffaf, elektriksel olarak iletken indiyum kalay oksit filmlerinin üretiminde kullanılmaktadır. Bir diğer büyük uygulama ise çeliğin korozyona dayanıklı kalay kaplamasıdır. İnorganik kalayın düşük toksisitesi nedeniyle, kalay kaplı çelik, teneke kutular olarak gıda ambalajı için yaygın olarak kullanılmaktadır. Bazı organotin bileşikleri son derece toksik olabilir. ⓘ
Özellikleri
Fiziksel

Kalay yumuşak, dövülebilir, sünek ve yüksek kristalli gümüşi beyaz bir metaldir. Bir kalay çubuğu büküldüğünde, kristallerin ikizlenmesinden "kalay ağlaması" olarak bilinen bir çatırtı sesi duyulabilir. Kalay yaklaşık 232 °C'de (450 °F) erir ve 14. gruptaki en düşük sıcaklıktır. Erime noktası 11 nm parçacıklar için 177,3 °C'ye (351,1 °F) kadar düşer. ⓘ
| Harici video ⓘ | |
|---|---|
Metalik form veya beyaz kalay olan β-kalay, BCT yapısına sahiptir ve oda sıcaklığında ve üzerinde kararlıdır ve dövülebilir. Metalik olmayan form veya gri kalay olan α-kalay, 13,2 ° C'nin (55,8 ° F) altında kararlıdır ve kırılgandır. α-kalay, elmas, silikon veya germanyuma benzer bir elmas kübik kristal yapısına sahiptir. α-kalay metalik özelliklere sahip değildir, çünkü atomları elektronların serbestçe hareket edemediği kovalent bir yapı oluşturur. α-kalay, özel yarı iletken uygulamaları dışında yaygın kullanımı olmayan donuk gri toz halinde bir malzemedir. γ-tin ve σ-tin 161 °C'nin (322 °F) üzerindeki sıcaklıklarda ve birkaç GPa'nın üzerindeki basınçlarda bulunur. ⓘ
Soğuk koşullarda β-kalay kendiliğinden α-kalay'a dönüşme eğilimindedir, bu da "kalay zararlısı" veya "kalay hastalığı" olarak bilinen bir olgudur. Bazı doğrulanamayan kaynaklarda Napolyon'un 1812 Rusya seferi sırasında hava o kadar soğuktu ki, askerlerin üniformalarındaki kalay düğmeler zamanla parçalanarak Grande Armée'nin yenilgisine katkıda bulunduğundan bahsedilir ki bu da kalıcı bir efsanedir. ⓘ
α-β dönüşüm sıcaklığı 13,2 °C'dir (55,8 °F), ancak safsızlıklar (örneğin Al, Zn, vb.) bunu 0 °C'nin (32 °F) çok altına düşürür. Antimon veya bizmut ilavesiyle dönüşüm hiç gerçekleşmeyebilir ve dayanıklılık artar. ⓘ
Ticari kalay sınıfları (%99,8 kalay içeriği), safsızlık olarak bulunan az miktarda bizmut, antimon, kurşun ve gümüşün engelleyici etkisi nedeniyle dönüşüme direnç gösterir. Bakır, antimon, bizmut, kadmiyum ve gümüş gibi alaşım elementleri kalayın sertliğini arttırır. Kalay kolayca, tipik olarak istenmeyen sert, kırılgan intermetalik fazlar oluşturur. Çoğu metal ve elementle bir çözeltiye karışmaz, bu nedenle kalayın fazla katı çözünürlüğü yoktur. Kalay, basit ötektik sistemler oluşturan bizmut, galyum, kurşun, talyum ve çinko ile iyi karışır. ⓘ
Kalay 3.72 K'nin altında bir süper iletken haline gelir ve üzerinde çalışılan ilk süper iletkenlerden biridir. Süper iletkenlerin karakteristik özelliklerinden biri olan Meissner etkisi ilk olarak süper iletken kalay kristallerinde keşfedilmiştir. ⓘ
Kimyasal
Kalay sudan kaynaklanan korozyona karşı dirençlidir, ancak asitler ve alkaliler tarafından aşındırılabilir. Kalay yüksek derecede parlatılabilir ve diğer metaller için koruyucu bir kaplama olarak kullanılır, koruyucu bir oksit (pasivasyon) tabakası daha fazla oksidasyonu önler. Kalay, oksijen içeren bir çözeltinin kimyasal reaksiyonunu tetikleyen bir katalizör görevi görür ve sonuçta ortaya çıkan kimyasal reaksiyonun hızını artırmaya yardımcı olur. ⓘ
İzotoplar
Kalayın on kararlı izotopu vardır, bu sayı herhangi bir elementin en büyük sayısıdır. Kalay izotoplarının atom kütleleri 112, 114, 115, 116, 117, 118, 119, 120, 122 ve 124'tür. 120Sn tüm kalayın neredeyse üçte birini oluşturur; 118Sn ve 116Sn de yaygındır, 115Sn ise en az yaygın olan kararlı izotoptur. Çift kütle numarasına sahip izotopların nükleer spini yoktur, tek kütle numarasına sahip olanların ise 1/2 spini vardır. Kalay, moleküler ağırlığa dayanan NMR spektroskopisi ile tespit edilmesi ve analiz edilmesi en kolay elementler arasındadır ve kimyasal kaymaları SnMe
4. Çok sayıda kararlı izotopun, kalayın nükleer fizikte bir "sihirli sayı" olan 50 atom numarasına sahip olmasının doğrudan bir sonucu olduğu düşünülmektedir. ⓘ
Kalayın kütle numarası 99 ila 139 arasında değişen 31 kararsız izotopu vardır. Kararsız kalay izotoplarının, 230.000 yıllık bir yarı ömre sahip olan 126Sn hariç, bir yıldan daha az bir yarı ömrü vardır. 100Sn ve 132Sn "çift sihirli" çekirdeğe sahip az sayıdaki nüklitten ikisidir ve çok düzensiz nötron-proton oranlarına sahip oldukları için kararsız olmalarına rağmen, 100Sn'den daha hafif ve 132Sn'den daha ağır kalay izotoplarının çok daha az kararlı olduğu uç noktalardır. 111 ve 131 arasındaki kalay izotopları için 30 metastabil izomer daha tanımlanmıştır, en kararlı olanı 43,9 yıllık yarı ömrü ile 121mSn'dir. ⓘ
Kalayın kararlı izotoplarının sayısındaki göreceli farklılıklar, yıldız nükleosentezi sırasında nasıl oluştukları ile açıklanabilir. 116Sn'den 120Sn'ye kadar olan izotoplar çoğu yıldızda s-sürecinde (yavaş nötron yakalama) oluşur ve bu da en yaygın kalay izotopları olmalarına yol açar. 122Sn ve 124Sn ise yalnızca süpernovalardaki r-sürecinde (hızlı nötron yakalama) oluşur ve daha az yaygındır. 117Sn ile 120Sn arasındaki kalay izotopları da r-sürecinde üretilir. 112Sn, 114Sn ve 115Sn, s- veya r-süreçlerinde önemli miktarlarda üretilemez ve kökenleri iyi anlaşılmamış p-çekirdekleri arasındadır. Oluşumları hakkındaki bazı fikirler proton yakalama ve fotodintegrasyonu içerir. 115Sn kısmen s-sürecinde hem doğrudan hem de uzun ömürlü 115In'in kızı olarak üretilebilir. ⓘ
Etimoloji
Tin sözcüğü Cermen dilleri arasında paylaşılır ve yeniden yapılandırılmış Proto-Germence *tin-om'a kadar izlenebilir; soydaşları arasında Almanca Zinn, İsveççe tenn ve Felemenkçe tin bulunur. Hint-Avrupa'nın diğer kollarında, Cermen dilinden ödünç alma (örneğin, İrlandaca tinne İngilizceden) dışında bulunmaz. ⓘ
Latince stannum adı başlangıçta gümüş ve kurşun alaşımı anlamına geliyordu ve dördüncü yüzyılda 'kalay' anlamına geldi - daha önceki Latince kelime plumbum candidum veya "beyaz kurşun" idi. Görünüşe göre stannum, kalay için kullanılan Roman ve Kelt terimlerinin kökeni olan daha eski bir stāgnum'dan (aynı madde anlamına gelir) gelmektedir. Stannum/stāgnum'un kökeni bilinmemektedir; Hint-Avrupa öncesi olabilir. ⓘ
Meyers Konversations-Lexikon bunun yerine stannum'un Cornish stean'dan geldiğini ve MS ilk yüzyıllarda Cornwall'un ana kalay kaynağı olduğunun kanıtı olduğunu öne sürer. ⓘ
Tarih

Kalayın çıkarılması ve kullanımı, farklı metal içeriklerine sahip polimetalik cevherlerden oluşan bakır nesnelerin farklı fiziksel özelliklere sahip olduğunun gözlemlendiği MÖ 3000 civarında Bronz Çağı'nın başlangıcına tarihlendirilebilir. En eski bronz nesnelerin kalay veya arsenik içeriği %2'den azdı ve bakır cevherindeki eser metal içeriğine bağlı olarak kasıtsız alaşımlanmanın bir sonucu olduğuna inanılıyordu. Bakıra ikinci bir metalin eklenmesi sertliğini arttırır, erime sıcaklığını düşürür ve daha yoğun, daha az süngerimsi bir metale soğuyan daha akışkan bir eriyik üreterek döküm sürecini iyileştirir. Bu, Bronz Çağı'nın kapalı kalıplarında dökülen çok daha karmaşık şekillere izin veren önemli bir yenilikti. Arsenikli bronz nesneler ilk olarak arseniğin bakır cevheriyle birlikte yaygın olarak bulunduğu Yakın Doğu'da ortaya çıkmıştır, ancak sağlık riskleri kısa sürede fark edilmiş ve Bronz Çağı'nın başlarında çok daha az tehlikeli olan kalay cevherleri için kaynak arayışı başlamıştır. Bu durum nadir bulunan kalay metaline talep yaratmış ve uzak kalay kaynaklarını Bronz Çağı kültürlerinin pazarlarına bağlayan bir ticaret ağı oluşturmuştur. ⓘ
Kasiterit (SnO
2), kalayın oksit formu, büyük olasılıkla kalayın orijinal kaynağıydı. Diğer kalay cevherleri, stannit gibi daha az yaygın olan ve daha kapsamlı bir eritme işlemi gerektiren sülfürlerdir. Kasiterit genellikle alüvyon kanallarında plaser yatakları olarak birikir çünkü beraberindeki granitten daha sert, daha ağır ve kimyasal olarak daha dirençlidir. Kassiterit genellikle siyah veya koyu renklidir ve bu birikintiler nehir kıyılarında kolayca görülebilir. Alüvyal (plaser) tortular tesadüfen altın aramaya benzer yöntemlerle toplanmış ve ayrılmış olabilir. ⓘ
Bileşikler ve kimya
Bileşiklerinin büyük çoğunluğunda kalay, II veya IV oksidasyon durumuna sahiptir. ⓘ
İnorganik bileşikler
Halojenür bileşikleri her iki oksidasyon durumu için de bilinmektedir. Sn(IV) için dört halojenür de iyi bilinmektedir: SnF4, SnCl4, SnBr4 ve SnI4. Daha ağır olan üç üye uçucu moleküler bileşiklerken, tetraflorür polimeriktir. Dört halojenür de Sn(II) için bilinmektedir: SnF2, SnCl
2, SnBr2 ve SnI2. Hepsi polimerik katılardır. Bu sekiz bileşikten sadece iyodürler renklidir. ⓘ
Kalay(II) klorür (stannöz klorür olarak da bilinir) en önemli ticari kalay halojenürdür. Bu tür bileşiklere giden yolları göstermek gerekirse, klor kalay metali ile reaksiyona girerek SnCl4 verirken, hidroklorik asit ve kalay reaksiyonu SnCl
2 ve hidrojen gazından oluşur. Alternatif olarak SnCl4 ve Sn, bileşik oranlama adı verilen bir işlemle stannöz klorüre dönüşür:
- SnCl4 + Sn → 2 SnCl
2 ⓘ
Kalay birçok oksit, sülfit ve diğer kalkojenit türevlerini oluşturabilir. Dioksit SnO
2 (kasiterit) kalay hava varlığında ısıtıldığında oluşur. Sn)
2 amfoteriktir, yani hem asidik hem de bazik çözeltilerde çözünür. Sn(OH) yapısına sahip stannatlar
6]2-, K gibi
2[Sn(OH)
6], ayrıca serbest stannik asit H
2[Sn(OH)
6] bilinmemektedir. ⓘ
Kalay sülfürleri hem +2 hem de +4 oksidasyon durumlarında mevcuttur: kalay(II) sülfür ve kalay(IV) sülfür (mozaik altın). ⓘ
Hidrürler
Stannan (SnH
4), +4 oksidasyon durumundaki kalay ile kararsızdır. Ancak organotin hidrürler iyi bilinmektedir, örneğin tribütiltin hidrit (Sn(C4H9)3H). Bu bileşikler, kalay(III) bileşiklerinin nadir örnekleri olan geçici tributil kalay radikallerini serbest bırakır. ⓘ
Organotin bileşikleri
Bazen stannan olarak da adlandırılan organotin bileşikleri, kalay-karbon bağı içeren kimyasal bileşiklerdir. Kalay bileşiklerinden organik türevleri ticari olarak en kullanışlı olanlarıdır. Bazı organotin bileşikleri oldukça toksiktir ve biyosit olarak kullanılmıştır. Rapor edilen ilk organotin bileşiği 1849 yılında Edward Frankland tarafından rapor edilen dietiltin diiyodürdür ((C2H5)2SnI2). ⓘ
Organotin bileşiklerinin çoğu renksiz sıvılar veya hava ve suya karşı kararlı katılardır. Tetrahedral geometriyi benimserler. Tetraalkil ve tetraariltin bileşikleri Grignard reaktifleri kullanılarak hazırlanabilir:
- SnCl
4 + 4 RMgBr → R
4Sn + 4 MgBrCl
Tetraorgano türevlerinden daha yaygın ve ticari olarak daha önemli olan karışık halojenür-alkiller, yeniden dağılım reaksiyonları ile hazırlanır:
- SnCl
4 + R
4Sn → 2 SnCl
2R2 ⓘ
İki değerlikli organotin bileşikleri nadirdir, ancak ilgili iki değerlikli organogermanyum ve organosilikon bileşiklerinden daha yaygındır. Sn(II)'nin sahip olduğu daha büyük stabilizasyon "inert çift etkisine" bağlanmaktadır. Organotin(II) bileşikleri hem stannylenleri (formül: R2Sn, singlet karbenlerde görüldüğü gibi) hem de kabaca alkenlere eşdeğer olan distannylenleri (R4Sn2) içerir. Her iki sınıf da alışılmadık reaksiyonlar sergiler. ⓘ
Oluşum

Kalay, düşük ila orta kütleli yıldızlarda (Güneş'in 0,6 ila 10 katı kütleli) uzun s süreci ve son olarak da ağır indiyum izotoplarının beta bozunumu yoluyla üretilir. ⓘ
Kalay, Dünya'nın kabuğunda en bol bulunan 49. elementtir ve çinko için 75 ppm, bakır için 50 ppm ve kurşun için 14 ppm ile karşılaştırıldığında 2 ppm'i temsil eder. ⓘ
Kalay doğal element olarak bulunmaz ancak çeşitli cevherlerden çıkarılması gerekir. Kasiterit (SnO
2) ticari açıdan önemli tek kalay kaynağıdır, ancak stannit, silindirit, frankeit, canfieldit ve teallit gibi kompleks sülfitlerden az miktarda kalay elde edilir. Kalay içeren mineraller neredeyse her zaman granit kayasıyla ilişkilidir ve genellikle %1 kalay oksit içeriğine sahiptir. ⓘ
Kalay dioksitin daha yüksek özgül ağırlığı nedeniyle, çıkarılan kalayın yaklaşık %80'i birincil lodlardan aşağı akış yönünde bulunan ikincil yataklardan elde edilir. Kalay genellikle geçmişte akıntıya karşı yıkanan ve vadilerde veya denizde biriken granüllerden geri kazanılır. Kalay madenciliğinin en ekonomik yolları tarama, hidrolik veya açık ocaklardır. Dünyadaki kalayın çoğu, %0,015 kadar az kalay içerebilen plaser yataklarından üretilmektedir. ⓘ
| Ülke | Rezervler |
|---|---|
| 1,500,000 | |
| 250,000 | |
| 310,000 | |
| 800,000 | |
| 590,000 | |
| 400,000 | |
| 350,000 | |
| 180,000 | |
| 170,000 | |
| Diğer | 180,000 |
| Toplam | 4,800,000 |
| Yıl | Milyon ton ⓘ |
|---|---|
| 1965 | 4,265 |
| 1970 | 3,930 |
| 1975 | 9,060 |
| 1980 | 9,100 |
| 1985 | 3,060 |
| 1990 | 7,100 |
| 2000 | 7,100 |
| 2010 | 5,200 |
2011 yılında çoğunluğu Çin (110.000 t), Endonezya (51.000 t), Peru (34.600 t), Bolivya (20.700 t) ve Brezilya'da (12.000 t) olmak üzere yaklaşık 253.000 ton kalay çıkarılmıştır. Kalay üretimine ilişkin tahminler tarihsel olarak pazara ve madencilik teknolojisine göre değişiklik göstermiştir. Mevcut tüketim oranları ve teknolojilerle, Dünya'nın 40 yıl içinde madene elverişli kalayının tükeneceği tahmin edilmektedir. 2006 yılında Lester Brown, yıllık %2 büyüme gibi muhafazakar tahminlere dayanarak kalayın 20 yıl içinde tükenebileceğini öne sürmüştür. ⓘ
Hurda kalay önemli bir metal kaynağıdır. Kalayın geri dönüşüm yoluyla geri kazanımı hızla artmaktadır. Amerika Birleşik Devletleri ne kalay çıkarmış (1993'ten beri) ne de eritmiş (1989'dan beri) olsa da, 2006'da yaklaşık 14.000 ton geri dönüştürerek en büyük ikincil üretici olmuştur. ⓘ
Moğolistan'da yeni yataklar rapor edilmiştir ve 2009 yılında Kolombiya'da yeni kalay yatakları keşfedilmiştir. ⓘ
Üretim
Kalay, oksit cevherinin karbon veya kok ile karbotermik indirgenmesi ile üretilir. Hem reverber fırını hem de elektrikli fırın kullanılabilir. ⓘ
Endüstri
En büyük on şirket 2007 yılında dünyadaki kalayın çoğunu üretmiştir. ⓘ
Dünyadaki kalayın çoğu LME'de, 8 ülkeden, 17 marka altında işlem görmektedir. ⓘ
| Şirket | Polity | 2006 | 2007 | 2017 | 2006-2017 % değişim |
|---|---|---|---|---|---|
| Yunnan Kalay | Çin | 52,339 | 61,129 | 74,500 | 42.3 |
| PT Timah | Endonezya | 44,689 | 58,325 | 30,200 | -32.4 |
| Malaysia Smelting Corp | Malezya | 22,850 | 25,471 | 27,200 | 19.0 |
| Yunnan Chengfeng | Çin | 21,765 | 18,000 | 26,800 | 23.1 |
| Minsur | Peru | 40,977 | 35,940 | 18,000 | -56.1 |
| EM Vinto | Bolivya | 11,804 | 9,448 | 12,600 | 6.7 |
| Guangxi Çin Kalay | Çin | / | / | 11,500 | / |
| Thaisarco | Tayland | 27,828 | 19,826 | 10,600 | -61.9 |
| Metallo-Chimique | Belçika | 8,049 | 8,372 | 9,700 | 20.5 |
| Gejiu Zi Li | Çin | / | / | 8,700 | / |
Uluslararası Kalay Konseyi 1947 yılında kalay fiyatlarını kontrol etmek amacıyla kurulmuştur. Konsey 1985 yılında dağıldı. 1984 yılında Avustralya, Bolivya, Endonezya, Malezya, Nijerya, Tayland ve Zaire'nin üye olduğu Kalay Üreten Ülkeler Birliği kuruldu. ⓘ
Fiyat ve borsalar
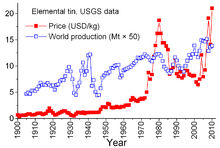
Kalay, üretici ülkeler ile tüketici ülkeler arasında 1921 yılına kadar uzanan karmaşık anlaşmalar nedeniyle mineral emtialar arasında benzersizdir. Daha önceki anlaşmalar biraz gayri resmi olma eğilimindeydi ve 1956'da "Birinci Uluslararası Kalay Anlaşması "na yol açtı, 1985'te etkili bir şekilde çöken bir serinin ilki. Bu anlaşmalar sayesinde Uluslararası Kalay Konseyi (ITC) kalay fiyatları üzerinde önemli bir etkiye sahip olmuştur. ITC, fiyatların düşük olduğu dönemlerde tampon stoku için kalay satın alarak kalay fiyatını destekledi ve fiyatların yüksek olduğu dönemlerde stoktan satış yaparak fiyatı dizginleyebildi. Bu serbest piyasa karşıtı bir yaklaşımdı ve tüketici ülkelere yeterli miktarda kalay akışını ve üretici ülkelerin kâr etmesini sağlamak için tasarlanmıştı. Ancak, tampon stok yeterince büyük değildi ve bu 29 yılın çoğunda kalay fiyatları, özellikle de enflasyonun birçok dünya ekonomisini sarstığı 1973'ten 1980'e kadar bazen keskin bir şekilde yükseldi. ⓘ
1970'lerin sonu ve 1980'lerin başında ABD, kısmen tarihsel olarak yüksek kalay fiyatlarından yararlanmak için stratejik kalay stokunu azalttı. 1981-82 resesyonu kalay endüstrisine zarar verdi. Kalay tüketimi önemli ölçüde azaldı. ITC, tampon stoku için hızlandırılmış alımlar yaparak gerçekten keskin düşüşlerden kaçınabildi; bu faaliyet kapsamlı borçlanma gerektirdi. ITC, kredi limitine ulaştığı 1985 yılının sonlarına kadar borçlanmaya devam etti. Hemen büyük bir "kalay krizi" ortaya çıktı ve kalay yaklaşık üç yıl boyunca Londra Metal Borsası'nda işlem görmekten men edildi. ITC kısa bir süre sonra dağıldı ve artık serbest piyasa ortamında olan kalayın fiyatı pound başına 4 dolara düştü ve 1990'lar boyunca bu seviyede kaldı. Fiyat, 2007-2008 ekonomik krizinin ardından tüketimde yaşanan toparlanma, buna eşlik eden yeniden stoklama ve tüketimde devam eden büyüme ile birlikte 2010 yılına kadar tekrar yükselmiştir. ⓘ
Londra Metal Borsası (LME) kalayın başlıca ticaret yeridir. Diğer kalay kontrat piyasaları Kuala Lumpur Kalay Piyasası (KLTM) ve Endonezya Kalay Borsası'dır (INATIN). ⓘ
2021'deki küresel tedarik zinciri krizine dahil olan faktörler nedeniyle, kalay fiyatları 2020-21 arasında neredeyse iki katına çıktı ve 30 yılı aşkın süredir en büyük yıllık artışını yaşadı. Uluslararası Kalay Birliği, COVID-19 salgınının küresel imalat sanayilerini sekteye uğratması nedeniyle 2020'de yüzde 1,6 gerileyen küresel rafine kalay tüketiminin 2021'de yüzde 7,2 artacağını tahmin ediyor. ⓘ
Yıllar içinde kg başına fiyat:
| 2008 | 2009 | 2010 | 2011 | 2012 | 2021 ⓘ | |
|---|---|---|---|---|---|---|
| Fiyat | 18.51 | 13.57 | 20.41 | 26.05 | 21.13 | 38.67 |
Uygulamalar
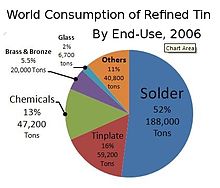
2018 yılında üretilen tüm kalayın yarısından biraz azı lehimde kullanılmıştır. Geri kalanı ise kalay kaplama, kalay kimyasalları, pirinç ve bronz alaşımları ve niş kullanımlar arasında paylaştırıldı. ⓘ
Lehim

Kalay uzun zamandır kurşun ile alaşımlarda lehim olarak %5 ila %70 w/w miktarlarında kullanılmaktadır. Kurşun ile kalay, ağırlıkça %61,9 kalay ve %38,1 kurşun oranında (atomik oran: %73,9 kalay ve %26,1 kurşun), 183 °C (361,4 °F) erime sıcaklığında ötektik bir karışım oluşturur. Bu tür lehimler öncelikle boruları veya elektrik devrelerini birleştirmek için kullanılır. Avrupa Birliği Atık Elektrikli ve Elektronik Ekipman Direktifi (WEEE Direktifi) ve Tehlikeli Maddelerin Kısıtlanması Direktifi 1 Temmuz 2006 tarihinde yürürlüğe girdiğinden beri, bu tür alaşımlardaki kurşun içeriği azalmıştır. Kurşuna maruz kalma ciddi sağlık sorunlarıyla ilişkilendirilse de, kurşunsuz lehimin daha yüksek erime noktası ve elektrik sorunlarına neden olan kalay bıyıklarının oluşumu gibi zorlukları da yok değildir. Kurşunsuz lehimlerde kalay zararlısı oluşabilir ve bu da lehimli bağlantının kaybına yol açabilir. İkame alaşımlar bulunmakta, ancak bağlantı bütünlüğü sorunları devam etmektedir. ⓘ
Kalay kaplama

Kalay demire kolayca bağlanır ve korozyonu önlemek için kurşun, çinko ve çeliğin kaplanmasında kullanılır. Kalay kaplı (veya kalaylanmış) çelik kaplar gıda muhafazası için yaygın olarak kullanılır ve bu metalik kalay pazarının büyük bir bölümünü oluşturur. Yiyecekleri muhafaza etmek için teneke kutu ilk kez 1812 yılında Londra'da üretilmiştir. İngiliz İngilizcesi konuşanlar bu tür kapları "tins" olarak adlandırırken, Amerikan İngilizcesi konuşanlar "cans" veya "tin cans" olarak adlandırmaktadır. Bu tür kullanımın bir türevi, Avustralya'da "kutu bira" anlamına gelen "tinnie" veya "tinny" argo terimidir. Teneke düdük, ilk olarak kalay kaplı çelikten seri olarak üretildiği için bu şekilde adlandırılmıştır. ⓘ
Tencere ve tava gibi bakır pişirme kaplarının asitli gıdalarla kullanımı zehirli olabileceğinden, elektrokaplama veya geleneksel kimyasal yöntemlerle sıklıkla ince bir kalay kaplama ile kaplanır. ⓘ
Özel alaşımlar


Kalay diğer elementlerle birlikte çok çeşitli faydalı alaşımlar oluşturur. Kalay en yaygın olarak bakır ile alaşımlandırılır. Kalayın %85-99'u kalaydır; yatak metalinde de yüksek oranda kalay bulunur. Bronz çoğunlukla bakır ve %12 kalaydan oluşurken, fosfor ilavesiyle fosfor bronz elde edilir. Çan metali de %22 kalay içeren bir bakır-kalay alaşımıdır. Kalay bazen madeni paralarda kullanılmıştır; bir zamanlar Amerikan ve Kanada madeni paralarının tek haneli bir yüzdesini (genellikle yüzde beş veya daha az) oluşturmuştur. Bu tür paralarda bakır genellikle ana metal olduğundan, bazen çinko da dahil olmak üzere, bunlara bronz veya pirinç alaşımları denilebilir. ⓘ
Niyobyum-kalay bileşiği Nb3Sn, yüksek kritik sıcaklığı (18 K) ve kritik manyetik alanı (25 T) nedeniyle ticari olarak süper iletken mıknatıs bobinlerinde kullanılır. İki kilogram kadar küçük bir süper iletken mıknatıs, tonlarca ağırlığındaki geleneksel bir elektromıknatısın manyetik alanını üretebilir. ⓘ
Nükleer yakıtın kaplanması için zirkonyum alaşımlarına küçük bir oranda kalay eklenir. ⓘ
Bir boru orgundaki metal boruların çoğu, en yaygın bileşim olarak 50/50 olmak üzere kalay/kurşun alaşımından oluşur. Borudaki kalay oranı borunun tonunu belirler, çünkü kalay arzu edilen bir tonal rezonansa sahiptir. Bir kalay/kurşun alaşımı soğuduğunda, önce kurşun fazı katılaşır, ardından ötektik sıcaklığa ulaşıldığında, kalan sıvı parlak olan katmanlı kalay/kurşun ötektik yapısını oluşturur; kurşun fazı ile kontrast, benekli veya benekli bir etki yaratır. Bu metal alaşımı benekli metal olarak adlandırılır. Borular için kalay kullanmanın başlıca avantajları arasında görünümü, işlenebilirliği ve korozyona karşı direnci yer alır. ⓘ
Optoelektronik
İndiyum ve kalay oksitleri elektriksel olarak iletken ve şeffaftır ve sıvı kristal ekranlar gibi optoelektronik cihazlardaki uygulamalarla şeffaf elektriksel olarak iletken filmler yapmak için kullanılır. ⓘ
Diğer uygulamalar

Delikli teneke olarak da adlandırılan delikli teneke kaplama çelik, işlevsel ve dekoratif ev eşyaları yaratmak için Orta Avrupa'da ortaya çıkan bir zanaatkar tekniğidir. Dekoratif delme tasarımları, yerel geleneklere ve zanaatkâra bağlı olarak geniş bir çeşitlilik gösterir. Delikli teneke fenerler bu zanaatkar tekniğinin en yaygın uygulamasıdır. Delikli tasarımın içinden parlayan bir mumun ışığı, bulunduğu odada dekoratif bir ışık deseni yaratır. Fenerler ve diğer delikli teneke eşyalar Yeni Dünya'da ilk Avrupa yerleşimlerinden itibaren üretilmiştir. İyi bilinen bir örnek, adını Paul Revere'den alan Revere feneridir. ⓘ
Modern çağdan önce, Alpler'in bazı bölgelerinde bir keçi ya da koyun boynuzu keskinleştirilir ve alfabe ve birden dokuza kadar sayılar kullanılarak bir teneke panel delinirdi. Bu öğrenme aracı uygun bir şekilde "boynuz" olarak bilinirdi. Modern reprodüksiyonlar kalp ve lale gibi motiflerle süslenmiştir. ⓘ
Amerika'da, soğutmadan önceki günlerde pasta kasaları ve yiyecek kasaları kullanılıyordu. Bunlar, haşarat ve böcekleri caydırmak ve bozulabilir gıda maddelerinden tozu uzak tutmak için tasarlanmış çeşitli stil ve boyutlarda ahşap dolaplardı - ya yerde duran ya da asılı dolaplar. Bu dolapların kapaklarında ve bazen yanlarında, ev sahibi, marangoz ya da bir kalaycı tarafından, sinekleri dışarıda bırakırken hava sirkülasyonuna izin vermek için çeşitli tasarımlarda delinmiş teneke ekler vardı. Bu eşyaların modern reprodüksiyonları Kuzey Amerika'da popülerliğini korumaktadır. ⓘ
Pencere camı çoğunlukla erimiş camın erimiş kalay (float cam) üzerinde yüzdürülmesiyle yapılır, böylece düz ve kusursuz bir yüzey elde edilir. Buna "Pilkington işlemi" de denir. ⓘ
Kalay, gelişmiş Li-ion pillerde negatif elektrot olarak kullanılır. Uygulaması, bazı kalay yüzeylerinin Li-ion pillerde kullanılan karbonat bazlı elektrolitlerin ayrışmasını katalize etmesi nedeniyle biraz sınırlıdır. ⓘ
Kalay(II) florür, bazı diş bakım ürünlerine stannöz florür (SnF2) olarak eklenir. Kalay(II) florür kalsiyum aşındırıcılarla karıştırılabilirken, daha yaygın olan sodyum florür kalsiyum bileşiklerinin varlığında kademeli olarak biyolojik olarak inaktif hale gelir. Ayrıca diş eti iltihabını kontrol etmede sodyum florürden daha etkili olduğu gösterilmiştir. ⓘ
Kalay, aşırı ultraviyole litografi için ışık kaynağı görevi gören lazer kaynaklı plazmalar oluşturmak için bir hedef olarak kullanılır. ⓘ
Organotin bileşikleri
Organotin bileşikleri en yoğun şekilde kullanılmaktadır. Dünya çapında endüstriyel üretim muhtemelen 50.000 tonu aşmaktadır. ⓘ
PVC stabilizatörleri
Organotin bileşiklerinin başlıca ticari uygulaması PVC plastiklerin stabilizasyonudur. Bu tür stabilizatörlerin yokluğunda, PVC ısı, ışık ve atmosferik oksijen altında hızla bozunarak renksiz, kırılgan ürünlere neden olur. Kalay, aksi takdirde plastik malzemeden HCl'yi sıyıracak olan kararsız klorür iyonlarını (Cl-) temizler. Tipik kalay bileşikleri, dilaurat gibi dibütiltin diklorürün karboksilik asit türevleridir. ⓘ
Biyositler
Bazı organotin bileşikleri nispeten toksiktir ve hem avantajları hem de sorunları vardır. Biyosidal özellikleri nedeniyle fungisitler, pestisitler, yosun öldürücüler, ahşap koruyucular ve zehirli boya maddeleri olarak kullanılırlar. Tribütiltin oksit ahşap koruyucu olarak kullanılır. Tribütiltin ayrıca kağıt fabrikalarında balçık kontrolü ve sirkülasyon halindeki endüstriyel soğutma sularının dezenfeksiyonu gibi çeşitli endüstriyel amaçlar için de kullanılmaktadır. Tributiltin, gemilerde kirlenen organizmaların büyümesini önlemek için gemi boyasına katkı maddesi olarak kullanılmış, organotin bileşiklerinin bazı deniz organizmaları (örneğin köpek balinası) için yüksek toksisiteye sahip kalıcı organik kirleticiler olarak kabul edilmesinden sonra kullanımı azalmıştır. AB 2003 yılında organotin bileşiklerinin kullanımını yasaklarken, bu bileşiklerin deniz yaşamı üzerindeki toksisitesi ve bazı deniz türlerinin üreme ve büyümesine verdiği zararla ilgili endişeler (bazı raporlar litre başına 1 nanogram konsantrasyonda deniz yaşamı üzerindeki biyolojik etkileri tanımlamaktadır) Uluslararası Denizcilik Örgütü tarafından dünya çapında yasaklanmasına yol açmıştır. Birçok ülke artık organotin bileşiklerinin kullanımını 25 m'den (82 ft) uzun gemilerle sınırlandırmaktadır. Tributiltinin su ortamındaki kalıcılığı ekosistemin doğasına bağlıdır. Bu kalıcılık ve gemi boyasında katkı maddesi olarak kullanılması nedeniyle, donanma rıhtımlarının yakınında bulunan deniz çökeltilerinde yüksek konsantrasyonlarda tribütiltin bulunmuştur. Tribütiltin, bilinen en az 82 türü olan neograstropodlarda imposeks için bir biyobelirteç olarak kullanılmıştır. Denizcilik faaliyetleri nedeniyle yerel kıyı bölgelerinde yüksek TBT seviyeleri ile kabuklu deniz hayvanları olumsuz etkilenmiştir. Imposex, erkek cinsel özelliklerinin bir penis ve bir pallial vas deferens geliştirdikleri dişi örneklere empoze edilmesidir. Yüksek düzeyde TBT memeli endokrin bezlerine, üreme ve merkezi sinir sistemlerine, kemik yapısına ve gastrointestinal sisteme zarar verebilir. Tribütiltin memelileri etkilemekle kalmaz, su samurlarını, balinaları, yunusları ve insanları da etkiler. ⓘ
Organik kimya
Bazı kalay reaktifleri organik kimyada kullanışlıdır. En büyük uygulamada, stannöz klorür, nitro ve oksim gruplarının aminlere dönüştürülmesi için yaygın bir indirgeyici maddedir. Stille reaksiyonu, organotin bileşiklerini organik halojenürler veya psödohalojenürler ile birleştirir. ⓘ
Li-iyon piller
Kalay, lityum metali ile çeşitli metaller arası fazlar oluşturarak onu pil uygulamaları için potansiyel olarak çekici bir malzeme haline getirir. Lityum ile alaşım oluşturduktan sonra kalayın büyük hacimsel genleşmesi ve düşük elektrokimyasal potansiyellerde kalay-organik elektrolit arayüzünün kararsızlığı, ticari hücrelerde kullanımın önündeki en büyük zorluklardır. Bu sorun Sony tarafından kısmen çözülmüştür. Sony, 2000'li yılların sonunda piyasaya sürdüğü Nexelion hücrelerinde kobalt ve karbon ile kalay metaller arası bileşik kullanmıştır. Aktif malzemenin bileşimi yaklaşık olarak Sn0.3Co0.4C0.3'tür. Araştırmalar, tetragonal (beta) Sn'nin sadece bazı kristal yüzlerinin istenmeyen elektrokimyasal aktiviteden sorumlu olduğunu göstermiştir. ⓘ
Önlemler
Kalay metali, oksitleri ve tuzlarından kaynaklanan zehirlenme vakaları neredeyse bilinmemektedir. Öte yandan, bazı organotin bileşikleri neredeyse siyanür kadar toksiktir. ⓘ
İşyerinde kalaya maruz kalma soluma, cilt teması ve göz teması yoluyla gerçekleşebilir. ABD Mesleki Güvenlik ve Sağlık İdaresi (OSHA) işyerinde kalay maruziyeti için izin verilen maruziyet sınırını 8 saatlik bir iş günü boyunca 2 mg/m3 olarak belirlemiştir. Ulusal Mesleki Güvenlik ve Sağlık Enstitüsü (NIOSH) 8 saatlik bir iş gününde 2 mg/m3 tavsiye edilen maruz kalma sınırı (REL) belirlemiştir. 100 mg/m3 seviyelerinde, kalay yaşam ve sağlık için hemen tehlikelidir. ⓘ



