Sepsis
| Sepsis ⓘ | |
|---|---|
| Diğer isimler | Septisemi, septisemi, kan enfeksiyonu, kan zehirlenmesi |
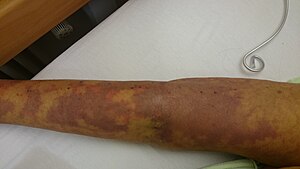 | |
| Sepsise bağlı ciltte lekelenme ve iltihaplanma | |
| Telaffuz |
|
| Uzmanlık | Bulaşıcı hastalık |
| Semptomlar |
|
| Komplikasyonlar |
|
| Olağan başlangıç | Hızlı (üç saatten az) veya uzun süreli (birkaç gün) olabilir |
| Nedenler | Bir enfeksiyon tarafından tetiklenen bağışıklık tepkisi |
| Risk faktörleri |
|
| Teşhis yöntemi | Sistemik inflamatuvar yanıt sendromu (SIRS), qSOFA |
| Önleme | grip aşısı, aşılar, zatürre aşısı |
| Tedavi | İntravenöz sıvılar, antimikrobiyaller, vazopressörler |
| Prognoz | 10 ila %80 ölüm riski; bu ölüm oranlarının (sepsis, ağır sepsis ve septik şok gibi bir spektrumdaki bir dizi durum içindir), organizma ve hastalığa, hastanın önceki sağlık durumuna ve tedavi yerinin ve personelinin yeteneklerine bağlı olarak agresif ve erken tedavi edilirse daha düşük olabileceğine dikkat etmek önemlidir |
| Frekans | Yılda 1000'de 0,2-3 (gelişmiş dünya) |
Eskiden septisemi (İngilizcede septicaemia) veya kan zehirlenmesi olarak bilinen sepsis, vücudun enfeksiyona verdiği yanıtın kendi doku ve organlarında hasara yol açmasıyla ortaya çıkan ve yaşamı tehdit eden bir durumdur. Bu ilk aşamayı bağışıklık sisteminin baskılanması takip eder. Yaygın belirti ve semptomlar arasında ateş, kalp atış hızında artış, solunum hızında artış ve kafa karışıklığı yer alır. Ayrıca zatürrede öksürük veya böbrek enfeksiyonunda ağrılı idrara çıkma gibi belirli bir enfeksiyonla ilgili semptomlar da olabilir. Çok genç, yaşlı ve bağışıklık sistemi zayıflamış kişilerde belirli bir enfeksiyon belirtisi olmayabilir ve ateş yerine vücut ısısı düşük veya normal olabilir. Şiddetli sepsis organ fonksiyonlarının veya kan akışının zayıflamasına neden olur. Düşük kan basıncı, yüksek kan laktatı veya düşük idrar çıkışı varlığı zayıf kan akışına işaret edebilir. Septik şok, sıvı replasmanından sonra düzelmeyen sepsise bağlı düşük kan basıncıdır. ⓘ
Sepsise bakteriler, virüsler ve mantarlar dahil olmak üzere birçok organizma neden olur. Birincil enfeksiyon için yaygın yerler arasında akciğerler, beyin, idrar yolu, deri ve karın organları bulunur. Risk faktörleri arasında çok genç veya yaşlı olmak, kanser veya diyabet gibi durumlar nedeniyle zayıflamış bir bağışıklık sistemi, büyük travma ve yanıklar yer alır. Önceden sepsis tanısı için enfeksiyon olduğu varsayılan bir ortamda en az iki sistemik inflamatuar yanıt sendromu (SIRS) kriterinin bulunması gerekiyordu. 2016 yılında, hızlı SOFA skoru (qSOFA) olarak bilinen kısaltılmış bir sıralı organ yetmezliği değerlendirme skoru (SOFA skoru), SIRS tanı sisteminin yerini almıştır. qSOFA sepsis kriterleri şu üç kriterden en az ikisini içerir: solunum hızında artış, bilinç düzeyinde değişiklik ve düşük kan basıncı. Sepsis kılavuzları antibiyotiklere başlamadan önce kan kültürü alınmasını önerir; ancak tanı için kanın enfekte olması gerekmez. Tıbbi görüntüleme, enfeksiyonun olası yerini ararken yardımcı olur. Benzer belirti ve semptomların diğer potansiyel nedenleri arasında anafilaksi, adrenal yetmezlik, düşük kan hacmi, kalp yetmezliği ve pulmoner emboli yer alır. ⓘ
Sepsis, intravenöz sıvılar ve antimikrobiyallerle acil tedavi gerektirir. Devam eden bakım genellikle bir yoğun bakım ünitesinde devam eder. Yeterli bir sıvı replasmanı denemesi kan basıncını korumak için yeterli olmazsa, kan basıncını yükselten ilaçların kullanımı gerekli hale gelir. Akciğerlerin ve böbreklerin işlevini desteklemek için sırasıyla mekanik ventilasyon ve diyaliz gerekebilir. Kan dolaşımına erişim ve tedaviyi yönlendirmek için bir santral venöz kateter ve bir arteriyel kateter yerleştirilebilir. Diğer yararlı ölçümler arasında kalp debisi ve superior vena kava oksijen satürasyonu yer alır. Sepsisli kişiler, diğer koşullar bu tür müdahaleleri engellemediği sürece derin ven trombozu, stres ülserleri ve basınç ülserleri için önleyici tedbirlere ihtiyaç duyar. Bazı kişiler insülin ile kan şekeri seviyelerinin sıkı kontrolünden fayda sağlayabilir. Kortikosteroidlerin kullanımı tartışmalıdır; bazı incelemelerde fayda görülürken bazılarında görülmemiştir. ⓘ
Hastalığın şiddeti kısmen sonucu belirler. Sepsisten ölüm riski %30 kadar yüksekken, ağır sepsis için bu risk %50'ye ve septik şok için %80'e kadar çıkmaktadır. Sepsis, 2017 yılında yaklaşık 49 milyon kişiyi etkilemiş ve 11 milyon ölüm gerçekleşmiştir (dünya genelinde her 5 ölümden 1'i). Gelişmiş dünyada, her 1000 kişide yaklaşık 0,2 ila 3 kişi sepsisten etkilenmektedir ve bu da Amerika Birleşik Devletleri'nde yılda yaklaşık bir milyon vakayla sonuçlanmaktadır. Hastalık oranları artmaktadır. Bazı veriler sepsisin erkekler arasında kadınlardan daha yaygın olduğunu gösterirken, diğer veriler hastalığın kadınlar arasında daha yaygın olduğunu göstermektedir. Sepsis tanımları Hipokrat zamanına kadar uzanmaktadır. ⓘ
Septisemi, (Kan zehirlenmesi) kana bakteri ya da toksin karışmasıdır. Septisemi birkaç yolla oluşabilir:
- Deri üstündeki bir yarada mikrop kapma sonucu enfeksiyon oluşması
- Bir apsenin patlayarak iltihabın kana karışması
- Boğaz enfeksiyonu (söz gelimi difteri)
- Bağırsak iltihabı (tifo gibi)
- Akciğer enfeksiyonu (zatürre gibi)
- İdraryolları enfeksiyonu sonucu ⓘ
Septisemi yerel değildir, kontrol altına alınmazsa bütün bedene yayılır. Septisemiye neden olan bakteri bedene çeşitli yollarla girebilir: söz gelimi diş çekiminden sonra, açık bir yara ya da iç organlardaki bir enfeksiyon yoluyla. Normal olarak akyuvarlar bakteriye karşı koyarlar ama bakteriler akyuvarların direnme gücünü aşacak kadar çoğalırlarsa septisemiyle bedene yayılırlar. Bu ya başka bir hastalık nedeniyle zayıf düşmüş bir bedende ya da sağlıklı bir kişide güçlü bir organizma tarafından oluşturulabilir. Septisemi belirtileri ateş, şok, ayakta duramayacak kadar halsizlikle birlikte kan basıncının ansızın düşmesidir. Hasta kendini çok kötü hisseder, komaya girer ve ölebilir. ⓘ
Bazen beden, enfeksiyona karşı koyabilmesine karşılık, enfeksiyona neden olan bakterinin salgıladığı toksinin (zehirli maddeler) kan dolaşımına karışmasını önleyemez. Bu da, kan zehirlenmesinin öteki türü olan toksemiyi ortaya çıkarır. ⓘ
İki tür toksin vardır: Biri bakteriler tarafından salınan ve asıl enfeksiyonun yanı sıra yan etkiler de yapan toksindir. Tetanosta görülen felç gibi kendine özgü belirtiler oluşturur. Öteki toksinler ise, doğal olarak bakteri hücrelerinin içinde bulunurlar ve bakterinin gerek akyuvarlar gerekse antibiyotik tarafından tahrip edilmesi sonucu kana karışırlar. Toksemi durumunda hasta kendini kötü hisseder ve ateşi yükselir. Genellikle antibiyotik aldıktan sonra ilacın iyi gelmediğini söyler, ama asıl neden ilacın kendi etkisinden çok, toksinlerin salınmasıdır. ⓘ
Bazı bakteriler derinin altındaki dokuyu tahrip ederek, bakterilerin derialtına yayılmasına neden olur. Bu durum sellülit diye adlandırılır ve enfeksiyon kapan bir yara ya da apsenin çevresinde ağrı veren bir kızarıklığın yayılması durumudur. ⓘ
Belirtiler ve semptomlar
Sepsisli kişilerde asıl nedene bağlı semptomlara ek olarak ateş, düşük vücut ısısı, hızlı nefes alma, hızlı kalp atış hızı, kafa karışıklığı ve ödem görülebilir. Erken belirtiler arasında hızlı kalp atış hızı, idrara çıkmada azalma ve yüksek kan şekeri yer alır. Yerleşik sepsis belirtileri arasında kafa karışıklığı, metabolik asidoz (solunum alkalozuna yol açan daha hızlı bir solunum hızı eşlik edebilir), sistemik vasküler direncin azalmasına bağlı düşük kan basıncı, daha yüksek kalp debisi ve organ yetmezliğine yol açabilecek kan pıhtılaşma bozuklukları yer alır. Ateş sepsiste en sık görülen belirtidir, ancak yaşlılar veya bağışıklık sistemi baskılanmış olanlar gibi bazı kişilerde ateş olmayabilir. ⓘ
Sepsiste görülen kan basıncındaki düşüş sersemliğe neden olabilir ve septik şok kriterlerinin bir parçasıdır. ⓘ
Septik şokta oksidatif stres gözlenir ve dolaşımdaki bakır ve C vitamini seviyeleri azalır. ⓘ
Neden
Sepsise yol açan enfeksiyonlar genellikle bakteriyeldir ancak mantar, parazit veya viral de olabilir. 1950'lerde antibiyotiklerin kullanılmaya başlanmasından önce sepsisin başlıca nedeni gram-pozitif bakterilerdi. Antibiyotiklerin kullanılmaya başlanmasından sonra, gram-negatif bakteriler 1960'lardan 1980'lere kadar sepsisin baskın nedeni olmuştur. 1980'lerden sonra, en yaygın olarak stafilokoklar olmak üzere gram-pozitif bakterilerin sepsis vakalarının %50'sinden fazlasına neden olduğu düşünülmektedir. Diğer yaygın bakteriler arasında Streptococcus pyogenes, Escherichia coli, Pseudomonas aeruginosa ve Klebsiella türleri yer almaktadır. Mantar sepsisi, şiddetli sepsis ve septik şok vakalarının yaklaşık %5'ini oluşturur; mantar sepsisinin en yaygın nedeni, hastanede sık görülen bir enfeksiyon olan Candida türü maya enfeksiyonudur. Parazitik sepsisin en yaygın nedenleri Plasmodium (sıtmaya yol açar), Schistosoma ve Echinococcus'tur. ⓘ
Şiddetli sepsisle sonuçlanan en yaygın enfeksiyon bölgeleri akciğerler, karın ve idrar yollarıdır. Tipik olarak, tüm sepsis vakalarının %50'si akciğerlerde bir enfeksiyon olarak başlar. Vakaların üçte biri ila yarısında enfeksiyonun kaynağı belirsizdir. ⓘ
Patofizyoloji
Sepsis, belirli istilacı patojen(ler) ve konağın bağışıklık sisteminin durumu ile ilgili faktörlerin bir kombinasyonundan kaynaklanır. Sepsisin aşırı inflamasyonla karakterize erken evresini (bazen sitokin fırtınasıyla sonuçlanan), bağışıklık sisteminin işlevinin azaldığı uzun bir dönem izleyebilir. Bu aşamaların her ikisi de ölümcül olabilir. Öte yandan, sistemik inflamatuar yanıt sendromu (SIRS) enfeksiyonun bulunmadığı kişilerde, örneğin yanık, politravma veya pankreatit ve kimyasal pnömonitte başlangıç durumunda ortaya çıkar. Bununla birlikte, sepsis de SIRS'a benzer yanıtlara neden olur. ⓘ
Mikrobiyal faktörler
Glikokaliks ve çeşitli adezinler gibi bakteriyel virülans faktörleri, kolonizasyona, bağışıklıktan kaçışa ve konakta hastalık oluşumuna izin verir. Gram-negatif bakterilerin neden olduğu sepsisin büyük ölçüde, endotoksin olarak da adlandırılan lipopolisakkaritin lipid A bileşenine karşı konakçı tarafından verilen bir yanıttan kaynaklandığı düşünülmektedir. Gram-pozitif bakterilerin neden olduğu sepsis, hücre duvarı lipoteikoik asidine karşı immünolojik bir yanıttan kaynaklanabilir. Süperantijen olarak hareket eden bakteriyel ekzotoksinler de sepsise neden olabilir. Süperantijenler, antijen sunumunun olmadığı durumlarda majör histokompatibilite kompleksi ve T-hücresi reseptörlerini eş zamanlı olarak bağlar. Bu zorunlu reseptör etkileşimi, T-hücreleri tarafından pro-inflamatuar kimyasal sinyallerin (sitokinler) üretimini indükler. ⓘ
Tipik septik enflamatuar kaskadına neden olabilecek bir dizi mikrobiyal faktör vardır. İstilacı bir patojen, patojenle ilişkili moleküler kalıpları (PAMP'ler) tarafından tanınır. PAMP örnekleri arasında gram-negatif bakterilerde lipopolisakkaritler ve flagellin, gram-pozitif bakteri hücre duvarının peptidoglikanında bulunan muramil dipeptit ve CpG bakteri DNA'sı yer alır. Bu PAMP'lar doğuştan gelen bağışıklık sisteminin membrana bağlı veya sitozolik olabilen örüntü tanıma reseptörleri (PRR'ler) tarafından tanınır. PRR'lerin dört ailesi vardır: toll benzeri reseptörler, C-tipi lektin reseptörleri, NOD benzeri reseptörler ve RIG-I benzeri reseptörler. Değişmez bir şekilde, bir PAMP ve bir PRR'nin birlikteliği bir dizi hücre içi sinyalizasyon kaskadına neden olacaktır. Sonuç olarak, nükleer faktör-kappa B ve aktivatör protein-1 gibi transkripsiyon faktörleri, pro-enflamatuar ve anti-enflamatuar sitokinlerin ekspresyonunu yukarı doğru düzenleyecektir. ⓘ
Konak faktörleri
Mikrobiyal antijenlerin tespit edilmesi üzerine, konakçı sistemik bağışıklık sistemi aktive olur. Bağışıklık hücreleri sadece patojenle ilişkili moleküler kalıpları değil aynı zamanda hasarlı dokulardan gelen hasarla ilişkili moleküler kalıpları da tanır. Daha sonra kontrolsüz bir bağışıklık tepkisi aktive olur çünkü lökositler spesifik enfeksiyon bölgesine değil, vücudun her yerine toplanır. Ardından, proinflamatuar T yardımcı hücre 1 (TH1), interlökin 10'un aracılık ettiği TH2'ye geçtiğinde, "telafi edici anti-inflamatuar yanıt sendromu" olarak bilinen bir immünosupresyon durumu ortaya çıkar. Lenfositlerin apoptozisi (hücre ölümü) immünosupresyonu daha da kötüleştirir. Nötrofiller, monositler, makrofajlar, dendritik hücreler, CD4+ T hücreleri ve B hücrelerinin tümü apoptoza uğrarken, düzenleyici T hücreleri apoptoza daha dirençlidir. Ardından, sitokrom c oksidazın inhibisyonu nedeniyle dokular oksijeni verimli bir şekilde kullanamadığından çoklu organ yetmezliği ortaya çıkar. ⓘ
Enflamatuar yanıtlar, aşağıda açıklanan çeşitli mekanizmalar yoluyla çoklu organ disfonksiyonu sendromuna neden olur. Akciğer damarlarının geçirgenliğinin artması alveollere sıvı sızmasına neden olarak akciğer ödemi ve akut solunum sıkıntısı sendromu (ARDS) ile sonuçlanır. Karaciğerde oksijen kullanımının bozulması safra tuzu taşınmasını bozarak sarılığa (ciltte sarımsı renk değişikliği) neden olur. Böbreklerde, yetersiz oksijenlenme tübüler epitel hücre hasarına (böbrek tübüllerini kaplayan hücrelerde) ve dolayısıyla akut böbrek hasarına (AKI) neden olur. Bu arada, kalpte, bozulmuş kalsiyum taşınması ve düşük adenozin trifosfat (ATP) üretimi, miyokardiyal depresyona neden olarak kalp kasılmasını azaltabilir ve kalp yetmezliğine neden olabilir. Gastrointestinal sistemde, mukozanın geçirgenliğinin artması mikroflorayı değiştirerek mukozal kanamaya ve paralitik ileusa neden olur. Merkezi sinir sisteminde, beyin hücrelerinin doğrudan hasar görmesi ve nörotransmisyonların bozulması zihinsel durumun değişmesine neden olur. Tümör nekroz faktörü, interlökin 1 ve interlökin 6 gibi sitokinler kan damarlarını kaplayan hücrelerdeki prokoagülasyon faktörlerini aktive ederek endotel hasarına yol açabilir. Hasarlı endotel yüzeyi antikoagülan özellikleri engellemenin yanı sıra antifibrinolizi artırarak damar içi pıhtılaşmaya, küçük kan damarlarında kan pıhtısı oluşumuna ve çoklu organ yetmezliğine yol açabilir. ⓘ
Sepsis hastalarında görülen düşük kan basıncı, nitrik oksit gibi kan damarlarını genişleten kimyasalların aşırı üretimi, vazopressin gibi kan damarlarını daraltan kimyasalların eksikliği ve ATP'ye duyarlı potasyum kanallarının aktivasyonu dahil olmak üzere çeşitli süreçlerin sonucudur. Şiddetli sepsis ve septik şoku olanlarda, bu olaylar dizisi distribütif şok olarak bilinen bir tür dolaşım şokuna yol açar. ⓘ
Teşhis
Sepsisin uygun şekilde yönetilebilmesi için erken teşhis gereklidir, zira hızlı tedavinin başlatılması ciddi sepsis kaynaklı ölümlerin azaltılmasında kilit rol oynamaktadır. Bazı hastaneler, potansiyel vakalara mümkün olduğunca erken dikkat çekmek için elektronik sağlık kayıtlarından oluşturulan uyarıları kullanmaktadır. ⓘ

Sepsis şüphesinin ilk üç saati içinde, tanısal çalışmalar beyaz kan hücresi sayımı, serum laktat ölçümü ve antibiyotiklere başlamadan önce, kullanımlarını 45 dakikadan fazla geciktirmediği sürece uygun kültürlerin alınmasını içermelidir. Etken organizma(lar)ı belirlemek için, aerobik ve anaerobik organizmalar için besiyeri içeren şişeler kullanılarak en az iki set kan kültürü gereklidir. En az bir tanesi ciltten ve bir tanesi de 48 saatten uzun süredir yerinde olan her damar erişim cihazından (IV kateter gibi) alınmalıdır. Bakteriler vakaların sadece yaklaşık %30'unda kanda bulunur. Bir başka olası tespit yöntemi de polimeraz zincir reaksiyonudur. Diğer enfeksiyon kaynaklarından şüpheleniliyorsa, antibiyotik kullanımını geciktirmediği sürece idrar, beyin omurilik sıvısı, yaralar veya solunum salgıları gibi bu kaynakların kültürleri de alınmalıdır. ⓘ
Altı saat içinde, 30 ml/kg'lık ilk sıvı resüsitasyonuna rağmen kan basıncı düşük kalırsa veya ilk laktat ≥ dört mmol/l (36 mg/dl) ise, santral venöz basınç ve santral venöz oksijen satürasyonu ölçülmelidir. İlk laktat yükselmişse laktat yeniden ölçülmelidir. Ancak normal ölçüm yöntemlerine kıyasla bakım noktasında laktat ölçümüne ilişkin kanıtlar zayıftır. ⓘ
On iki saat içinde, nekrotizan yumuşak doku enfeksiyonu, karın boşluğu astarında iltihaplanmaya neden olan bir enfeksiyon, safra kanalı enfeksiyonu veya bağırsak enfarktüsü gibi acil kaynak kontrolü gerektirecek herhangi bir enfeksiyon kaynağının teşhis edilmesi veya dışlanması esastır. Delinmiş bir iç organ (karın röntgeni veya BT taramasında serbest hava), pnömoni ile uyumlu anormal bir göğüs röntgeni (fokal opasifikasyon ile) veya peteşi, purpura veya purpura fulminans bir enfeksiyonun varlığına işaret edebilir. ⓘ
Tanımlar
| Bulma | Değer |
|---|---|
| Sıcaklık | <36 °C (96,8 °F) veya >38 °C (100,4 °F) |
| Kalp atış hızı | >90/dak |
| Solunum hızı | >20/dk veya PaCO2<32 mmHg (4,3 kPa) |
| WBC | <4x109/L (<4000/mm3), >12x109/L (>12.000/mm3) veya ≥%10 bantlar |

Daha önce sepsisi tanımlamak için SIRS kriterleri kullanılmaktaydı. SIRS kriterleri negatifse, kişide sepsis olma ihtimali çok düşüktür; pozitifse, kişide sepsis olma ihtimali orta düzeydedir. SIRS'e göre sepsisin farklı seviyeleri vardır: sepsis, ağır sepsis ve septik şok. SIRS'ın tanımı aşağıda gösterilmiştir:
- SIRS aşağıdakilerden iki veya daha fazlasının varlığıdır: anormal vücut ısısı, kalp atış hızı, solunum hızı veya kan gazı ve beyaz kan hücresi sayısı.
- Sepsis, enfeksiyöz bir sürece yanıt olarak SIRS olarak tanımlanır.
- Ağır sepsis, sepsise bağlı organ disfonksiyonu veya doku hipoperfüzyonu (hipotansiyon, yüksek laktat veya azalmış idrar çıkışı şeklinde kendini gösterir) ile birlikte görülen sepsis olarak tanımlanır. Şiddetli sepsis, çoklu organ disfonksiyon sendromu (MODS) ile ilişkili bir enfeksiyon hastalığı durumudur
- Septik şok, şiddetli sepsis ve intravenöz sıvı verilmesine rağmen devam eden düşük kan basıncıdır. ⓘ
2016 yılında, sistemik inflamatuar yanıt sendromu (SIRS) ile taramanın yerini sıralı organ yetmezliği değerlendirmesi (SOFA skoru) ve kısaltılmış versiyonunun (qSOFA) alması için yeni bir fikir birliğine varılmıştır. qSOFA skoru için üç kriter, dakikada 22 nefes veya daha fazla solunum hızı, 100 mmHg veya daha düşük sistolik kan basıncı ve değişmiş zihinsel durumu içerir. QSOFA kriterlerinden 2'si karşılandığında sepsisten şüphelenilir. SOFA skoru yoğun bakım ünitesinde (YBÜ) kullanılmak üzere tasarlanmıştır ve YBÜ'ye kabul edildikten sonra uygulanır ve her 48 saatte bir tekrarlanır; qSOFA ise YBÜ dışında kullanılabilir. qSOFA skorunun bazı avantajları hızlı bir şekilde uygulanabilmesi ve laboratuvar gerektirmemesidir. Ancak Amerikan Göğüs Hekimleri Koleji (CHEST), qSOFA ve SOFA kriterlerinin ciddi enfeksiyon tanısında gecikmeye yol açarak tedavinin gecikmesine neden olabileceğine dair endişelerini dile getirmiştir. SIRS kriterleri sepsisi tanımlamada çok hassas ve yeterince spesifik olmasa da, SOFA'nın da sınırlamaları vardır ve SIRS tanımının yerini alması amaçlanmamıştır. qSOFA'nın da, SIRS ile ölüm riski için makul derecede spesifik olmasına rağmen, tarama için muhtemelen daha iyi olmasına rağmen, zayıf duyarlı olduğu bulunmuştur. NOT - Surviving Sepsis Campaign 2021 Kılavuzları "sepsis veya septik şok için tek bir tarama aracı olarak SIRS, NEWS veya MEWS ile karşılaştırıldığında qSOFA'nın kullanılmamasını" önermektedir. ⓘ
Son organ disfonksiyonu
Son organ disfonksiyonu örnekleri aşağıdakileri içerir:
- Akciğerler: akut solunum sıkıntısı sendromu (ARDS) (PaO2/FiO2 oranı < 300), pediatrik akut solunum sıkıntısı sendromunda farklı oran
- Beyin: ajitasyon, konfüzyon, koma gibi ensefalopati semptomları; nedenleri arasında iskemi, kanama, küçük kan damarlarında kan pıhtısı oluşumu, mikroabse, multifokal nekrotizan lökoensefalopati yer alabilir
- Karaciğer: Protein sentezleme işlevinin bozulması, pıhtılaşma faktörlerinin sentezlenememesi nedeniyle kanın pıhtılaşmasında ilerleyici bozulma olarak akut bir şekilde ortaya çıkar ve metabolik işlevlerin bozulması bilirubin metabolizmasının bozulmasına yol açarak yüksek konjuge olmayan serum bilirubin seviyelerine neden olur
- Böbrek: düşük idrar çıkışı veya hiç idrar çıkışı olmaması, elektrolit anormallikleri veya aşırı hacim yüklenmesi
- Kalp: sistolik ve diyastolik kalp yetmezliği, muhtemelen miyosit fonksiyonunu baskılayan kimyasal sinyaller, hücresel hasar, troponin sızıntısı olarak kendini gösterir (doğası gereği iskemik olması gerekmese de) ⓘ
Pediatride SIRS için daha spesifik son organ disfonksiyonu tanımları mevcuttur.
- Kardiyovasküler disfonksiyon (en az 40 ml/kg kristalloid ile sıvı resüsitasyonundan sonra)
- Kan basıncının yaşa göre < 5. persentil veya sistolik kan basıncının yaşa göre normalin < 2 standart sapma altında olduğu hipotansiyon veya
- vazopressör gereksinimi veya
- aşağıdaki kriterlerden ikisi:
- baz açığı > 5 mEq/l olan açıklanamayan metabolik asidoz
- laktik asidoz: serum laktatı normalin üst sınırının 2 katı
- oligüri (idrar çıkışı < 0,5 ml/kg/saat)
- uzamış kılcal dolum > 5 saniye
- çekirdek ile çevresel sıcaklık farkı > 3 °C
- Solunum fonksiyon bozukluğu (siyanotik kalp defekti veya bilinen bir kronik solunum hastalığı yoksa)
- arteriyel kısmi oksijen basıncının solunan gazlardaki oksijen fraksiyonuna oranı (PaO2/FiO2) < 300 (akut akciğer hasarı tanımı) veya
- arteriyel kısmi karbondioksit basıncı (PaCO2), başlangıç PaCO2 değerinden > 65 torr (20 mmHg) fazla (hiperkapnik solunum yetmezliği kanıtı) veya
- Oksijen satürasyonunu ≥ %92 tutmak için FiO2 0,5'ten daha fazla ek oksijen gereksinimi
- Nörolojik işlev bozukluğu
- Glasgow Koma Skoru (GKS) ≤ 11 veya
- gelişimsel gecikmesi/zihinsel engeli olan bir kişide GKS'de 3 veya daha fazla puanlık düşüşle birlikte değişen zihinsel durum
- Hematolojik işlev bozukluğu
- trombosit sayısı < 80.000/mm3 veya kronik trombositopeniklerde maksimumdan %50 düşüş veya
- uluslararası normalleştirilmiş oran (INR) > 2
- Yaygın damar içi pıhtılaşma
- Böbrek fonksiyon bozukluğu
- serum kreatinin yaşa göre normalin üst sınırının ≥ 2 katı veya kronik böbrek hastalığı olan kişilerde bazal kreatinin değerinde 2 kat artış
- Karaciğer fonksiyon bozukluğu (yalnızca > 1 aylık bebekler için geçerlidir)
- total serum bilirubini ≥ 4 mg/dl veya
- alanin aminotransferaz (ALT) ≥ normalin üst sınırının 2 katı ⓘ
Bununla birlikte, konsensüs tanımları gelişmeye devam etmekte ve en sonuncusu klinik hasta başı deneyimini yansıtacak şekilde sepsis belirti ve semptomlarının listesini genişletmektedir. ⓘ
Biyobelirteçler
Biyobelirteçler sepsisin varlığına veya ciddiyetine işaret edebildikleri için tanıya yardımcı olabilirler, ancak sepsis yönetimindeki rolleri tam olarak tanımlanmamıştır. 2013 yılında yapılan bir incelemede, sepsisi SIRS'nin enfeksiyöz olmayan nedenlerinden ayırt etmek için bir yöntem olarak prokalsitonin düzeyinin kullanımını destekleyen orta kalitede kanıtlar olduğu sonucuna varılmıştır. Aynı derlemede testin duyarlılığı %77, özgüllüğü ise %79 olarak bulunmuştur. Yazarlar, prokalsitoninin sepsis için yararlı bir tanısal belirteç olarak hizmet edebileceğini öne sürmüş, ancak seviyesinin tek başına kesin tanı koydurmadığı konusunda uyarmıştır. 2012 yılında yapılan sistematik bir incelemede, çözünür ürokinaz tipi plazminojen aktivatör reseptörünün (SuPAR) spesifik olmayan bir enflamasyon belirteci olduğu ve sepsis tanısını doğru bir şekilde koymadığı tespit edilmiştir. Bununla birlikte, aynı derlemede SuPAR'ın prognostik değeri olduğu sonucuna varılmıştır, çünkü yüksek SuPAR seviyeleri sepsisli hastalarda artmış ölüm oranı ile ilişkilidir. Laktat seviyelerinin seri ölçümü (yaklaşık her 4 ila 6 saatte bir) tedaviyi yönlendirebilir ve sepsiste daha düşük mortalite ile ilişkilidir. ⓘ
Ayırıcı tanı
Sepsis için ayırıcı tanı geniştir ve SIRS'ın sistemik belirtilerine neden olabilecek enfeksiyöz olmayan durumları incelemek (dışlamak) gerekir: alkol yoksunluğu, akut pankreatit, yanıklar, pulmoner emboli, tirotoksikoz, anafilaksi, adrenal yetmezlik ve nörojenik şok. Hemofagositik lenfohistiositoz (HLH) gibi hiperinflamatuar sendromlar benzer semptomlara sahip olabilir ve ayırıcı tanıda yer alır. ⓘ
Yenidoğan sepsisi
Yaygın klinik kullanımda yenidoğan sepsisi, yaşamın ilk ayında menenjit, pnömoni, piyelonefrit veya gastroenterit gibi bakteriyel bir kan dolaşımı enfeksiyonunu ifade eder, ancak yenidoğan sepsisi mantar, virüs veya parazit enfeksiyonuna da bağlı olabilir. Hemodinamik bozulma veya solunum yetmezliği ile ilgili kriterler, müdahale için çok geç ortaya çıktıklarından yararlı değildir. ⓘ
Yönetim
Erken tanı ve odaklanmış yönetim, sepsis sonuçlarını iyileştirebilir. Mevcut profesyonel tavsiyeler, tanı konulduktan sonra mümkün olan en kısa sürede izlenmesi gereken bir dizi eylem ("paketler") içermektedir. İlk üç saat içinde, sepsisli bir kişi antibiyotik almalı ve düşük kan basıncı ya da organlara yetersiz kan gittiğine dair başka kanıtlar varsa (laktat seviyesinin yükselmesiyle kanıtlandığı gibi) intravenöz sıvılar verilmelidir; kan kültürleri de bu süre içinde alınmalıdır. Altı saat sonra kan basıncı yeterli olmalı, kan basıncı ve organlara giden kan akışı yakından izlenmeli ve başlangıçta yükselmişse laktat tekrar ölçülmelidir. İlgili bir paket olan "Sepsis Altılısı" Birleşik Krallık'ta yaygın olarak kullanılmaktadır; bu paket, fark edildikten sonraki bir saat içinde antibiyotik verilmesini, kan kültürü, laktat ve hemoglobin belirlenmesini, idrar çıkışının izlenmesini, yüksek akışlı oksijen ve intravenöz sıvı verilmesini gerektirmektedir. ⓘ
Sıvıların ve antibiyotiklerin zamanında verilmesinin yanı sıra, sepsis yönetimi enfekte sıvı koleksiyonlarının cerrahi drenajını ve organ disfonksiyonu için uygun desteği de içerir. Bu, böbrek yetmezliğinde hemodiyaliz, akciğer fonksiyon bozukluğunda mekanik ventilasyon, kan ürünlerinin transfüzyonu ve dolaşım yetmezliği için ilaç ve sıvı tedavisini içerebilir. Yeterli beslenmenin sağlanması (tercihen enteral beslenme, ancak gerekirse parenteral beslenme) uzun süreli hastalık sırasında önemlidir. Derin ven trombozu ve mide ülserini önlemeye yönelik ilaçlar da kullanılabilir. ⓘ
Antibiyotikler
Antibiyotiklerin başlatılmasını geciktirmeden iki set kan kültürü (aerobik ve anaerobik) önerilir. Solunum sekresyonları, idrar, yaralar, beyin omurilik sıvısı ve kateter takma yerleri (48 saatten fazla yerinde) gibi diğer bölgelerden alınan kültürler, bu bölgelerden kaynaklanan enfeksiyonlardan şüpheleniliyorsa önerilir. Ağır sepsis ve septik şokta, geniş spektrumlu antibiyotikler (genellikle iki, geniş kapsama alanına sahip bir β-laktam antibiyotik veya florokinolonlar, makrolidler veya aminoglikozidlerle kombine edilmiş geniş spektrumlu karbapenem) önerilir. Antibiyotik seçimi kişinin hayatta kalma süresini belirlemede önemlidir. Bazıları antibiyotiklerin tanı konulduktan sonraki bir saat içinde verilmesini önermekte ve antibiyotiklerin verilmesinde gecikilen her saat için ölüm oranında %6'lık bir artış olduğunu belirtmektedir. Diğerleri ise erken uygulamada bir fayda bulamamıştır. ⓘ
Başlangıç antibiyotik rejimi için en uygun seçimi çeşitli faktörler belirler. Bu faktörler arasında antibiyotiklere karşı bakteriyel duyarlılığın yerel modelleri, enfeksiyonun hastane veya toplum kaynaklı bir enfeksiyon olarak düşünülüp düşünülmediği ve hangi organ sistemlerinin enfekte olduğunun düşünüldüğü yer almaktadır. Antibiyotik rejimleri günlük olarak yeniden değerlendirilmeli ve uygunsa daraltılmalıdır. Tedavi süresi tipik olarak 7-10 gündür ve kullanılan antibiyotik türü kültür sonuçlarına göre belirlenir. Kültür sonucu negatifse, kişinin çoklu ilaç direnci olan organizmalarla enfekte olma olasılığını azaltmak için antibiyotikler kişinin klinik yanıtına göre azaltılmalı veya bir enfeksiyon yoksa tamamen kesilmelidir. Pseudomonas aeruginosa, Acinetobacter baumannii gibi çoklu ilaca dirençli organizmalarla enfekte olma riski yüksek olan kişilerde gram-negatif organizmaya özgü bir antibiyotiğin eklenmesi önerilir. Metisiline dirençli Staphylococcus aureus (MRSA) için vankomisin veya teikoplanin önerilir. Legionella enfeksiyonu için makrolid veya florokinolon ilavesi seçilir. Mantar enfeksiyonundan şüpheleniliyorsa, şiddetli sepsisi olan kişiler için kaspofungin veya mikafungin gibi bir ekinokandin, daha az hasta kişiler için triazol (flukonazol ve itrakonazol) seçilir. Sepsisten şüphelenilmediği sürece, akut pankreatit ve yanıklar gibi herhangi bir enfeksiyon kaynağı olmayan SIRS'li kişilerde uzun süreli antibiyotik profilaksisi önerilmemektedir. ⓘ
Günde bir kez aminoglikozid dozu, böbrek toksisitesi olmaksızın klinik yanıt için pik plazma konsantrasyonuna ulaşmak için yeterlidir. Bu arada, düşük hacim dağılımına sahip antibiyotikler için (vankomisin, teikoplanin, kolistin), enfeksiyonlarla savaşmak için yeterli bir terapötik seviyeye ulaşmak için bir yükleme dozu gereklidir. Beta-laktam antibiyotiklerin günlük toplam dozu aşmadan sık sık infüzyonu, antibiyotik seviyesini minimum inhibitör konsantrasyonun (MIC) üzerinde tutmaya yardımcı olacak ve böylece daha iyi bir klinik yanıt sağlayacaktır. Beta-laktam antibiyotiklerin sürekli olarak verilmesi, aralıklı olarak verilmesinden daha iyi olabilir. Terapötik ilaç izlemine erişim, yeterli ilaç terapötik seviyesini sağlamak ve aynı zamanda ilacın toksik seviyeye ulaşmasını önlemek için önemlidir. ⓘ
Bütün bakteri enfeksiyonlarında antibiyotikler kullanılır ve sonuç genellikle başarılı olur. Eğer septisemi kuşkusu varsa kandan örnek alınarak laboratuvarda kültür hazırlanmalı ve antibiyotiklere duyarlılık testi uygulanmalıdır. Tokseminin tedavisi daha güçtür. Bakteriler antibiyotiklerle öldürülebilir ama toksinlerin antitoksinlerle etkisiz hale getirilmesi gerekir. Tetanos, difteri ve bir toksemi olan yılan zehrine karşı antitoksinler vardır. Ancak hastanın tepkisi bilinemeyeceğinden büyük bir dikkatle kullanılmaları gerekir. Onun yerine, olabildiğince koruyucu önlem alınır ve bütün çocuklara ilk birkaç yıl içinde difteri ve tetanos aşısı yapılır. ⓘ
Septisemi bedenin savunma mekanizmasına büyük bir yük bindirebilir ve bazı kişiler bunun etkilerine ötekilerden daha açıktırlar: Şeker hastaları, alkolikler, uyuşturucu ve uyarıcı madde bağımlıları, kanser hastaları (özellikle ilaç tedavisi görenler), steroit ilaçlar kullananlar, yaşlılar ve direnci düşük olanlar. ⓘ
Toksemi, difteride kalbin zarar görmesi gibi, belirli zararlara yol açabilir. Ancak tıbbi tedaviyle sağlıklı bir kişinin bu tehlikeli dönemi atlatması olanaklıdır. Tetanos ise ender de olsa öldürücü olma özelliğini korumaktadır. ⓘ
İntravenöz sıvılar
Surviving Sepsis Campaign, yetişkinlerde ilk üç saatte 30 ml/kg sıvı verilmesini ve ardından kan basıncı, idrar çıkışı, solunum hızı ve oksijen satürasyonuna göre sıvı titrasyonu yapılmasını ve ortalama arter basıncının (MAP) 65 mmHg olmasını tavsiye etmiştir. Çocuklarda şok durumunda 20 ml/kg'lık bir başlangıç miktarı makuldür. Kan basınçlarını dinamik olarak ölçmek için santral venöz kateterin kullanıldığı ağır sepsis ve septik şok vakalarında, sıvılar santral venöz basınç 8-12 mmHg'ye ulaşana kadar verilmelidir. Bu hedeflere ulaşıldığında, santral venöz oksijen satürasyonu (ScvO2), yani venöz kanın kalbe dönerken vena kavada ölçülen oksijen satürasyonu optimize edilir. ScvO2 %70'in altındaysa, 10 g/dL hemoglobine ulaşmak için kan verilebilir ve ardından ScvO2 optimize edilene kadar inotroplar eklenir. Akut solunum sıkıntısı sendromu (ARDS) ve yeterli doku kan sıvısı olanlarda daha fazla sıvı dikkatli bir şekilde verilmelidir. ⓘ
Resüsitasyon için tercih edilen sıvı olarak kristalloid solüsyon önerilmektedir. Resüsitasyon için büyük miktarda kristalloid gerekiyorsa albümin kullanılabilir. Kristaloid solüsyonlar ölüm riski açısından hidroksietil nişasta ile çok az fark gösterir. Nişastalar ayrıca akut böbrek hasarı ve kan transfüzyonu ihtiyacında artış riski taşır. Çeşitli kolloid solüsyonların (modifiye jelatin gibi) kristalloidlere göre hiçbir avantajı yoktur. Albüminin de kristalloidlere göre bir faydası yok gibi görünmektedir. ⓘ
Kan ürünleri
Surviving Sepsis Campaign, miyokardiyal iskemi, hipoksemi veya akut kanama yoksa 70 g/L'nin altındaki hemoglobin seviyeleri için paketlenmiş kırmızı kan hücresi transfüzyonu önermektedir. 2014 yılında yapılan bir çalışmada, hedef hemoglobini 70 veya 90 g/L'nin üzerinde tutmak için yapılan kan transfüzyonları hayatta kalma oranlarında herhangi bir fark yaratmamıştır; bu arada, daha düşük transfüzyon eşiğine sahip olanlar toplamda daha az transfüzyon almıştır. Eritropoietin, kan pıhtılaşması olaylarını hızlandırabileceği için septik şokta anemi tedavisinde önerilmemektedir. Taze donmuş plazma transfüzyonu genellikle planlanan bir cerrahi işlem öncesinde altta yatan pıhtılaşma anormalliklerini düzeltmez. Bununla birlikte, kanama riski olmayan (10 × 109/L) veya yüksek kanama riski olan (20 × 109/L) veya aktif kanaması olan (50 × 109/L) altındaki trombosit sayılarında, planlanan bir ameliyat veya invaziv bir prosedürden önce trombosit transfüzyonu önerilir. IV immünoglobulin önerilmemektedir çünkü yararlı etkileri belirsizdir. Monoklonal ve poliklonal intravenöz immünoglobulin (IVIG) preparatları yenidoğanlarda ve sepsisli yetişkinlerde ölüm oranını azaltmamaktadır. IgM ile zenginleştirilmiş poliklonal IVIG preparatlarının kullanımına ilişkin kanıtlar tutarsızdır. Öte yandan, dissemine intravasküler koagülasyonu tedavi etmek için antitrombin kullanımı da yararlı değildir. Bu arada, enflamatuar aracıları ve bakteriyel toksinleri kandan uzaklaştırmak için kan saflaştırma tekniği (hemoperfüzyon, plazma filtrasyonu ve birleşik plazma filtrasyonu adsorpsiyonu gibi) de septik şok için herhangi bir sağkalım faydası göstermemektedir. ⓘ
Vazopressörler
Kişiye yeterince sıvı resüsitasyonu yapıldıysa ancak ortalama arter basıncı 65 mmHg'den yüksek değilse vazopressörler önerilir. Norepinefrin (noradrenalin) ilk seçenek olarak önerilmektedir. Septik şok sırasında vazopresör tedavisinin başlatılmasının geciktirilmesi mortalitenin artmasıyla ilişkilidir. ⓘ
Norepinefrin genellikle hipotansif septik şok için ilk basamak tedavi olarak kullanılır çünkü kanıtlar şok 24 ila 48 saat devam ettiğinde vazopressinin göreceli bir eksikliği olduğunu göstermektedir. Norepinefrin vazokonstriksiyon etkisiyle kan basıncını yükseltir, atım hacmi ve kalp hızı üzerinde çok az etkisi vardır. Bazı kişilerde ortalama arter basıncını artırmak için gereken vazopresör dozu toksik hale gelecek kadar yüksek olabilir. Gerekli vazopresör dozunu azaltmak için epinefrin eklenebilir. Epinefrin genellikle hipotansif şok için ilk basamak tedavi olarak kullanılmaz çünkü karın organlarına giden kan akışını azaltır ve laktat seviyelerini yükseltir. Vazopressin septik şokta kullanılabilir çünkü çalışmalar şok 24 ila 48 saat devam ettiğinde vazopressinde göreceli bir eksiklik olduğunu göstermiştir. Ancak vazopressin kalp, parmak/ayak parmakları ve karın organlarına giden kan akışını azaltarak bu dokulara oksijen gitmemesine neden olur. Dopamin tipik olarak önerilmez. Dopamin kalbin atım hacmini artırmak için faydalı olsa da, norepinefrinden daha fazla anormal kalp ritimlerine neden olur ve ayrıca bağışıklık sistemini baskılayıcı bir etkiye sahiptir. Dopaminin böbrekler üzerinde koruyucu özellikleri olduğu kanıtlanmamıştır. Dobutamin hipotansif septik şokta kalp debisini artırmak ve dokulara kan akışını düzeltmek için de kullanılabilir. Dobutamin, bağırsağa giden kan akışını azaltmayı da içeren ilişkili yan etkileri nedeniyle epinefrin kadar sık kullanılmaz. Ek olarak, dobutamin kalp hızını anormal şekilde artırarak kalp debisini artırır. ⓘ
Steroidler
Sepsiste steroid kullanımı tartışmalıdır. Çalışmalar, glukokortikoidlerin kullanılıp kullanılmayacağı ve ne zaman kullanılması gerektiği konusunda net bir tablo ortaya koymamaktadır. 2016 Surviving Sepsis Campaign, düşük doz hidrokortizonu yalnızca hem intravenöz sıvılar hem de vazopressörler septik şoku yeterince tedavi edemiyorsa önermektedir. 2021 Surviving Sepsis Campaign, devam eden vazopresör tedavisi gereksinimi olan septik şoklu yetişkinler için IV kortikosteroidleri önermektedir. 2019 yılında yapılan bir Cochrane incelemesi, 2019 yılında yapılan iki inceleme gibi düşük kaliteli fayda kanıtı bulmuştur. ⓘ
Kritik hastalık sırasında, adrenal yetmezlik ve kortikosteroidlere karşı doku direnci durumu ortaya çıkabilir. Bu durum kritik hastalıkla ilişkili kortikosteroid yetmezliği olarak adlandırılmıştır. Kortikosteroidlerle tedavi en çok septik şok ve erken şiddetli ARDS hastalarında faydalı olabilirken, pankreatit veya şiddetli pnömoni gibi diğer hastalarda rolü belirsizdir. Bununla birlikte, kortikosteroid yetersizliğini belirlemenin kesin yolu sorunlu olmaya devam etmektedir. Sıvılar ve vazopressörlerle resüsitasyona yetersiz yanıt verenlerde şüphelenilmelidir. Tanıyı doğrulamak için ne ACTH stimülasyon testi ne de rastgele kortizol seviyeleri önerilmektedir. Glukokortikoid ilaçların kesilme yöntemi değişkendir ve yavaşça azaltılmaları mı yoksa aniden kesilmeleri mi gerektiği belirsizdir. Bununla birlikte, 2016 Surviving Sepsis Campaign, vazopressörlere artık ihtiyaç duyulmadığında steroidlerin azaltılmasını önermektedir. ⓘ
Anestezi
Sepsis kaynaklı şiddetli ARDS nedeniyle ventilasyon gerektiren kişiler için 6 mL/kg öngörülen vücut ağırlığı (PBW) hedef tidal hacim ve 30 cm H2O'dan düşük plato basıncı önerilir. Yüksek pozitif ekspirasyon sonu basıncı (PEEP), oksijen değişimi için daha fazla akciğer ünitesini açtığı için sepsiste orta ila şiddetli ARDS için önerilir. Tahmini vücut ağırlığı cinsiyet ve boya göre hesaplanır ve bunun için araçlar mevcuttur. Transpulmoner basıncı kısa süreliğine yükselterek şiddetli ARDS için işe alım manevraları gerekli olabilir. Ventilasyonu iyileştirmek için mümkünse yatak başının yükseltilmesi önerilir. Bununla birlikte, β2 adrenerjik reseptör agonistleri ARDS tedavisinde önerilmez çünkü sağkalım oranlarını düşürebilir ve anormal kalp ritimlerini hızlandırabilir. Sürekli pozitif hava yolu basıncı (CPAP), T parçası veya inspiratuar basınç artırımı kullanılarak yapılan spontan solunum denemesi ventilasyon süresini azaltmada yardımcı olabilir. Aralıklı veya sürekli sedasyonun en aza indirilmesi mekanik ventilasyon süresinin azaltılmasında yardımcı olur. ⓘ
Genel anestezi, enfektif kaynağı çıkarmak için cerrahi prosedürler gerektiren sepsisli kişiler için önerilir. Genellikle inhalasyon ve intravenöz anestezikler kullanılır. Sepsiste anestezik gereksinimleri azalabilir. İnhalasyon anestezikleri proinflamatuar sitokinlerin seviyesini azaltabilir, lökosit adezyonunu ve proliferasyonunu değiştirebilir, muhtemelen mitokondriyal fonksiyon üzerinde toksik bir etki ile lenfositlerin apoptozunu (hücre ölümü) indükleyebilir. Etomidatın kardiyovasküler sistem üzerinde minimal bir etkisi olmasına rağmen, adrenal fonksiyonların zayıflamasına ve ölüm riskinin artmasına neden olabileceği endişesiyle bu durumda entübasyona yardımcı olacak bir ilaç olarak genellikle önerilmez. Bununla birlikte, mevcut az miktarda kanıt, etomidat ile ölüm riskinde bir değişiklik bulmamıştır. ⓘ
Artan kanıtlar mekanik ventilasyon, YBÜ ve hastanede kalış sürelerinin kısaldığına işaret ettiğinden, ARDS'nin olmadığı sepsis vakalarında paralitik ajanların kullanılması önerilmemektedir. Bununla birlikte, ARDS vakalarında paralitik kullanımı tartışmalı olmaya devam etmektedir. Uygun şekilde kullanıldığında paralitikler başarılı mekanik ventilasyona yardımcı olabilir, ancak kanıtlar şiddetli sepsiste mekanik ventilasyonun oksijen tüketimini ve iletimini iyileştirmediğini de göstermiştir. ⓘ
Kaynak kontrolü
Kaynak kontrolü, bir enfeksiyon odağını kontrol etmek ve mikroorganizma büyümesi veya konakçı savunma bozukluğu için elverişli koşulları azaltmak için fiziksel müdahaleleri ifade eder, örneğin bir apseden irin drenajı gibi. Latince "Ubi pus, ibi evacua" deyimine yol açan bu yöntem, enfeksiyonların kontrolüne yönelik en eski prosedürlerden biridir ve daha modern tedavilerin ortaya çıkmasına rağmen önemini korumaktadır. ⓘ
Erken dönem hedefe yönelik tedavi
Erken hedefe yönelik tedavi (EGDT), tanıdan sonraki ilk 6 saat boyunca şiddetli sepsisin yönetimine yönelik bir yaklaşımdır. Fizyolojik hedefi kardiyak ön yük, ard yük ve kontraktiliteyi optimize etmek olan adım adım ilerleyen bir yaklaşımdır. Erken antibiyotik verilmesini içerir. EGDT ayrıca hemodinamik parametrelerin izlenmesini ve 8-12 mmHg arasında bir santral venöz basınç, 65 ila 90 mmHg arasında bir ortalama arter basıncı, %70'in üzerinde bir santral venöz oksijen satürasyonu (ScvO2) ve 0,5 ml/kg/saatten daha yüksek bir idrar çıkışı gibi temel resüsitasyon hedeflerine ulaşmak için spesifik müdahaleleri içerir. Amaç, dokulara oksijen iletimini optimize etmek ve sistemik oksijen iletimi ile talebi arasında bir denge sağlamaktır. Serum laktatında uygun bir düşüş ScvO2'ye eşdeğer olabilir ve elde edilmesi daha kolaydır. ⓘ
Orijinal çalışmada, erken hedefe yönelik tedavinin sepsisli hastalarda mortaliteyi %46,5'ten %30,5'e düşürdüğü bulunmuştur ve Surviving Sepsis Campaign bunun kullanılmasını önermektedir. Bununla birlikte, daha yeni üç büyük randomize kontrol çalışması (ProCESS, ARISE ve ProMISe), ağır sepsiste standart tedaviye kıyasla erken hedefe yönelik tedavinin 90 günlük mortalite faydasını göstermemiştir. EGDT'nin bazı bölümlerinin diğerlerinden daha önemli olması muhtemeldir. Bu çalışmaların ardından EGDT'nin kullanımının hala makul olduğu düşünülmektedir. ⓘ
Yenidoğanlar
Yenidoğan sepsisini teşhis etmek zor olabilir çünkü yenidoğanlar asemptomatik olabilir. Bir yenidoğan sepsisi düşündüren belirti ve semptomlar gösterirse, antibiyotikler derhal başlatılır ve ya tanı testleriyle belirlenen belirli bir organizmayı hedef alacak şekilde değiştirilir ya da semptomlar için bulaşıcı bir neden ekarte edildikten sonra kesilir. Erken müdahaleye rağmen, septik şok gelişen çocukların %13'ünde ölüm meydana gelir ve bu risk kısmen diğer sağlık sorunlarına bağlıdır. Çoklu organ sistemi yetmezliği olmayan veya sadece bir inotropik ajana ihtiyaç duyanlarda mortalite düşüktür. ⓘ
Diğer
Septik şoktaki kişiler de dahil olmak üzere sepsiste ateşin tedavi edilmesi, 28 günlük bir süre boyunca mortalitede herhangi bir iyileşme ile ilişkilendirilmemiştir. Ateş tedavisi hala başka nedenlerle yapılmaktadır. ⓘ
2012 yılında yapılan bir Cochrane incelemesi, N-asetilsisteinin SIRS veya sepsis hastalarında mortaliteyi azaltmadığı ve hatta zararlı olabileceği sonucuna varmıştır. ⓘ
Rekombinant aktive protein C (drotrecogin alpha) ilk olarak ağır sepsis (yüksek APACHE II skoru ile tanımlanan) için kullanılmaya başlanmış ve sağkalım açısından fayda sağlayacağı düşünülmüştür. Ancak daha sonra yapılan çalışmalar advers olayları -özellikle kanama riskini- artırdığını ve mortaliteyi azaltmadığını göstermiştir. Bu ilaç 2011 yılında satıştan kaldırılmıştır. Eritoran olarak bilinen bir başka ilaç da fayda göstermemiştir. ⓘ
Kan şekeri yüksek olanlarda, 7,8-10 mmol/L'ye (140-180 mg/dL) düşürmek için insülin önerilir; daha düşük seviyeler potansiyel olarak sonuçları kötüleştirir. Kılcal kandan alınan glikoz seviyeleri dikkatle yorumlanmalıdır çünkü bu tür ölçümler doğru olmayabilir. Bir kişinin arteriyel kateteri varsa, kan şekeri testi için arteriyel kan önerilir. ⓘ
Eğer endike ise aralıklı veya sürekli renal replasman tedavisi kullanılabilir. Ancak, hipoperfüzyona bağlı laktik asidozu olan bir kişi için sodyum bikarbonat önerilmemektedir. Düşük molekül ağırlıklı heparin (LMWH), fraksiyone olmayan heparin (UFH) ve aralıklı pnömatik kompresyon cihazlarıyla mekanik profilaksi, orta ila yüksek venöz tromboembolizm riski olan sepsisli herhangi bir kişi için önerilir. Proton pompası inhibitörü (PPI) ve H2 antagonisti ile stres ülserinin önlenmesi, 48 saatten uzun süredir mekanik ventilasyonda olan, pıhtılaşma bozuklukları, karaciğer hastalığı ve renal replasman tedavisi gibi üst gastrointestinal kanama (ÜGIB) geliştirme risk faktörleri olan bir kişide yararlıdır. Kısmi veya tam enteral beslenmenin sağlanması (besinlerin bir beslenme tüpü aracılığıyla verilmesi), intravenöz beslenmeye kıyasla sepsisin ilk yedi gününde oral alım için kontrendike olan veya oral alımı tolere edemeyen bir kişinin beslenmesini sağlamak için en iyi yaklaşım olarak seçilmektedir. Bununla birlikte, omega-3 yağ asitleri sepsis veya septik şok geçiren bir kişi için bağışıklık takviyesi olarak önerilmemektedir. Septik olan ve enteral beslenmeyi tolere edemeyen kişiler için metoklopramid, domperidon ve eritromisin gibi prokinetik ajanların kullanımı önerilmektedir. Bununla birlikte, bu ajanlar QT aralığının uzamasını hızlandırabilir ve sonuç olarak torsades de pointes gibi bir ventriküler aritmiyi tetikleyebilir. Prokinetik ajanların kullanımı günlük olarak yeniden değerlendirilmeli ve artık endike değilse durdurulmalıdır. ⓘ
Prognoz
Sepsis, insanların yaklaşık %24,4'ünde, septik şok ise %34,7'sinde 30 gün içinde (%32,2 ve %38,5'inde 90 gün sonra) ölümcül olabilir. Laktat, prognozu belirlemede faydalı bir yöntemdir; 4 mmol/L'den yüksek bir seviyeye sahip olanların mortalitesi %40, 2 mmol/L'den düşük olanların mortalitesi ise %15'ten azdır. ⓘ
APACHE II ve Acil Servis Sepsisinde Mortalite gibi bir dizi prognostik tabakalandırma sistemi bulunmaktadır. APACHE II kişinin yaşını, altta yatan durumunu ve çeşitli fizyolojik değişkenleri hesaba katarak ağır sepsis nedeniyle ölme riskine ilişkin tahminlerde bulunur. Bireysel ortak değişkenler arasında, altta yatan hastalığın şiddeti ölüm riskini en güçlü şekilde etkilemektedir. Septik şok da kısa ve uzun vadeli mortalitenin güçlü bir öngörücüsüdür. Kültür-pozitif ve kültür-negatif ağır sepsis için vaka-ölüm oranları benzerdir. Acil Servis Sepsisinde Mortalite (MEDS) skoru acil servis ortamında daha basit ve kullanışlıdır. ⓘ
Bazı kişiler şiddetli sepsis atağını takiben uzun vadede ciddi bilişsel gerileme yaşayabilir, ancak sepsisli çoğu kişide başlangıç nöropsikolojik verilerinin olmaması, bunun insidansının ölçülmesini veya çalışılmasını zorlaştırmaktadır. ⓘ
Epidemiyoloji
Sepsis her yıl dünya çapında milyonlarca ölüme neden olmaktadır ve hastaneye kaldırılan kişilerde en yaygın ölüm nedenidir. Dünya genelinde yeni sepsis vakalarının sayısının yılda 18 milyon olduğu tahmin edilmektedir. Amerika Birleşik Devletleri'nde sepsis yaklaşık 1.000 kişiden 3'ünü etkilemekte ve şiddetli sepsis yılda 200.000'den fazla ölüme katkıda bulunmaktadır. ⓘ
Sepsis tüm hastaneye yatışların %1-2'sinde görülür ve yoğun bakım yatak kullanımının %25'inden sorumludur. Nadiren birincil tanı olarak bildirilmesi nedeniyle (genellikle kanser veya diğer hastalıkların bir komplikasyonu olarak), sepsis insidansı, mortalite ve morbidite oranları muhtemelen düşük tahmin edilmektedir. ABD eyaletlerinde yapılan bir çalışmada, 2010 yılında sepsis tanısıyla 100.000 nüfus başına yaklaşık 651 hastane yatışı tespit edilmiştir. Koroner olmayan yoğun bakım ünitelerinde (YBÜ) ölüm nedenleri arasında ikinci sırada, genel ölüm nedenleri arasında ise onuncu sırada yer almaktadır (ilk sırada kalp hastalığı gelmektedir). 12 aylıktan küçük çocuklar ve yaşlılar en yüksek şiddetli sepsis insidansına sahiptir. ABD'de 2010 yılında hastaneye birden fazla sepsis yatışı olan kişiler arasında, ilk hastaneye yatışın ardından vasıflı bir bakım tesisine veya uzun süreli bakıma taburcu edilenlerin, başka bir bakım türüne taburcu edilenlere kıyasla yeniden hastaneye yatırılma olasılığı daha yüksektir. ABD'nin 18 eyaletinde yapılan bir araştırmaya göre, 2011 yılında Medicare'i olan kişiler arasında sepsis, 30 gün içinde yeniden hastaneye yatışın en yaygın ikinci temel nedeni olmuştur. ⓘ
Çeşitli tıbbi durumlar bir kişinin enfeksiyona ve sepsis gelişimine yatkınlığını artırır. Yaygın sepsis risk faktörleri arasında yaş (özellikle çok genç ve yaşlılar); kanser, diyabet veya dalak yokluğu gibi bağışıklık sistemini zayıflatan durumlar ve büyük travma ve yanıklar yer almaktadır. ⓘ
1979'dan 2000'e kadar, Amerika Birleşik Devletleri Ulusal Hastane Taburcu Anketi'nden elde edilen veriler, sepsis insidansının dört kat artarak 100.000 nüfus başına 240 vakaya ulaştığını ve erkeklerde kadınlara kıyasla daha yüksek bir insidans olduğunu göstermiştir. Bununla birlikte, sepsisin küresel prevalansının kadınlarda daha yüksek olduğu tahmin edilmektedir. Aynı zaman diliminde, hastane içi vaka ölüm oranı %28'den %18'e düşürülmüştür. Bununla birlikte, Amerika Birleşik Devletleri'nden ülke çapında yatan hasta örneklemine göre, şiddetli sepsis insidansı 18 yaş üstü nüfus için 2003 yılında 10.000 nüfus başına 200'den 2007 yılında 300 vakaya yükselmiştir. İnsidans oranı, 100.000 nüfus başına 500 vaka ile özellikle bebekler arasında yüksektir. Sepsise bağlı ölüm oranı yaşla birlikte artmakta, 3 ila 5 yaş grubunda %10'dan az iken altıncı on yılda %60'a çıkmaktadır. Nüfusun yaş ortalamasındaki artışın yanı sıra kronik hastalıkları olan veya bağışıklık sistemini baskılayıcı ilaçlar kullanan daha fazla kişinin varlığı ve uygulanan invaziv prosedürlerin sayısındaki artış, sepsis oranının artmasına neden olmuştur. ⓘ
Tarihçe
"σήψις" (sepsis) terimi MÖ dördüncü yüzyılda Hipokrat tarafından ortaya atılmıştır ve organik maddenin çürüme veya ayrışma süreci anlamına gelmektedir. On birinci yüzyılda İbn-i Sina, şiddetli pürülan süreçle bağlantılı hastalıklar için "kan çürümesi" terimini kullanmıştır. Şiddetli sistemik toksisite halihazırda gözlemlenmiş olsa da, bu durum için spesifik bir terim olan sepsis ancak 19. yüzyılda kullanılmaya başlanmıştır. ⓘ
"Septisemi" olarak da yazılan "septisemi" ve "kan zehirlenmesi" terimleri kandaki mikroorganizmalara veya toksinlerine atıfta bulunuyordu. ABD'de 2013 yılına kadar kullanılan Hastalıkların ve İlgili Sağlık Sorunlarının Uluslararası İstatistiksel Sınıflandırması (ICD) versiyon 9, septisemi terimini "Streptokokal septisemi" gibi farklı tanılar için çok sayıda değiştirici ile birlikte kullanmıştır. Tüm bu tanılar ICD-10'da yine değiştiricilerle birlikte sepsise dönüştürülmüştür, örneğin "Streptokoklara bağlı sepsis" gibi. ⓘ
Mevcut terimler, mevcut olan mikroorganizmaya bağlıdır: kanda anormal seviyelerde bakteri mevcutsa ve neden olan sorun bakteriyemi, virüsler için viremi ve bir mantar için fungemi. ⓘ
19. yüzyılın sonunda, mikropların memeli konakçıya zarar verebilecek maddeler ürettiğine ve enfeksiyon sırasında salınan çözünebilir toksinlerin şiddetli enfeksiyonlar sırasında yaygın olan ateş ve şoka neden olduğuna yaygın olarak inanılıyordu. Pfeiffer, 20. yüzyılın başında Vibrio cholerae ile ilişkili pirojenik prensibi belirtmek için endotoksin terimini ortaya attı. Kısa süre sonra endotoksinlerin çoğu ve belki de tüm gram-negatif bakteriler tarafından ifade edildiği anlaşılmıştır. Enterik endotoksinlerin lipopolisakkarit karakteri 1944 yılında Shear tarafından aydınlatılmıştır. Bu maddenin moleküler karakteri 1973 yılında Luderitz ve arkadaşları tarafından belirlenmiştir. ⓘ
1965'te bir C3H/HeJ fare türünün endotoksinle indüklenen şoka karşı bağışık olduğu keşfedilmiştir. Bu etki için genetik lokus Lps olarak adlandırıldı. Bu farelerin aynı zamanda gram-negatif bakterilerle enfeksiyona karşı aşırı duyarlı olduğu bulunmuştur. Bu gözlemler nihayet 1998 yılında toll benzeri reseptör geni 4'ün (TLR 4) keşfedilmesiyle birbirine bağlandı. Beş yıllık bir süre içinde gerçekleştirilen genetik haritalama çalışması, TLR4'ün Lps kritik bölgesindeki tek aday lokus olduğunu gösterdi; bu da TLR4 içindeki bir mutasyonun lipopolisakkarit direnci fenotipini açıklaması gerektiğini kuvvetle ima etti. Endotoksine dirençli fenotipe yol açan TLR4 genindeki bozukluğun sitoplazmadaki bir mutasyondan kaynaklandığı keşfedilmiştir. ⓘ
Bilim camiasında sepsis araştırmalarında fare modellerinin kullanımına ilişkin tartışmalar 2013 yılında bilim insanlarının fare bağışıklık sistemi ile insan bağışıklık sistemini karşılaştıran ve sistem düzeyinde ikisinin çok farklı çalıştığını gösteren bir inceleme yayınlamasıyla başladı; yazarlar makalelerinin yayınlandığı tarih itibariyle insanlarda 150'den fazla klinik sepsis denemesi yapıldığını, bunların neredeyse tamamının farelerdeki umut verici verilerle desteklendiğini ve hepsinin başarısız olduğunu belirttiler. Yazarlar, sepsis araştırmalarında fare modellerinin kullanımından vazgeçilmesi çağrısında bulunmuştur; diğerleri bunu reddetmiş ancak fare çalışmalarının sonuçlarının yorumlanmasında daha dikkatli olunması ve klinik öncesi çalışmaların daha dikkatli tasarlanması çağrısında bulunmuştur. Yaklaşımlardan biri, biyobelirteçleri ve müdahale için ilaç hedeflerini belirlemeye çalışmak için sepsis geçirmiş kişilerden alınan biyopsi ve klinik verileri incelemeye daha fazla güvenmektir. ⓘ
Toplum ve kültür
Ekonomi
Sepsis, 2013 yılında yaklaşık 1,3 milyon hastane yatışı için toplam 23,6 milyar dolar maliyetle Amerika Birleşik Devletleri'nde hastane yatışlarında tedavi edilen en pahalı durum olmuştur. Sepsis hastanede yatış maliyetleri 1997'den bu yana yıllık yüzde 11,5'lik bir artışla dört kattan fazla artmıştır. Ödeyenlere göre, Medicare ve sigortasızlara fatura edilen en maliyetli durum, Medicaid'e fatura edilen ikinci en maliyetli durum ve özel sigortaya fatura edilen dördüncü en maliyetli durum olmuştur. ⓘ
Eğitim
İnsanları sepsis konusunda eğitmek ve sepsis sonuçlarını iyileştirmek amacıyla 2002 yılında "Surviving Sepsis Campaign" adlı büyük bir uluslararası işbirliği kurulmuştur. Kampanya, sonraki yıllarda eksiksiz bir kılavuz seti yayınlamak amacıyla, şiddetli sepsis için yönetim stratejilerinin kanıta dayalı bir incelemesini yayınlamıştır. Kılavuzlar 2016'da ve 2021'de tekrar güncellenmiştir. ⓘ
Sepsis Alliance, hem genel halk hem de sağlık çalışanları arasında sepsis farkındalığını artırmak için oluşturulmuş bir hayır kurumudur. ⓘ
Araştırma

Bazı yazarlar, mikrobiyomun normalde mutualist (veya nötr) üyeleri tarafından sepsisin başlatılmasının her zaman kötüleşen konakçı bağışıklık sisteminin tesadüfi bir yan etkisi olmayabileceğini öne sürmektedir. Bunun yerine, genellikle konağın hayatta kalma şansındaki ani düşüşe karşı uyarlanabilir bir mikrobiyal yanıttır. Bu senaryoya göre, sepsise neden olan mikrop türleri, gelecekteki kadavrayı tekellerine almaktan, biyokütlesini ayrıştırıcı olarak kullanmaktan ve daha sonra yeni bireylerle mutualistik ilişkiler kurmak için toprak veya su yoluyla bulaşmaktan fayda sağlar. Streptococcus pneumoniae, Escherichia coli, Proteus spp., Pseudomonas aeruginosa, Staphylococcus aureus, Klebsiella spp., Clostridium spp., Lactobacillus spp., Bacteroides spp. bakterileri ve Candida spp. mantarları bu tür yüksek düzeyde fenotipik plastisite yeteneğine sahiptir. Açıkça görülüyor ki, tüm sepsis vakaları bu tür adaptif mikrobiyal strateji değişimleri yoluyla ortaya çıkmıyor. ⓘ
Paul E. Marik'in "HAT" protokolü olarak da bilinen "Marik protokolü", yoğun bakımdaki kişilerde sepsisi önlemeye yönelik bir tedavi olarak hidrokortizon, C vitamini ve tiamin kombinasyonunu önermiştir. Marik'in 2017'de yayınlanan ilk araştırması, dramatik bir fayda kanıtı göstererek protokolün yoğun bakım doktorları arasında popüler hale gelmesine yol açmış, özellikle de protokolün sosyal medyada ve Ulusal Halk Radyosu'nda ilgi görmesinin ardından, daha geniş tıp camiasından basın toplantısı yoluyla bilime yönelik eleştirilere yol açmıştır. Daha sonra yapılan bağımsız araştırmalar, Marik'in olumlu sonuçlarını tekrarlayamadı ve bu da önyargı nedeniyle tehlikeye atılmış olma ihtimalini gösterdi. 2021'deki denemelerin sistematik bir incelemesi, protokolün iddia edilen faydalarının doğrulanamadığını ortaya koydu. Daha yakın tarihli bir başka inceleme ise "HAT tedavisinin vazopressör kullanım süresini önemli ölçüde azalttığını ve SOFA skorunu iyileştirdiğini ancak sepsisli hastalar için diğer sonuçlarda önemli faydalar sağlamadığını" ortaya koymuştur. ⓘ
Genel olarak, 2021 itibariyle sepsis tedavisinde C vitamininin herhangi bir rolü olduğuna dair kanıtlar belirsizliğini korumaktadır. ⓘ
