Neon
 | |||||||||||||||||||||
| Neon | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Görünüş | Bir elektrik alanına yerleştirildiğinde turuncu-kırmızı bir parıltı sergileyen renksiz gaz | ||||||||||||||||||||
| Standart atom ağırlığı Ar°(Ne) |
| ||||||||||||||||||||
| Periyodik tabloda neon | |||||||||||||||||||||
| |||||||||||||||||||||
| Atom numarası (Z) | 10 | ||||||||||||||||||||
| Grup | grup 18 (asal gazlar) | ||||||||||||||||||||
| Dönem | dönem 2 | ||||||||||||||||||||
| Blok | p-blok | ||||||||||||||||||||
| Elektron konfigürasyonu | [[[Helyum|He]]] 2s2 2p6 | ||||||||||||||||||||
| Kabuk başına elektron | 2, 8 | ||||||||||||||||||||
| Fiziksel özellikler | |||||||||||||||||||||
| STP'de Faz | gaz | ||||||||||||||||||||
| Erime noktası | 24,56 K (-248,59 °C, -415,46 °F) | ||||||||||||||||||||
| Kaynama noktası | 27.104 K (-246.046 °C, -410.883 °F) | ||||||||||||||||||||
| Yoğunluk (STP'de) | 0,9002 g/L | ||||||||||||||||||||
| sıvı olduğunda (b.p.'de) | 1.207 g/cm3 | ||||||||||||||||||||
| Üçlü nokta | 24.556 K, 43.37 kPa | ||||||||||||||||||||
| Kritik nokta | 44,4918 K, 2,7686 MPa | ||||||||||||||||||||
| Füzyon ısısı | 0,335 kJ/mol | ||||||||||||||||||||
| Buharlaşma ısısı | 1,71 kJ/mol | ||||||||||||||||||||
| Molar ısı kapasitesi | 20,79 J/(mol-K) | ||||||||||||||||||||
Buhar basıncı
| |||||||||||||||||||||
| Atomik özellikler | |||||||||||||||||||||
| Oksidasyon durumları | 0 | ||||||||||||||||||||
| İyonlaşma enerjileri |
| ||||||||||||||||||||
| Kovalent yarıçap | 58 pm | ||||||||||||||||||||
| Van der Waals yarıçapı | 154 pm | ||||||||||||||||||||
| Neonun spektral çizgileri | |||||||||||||||||||||
| Diğer özellikler | |||||||||||||||||||||
| Doğal oluşum | ilkel | ||||||||||||||||||||
| Kristal yapı | yüz merkezli kübik (fcc) | ||||||||||||||||||||
| Ses hızı | 435 m/s (gaz, 0 °C'de) | ||||||||||||||||||||
| Termal iletkenlik | 49,1×10-3 W/(m⋅K) | ||||||||||||||||||||
| Manyetik sıralama | diamanyetik | ||||||||||||||||||||
| Molar manyetik duyarlılık | -6,74×10-6 cm3/mol (298 K) | ||||||||||||||||||||
| Yığın modülü | 654 GPa | ||||||||||||||||||||
| CAS Numarası | 7440-01-9 | ||||||||||||||||||||
| Tarih | |||||||||||||||||||||
| Tahmin | William Ramsay (1897) | ||||||||||||||||||||
| Keşif ve ilk izolasyon | William Ramsay & Morris Travers (1898) | ||||||||||||||||||||
| Neonun ana izotopları | |||||||||||||||||||||
| |||||||||||||||||||||
Neon, sembolü Ne ve atom numarası 10 olan kimyasal bir elementtir. Asal bir gazdır. Neon, standart koşullar altında renksiz, kokusuz, inert monatomik bir gazdır ve yoğunluğu havanın yaklaşık üçte ikisidir. Azot, oksijen, argon ve karbondioksit çıkarıldıktan sonra kuru havada kalan üç nadir asal elementten biri olarak 1898 yılında (kripton ve ksenon ile birlikte) keşfedilmiştir. Neon, keşfedilen bu üç nadir gazdan ikincisiydi ve parlak kırmızı emisyon spektrumundan hemen yeni bir element olarak tanındı. Neon ismi Yunanca νέος (neos) kelimesinin nötr tekil hali olan ve 'yeni' anlamına gelen νέον kelimesinden türetilmiştir. Neon kimyasal olarak inerttir ve yüksüz neon bileşikleri bilinmemektedir. Şu anda bilinen neon bileşikleri arasında iyonik moleküller, van der Waals kuvvetleri ile bir arada tutulan moleküller ve klatratlar bulunmaktadır. ⓘ
Elementlerin kozmik nükleojenezi sırasında, yıldızlardaki alfa yakalama füzyon sürecinden büyük miktarlarda neon oluşur. Neon evrende ve güneş sisteminde çok yaygın bir element olmasına rağmen (hidrojen, helyum, oksijen ve karbondan sonra kozmik bollukta beşinci sırada yer alır), Dünya'da nadir bulunur. Hacim olarak havanın yaklaşık 18,2 ppm'ini (bu yaklaşık olarak moleküler veya mol fraksiyonu ile aynıdır) ve Dünya'nın kabuğunda daha küçük bir fraksiyonu oluşturur. Neonun Dünya'da ve iç (karasal) gezegenlerde göreceli olarak az bulunmasının nedeni, neonun oldukça uçucu olması ve katı maddelere sabitlenmesi için hiçbir bileşik oluşturmamasıdır. Sonuç olarak, Güneş Sistemi'nin ilk zamanlarında yeni tutuşmuş Güneş'in sıcaklığı altında gezegenimsi maddelerden kaçmıştır. Jüpiter'in dış atmosferi bile, farklı bir nedenden dolayı olsa da, neondan bir şekilde tükenmiştir. ⓘ
Neon, düşük voltajlı neon kızdırma lambalarında, yüksek voltajlı deşarj tüplerinde ve neon reklam tabelalarında kullanıldığında belirgin bir kırmızımsı-turuncu parıltı verir. Neondan gelen kırmızı emisyon hattı aynı zamanda helyum-neon lazerlerin iyi bilinen kırmızı ışığına da neden olur. Neon bazı plazma tüpü ve soğutucu uygulamalarında kullanılır, ancak çok az ticari kullanımı vardır. Ticari olarak sıvı havanın fraksiyonel damıtılmasıyla elde edilir. Tek kaynak hava olduğu için helyumdan çok daha pahalıdır. ⓘ


Neon (Ne), periyodik tablonun 8-A grubunda yer alan soy gazdır. ⓘ
Neon 1898 yılında William Ramsay ve Morris Travers tarafından keşfedilmiştir. ⓘ
| Element veya periyodik tablo ile ilgili bu madde taslak seviyesindedir. Madde içeriğini genişleterek Vikipedi'ye katkı sağlayabilirsiniz. ⓘ |
Tarih

Neon 1898 yılında İngiliz kimyagerler Sir William Ramsay (1852-1916) ve Morris Travers (1872-1961) tarafından Londra'da keşfedilmiştir. Neon, Ramsay'in bir hava örneğini sıvı hale gelene kadar soğutması, ardından sıvıyı ısıtması ve gazları kaynarken yakalamasıyla keşfedildi. Azot, oksijen ve argon gazları tanımlanmıştı, ancak geri kalan gazlar Mayıs 1898'in sonunda başlayan altı haftalık bir süre içinde kabaca bolluk sırasına göre izole edildi. İlk tanımlanan kripton oldu. Kriptonun çıkarılmasının ardından, spektroskopik deşarj altında parlak kırmızı ışık veren bir gaz geldi. Haziran ayında tanımlanan bu gaza, Ramsay'in oğlu tarafından önerilen Latince novum ('yeni') kelimesinin Yunanca karşılığı olan "neon" adı verildi. Gaz halindeki neonun elektriksel olarak uyarıldığında yaydığı karakteristik parlak kırmızı-turuncu renk hemen fark edildi. Travers daha sonra şöyle yazmıştır: "Tüpten çıkan kıpkırmızı ışık kendi hikayesini anlatıyordu ve üzerinde durulması ve asla unutulmaması gereken bir manzaraydı." ⓘ
Neonla birlikte, argonla yaklaşık aynı yoğunlukta ancak farklı bir spektruma sahip ikinci bir gaz da rapor edildi - Ramsay ve Travers buna metargon adını verdi. Ancak daha sonra yapılan spektroskopik analizler bunun karbon monoksitle kirlenmiş argon olduğunu ortaya çıkardı. Son olarak, aynı ekip Eylül 1898'de aynı süreçle ksenonu keşfetti. ⓘ
Neon'un kıtlığı, azot kullanan ve 1900'lerin başında ticarileştirilen Moore tüpleri doğrultusunda aydınlatma için hızlı bir şekilde uygulanmasını engelledi. 1902'den sonra Georges Claude'un şirketi Air Liquide, hava sıvılaştırma işinin bir yan ürünü olarak endüstriyel miktarlarda neon üretti. Aralık 1910'da Claude, kapalı bir neon tüpüne dayanan modern neon aydınlatmasını gösterdi. Claude, yoğunluğu nedeniyle kısa bir süre iç mekan aydınlatması için neon tüpleri satmayı denedi, ancak ev sahipleri renge itiraz ettiği için pazar başarısız oldu. 1912 yılında Claude'un ortağı göz alıcı reklam tabelaları olarak neon deşarj tüpleri satmaya başladı ve anında daha başarılı oldu. Neon tüpler 1923 yılında Los Angeles Packard otomobil bayisi tarafından satın alınan iki büyük neon tabela ile ABD'ye tanıtıldı. Parıltısı ve dikkat çekici kırmızı rengi neon reklamcılığını rakiplerinden tamamen farklı kıldı. Neonun yoğun rengi ve canlılığı o dönemdeki Amerikan toplumuna denk düşüyor, "ilerleme yüzyılı "nı çağrıştırıyor ve şehirleri ışıldayan reklamlar ve "elektro-grafik mimari" ile dolu sansasyonel yeni ortamlara dönüştürüyordu. ⓘ
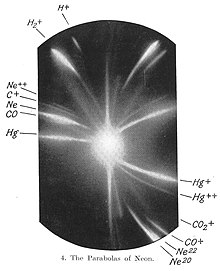
Neon, 1913 yılında J. J. Thomson'un kanal ışınlarının bileşimine yönelik araştırmasının bir parçası olarak neon iyonlarını bir manyetik ve bir elektrik alanından geçirip bir fotoğraf plakasıyla akımların sapmasını ölçmesiyle atomların doğasının temel olarak anlaşılmasında rol oynamıştır. Thomson fotoğraf plakası üzerinde iki ayrı ışık lekesi gözlemledi (resme bakın), bu da iki farklı sapma parabolü olduğunu gösteriyordu. Thomson sonunda neon gazındaki bazı atomların diğerlerinden daha yüksek kütleli olduğu sonucuna vardı. O zamanlar Thomson tarafından anlaşılmamış olsa da bu, kararlı atomların izotoplarının ilk keşfiydi. Thomson'ın cihazı, bugün kütle spektrometresi olarak adlandırdığımız aletin ilkel bir versiyonuydu. ⓘ
İzotoplar
Neon en hafif ikinci soy gazdır. Neonun üç kararlı izotopu vardır: 20Ne (%90,48), 21Ne (%0,27) ve 22Ne (%9,25). 21Ne ve 22Ne kısmen primordial ve kısmen nükleojeniktir (yani diğer nüklitlerin nötronlarla veya ortamdaki diğer parçacıklarla nükleer reaksiyonları sonucu oluşur) ve doğal bolluktaki değişimleri iyi anlaşılmıştır. Buna karşılık, 20Ne'nin (yıldız nükleosentezinde oluşan başlıca ilkel izotop) nükleojenik veya radyojenik olduğu bilinmemektedir. Bu nedenle Dünya'daki 20Ne değişiminin nedenleri hararetle tartışılmaktadır. ⓘ
Nükleojenik neon izotoplarını üreten başlıca nükleer reaksiyonlar, nötron yakalama ve hemen bir alfa parçacığı emisyonundan sonra sırasıyla 21Ne ve 22Ne üreten 24Mg ve 25Mg'den başlar. Bu reaksiyonları üreten nötronlar çoğunlukla uranyum serisi bozunma zincirlerinden türetilen alfa parçacıklarından ikincil parçalanma reaksiyonları ile üretilir. Net sonuç, granitler gibi uranyum açısından zengin kayaçlarda gözlemlenen daha düşük 20Ne/22Ne ve daha yüksek 21Ne/22Ne oranlarına doğru bir eğilim ortaya çıkarır. 21Ne, 20Ne çeşitli doğal karasal nötron kaynaklarından bir nötron emdiğinde nükleojenik bir reaksiyonda da üretilebilir. ⓘ
Buna ek olarak, maruz kalmış karasal kayaların izotopik analizi, 21Ne'nin kozmojenik (kozmik ışın) üretimini göstermiştir. Bu izotop magnezyum, sodyum, silikon ve alüminyum üzerindeki spallasyon reaksiyonları ile üretilir. Her üç izotop da analiz edilerek kozmojenik bileşen magmatik neon ve nükleojenik neondan ayrıştırılabilir. Bu, neonun yüzey kayaları ve meteoritlerin kozmik maruziyet yaşlarının belirlenmesinde yararlı bir araç olacağını göstermektedir. ⓘ
Ksenona benzer şekilde, volkanik gaz örneklerinde gözlemlenen neon içeriği, 22Ne içeriğine göre 20Ne ve nükleojenik 21Ne bakımından zenginleşmiştir. Manto kaynaklı bu örneklerin neon izotopik içeriği atmosferik olmayan bir neon kaynağını temsil etmektedir. 20Ne ile zenginleştirilmiş bileşenler, muhtemelen güneş neonunu temsil eden, Dünya'daki egzotik ilkel nadir gaz bileşenlerine atfedilmektedir. Elmaslarda yüksek 20Ne bolluğu bulunur ve bu da Dünya'da bir güneş neon rezervuarı olduğunu düşündürür. ⓘ
Özellikler
Neon, helyumdan sonra en hafif ikinci soy gazdır. Vakum deşarj tüpünde kırmızımsı-turuncu renkte parlar. Ayrıca neon, herhangi bir elementin en dar sıvı aralığına sahiptir: 24,55 ila 27,05 K (-248,45 °C ila -245,95 °C veya -415,21 °F ila -410,71 °F). Sıvı helyumun soğutma kapasitesinin (birim hacim başına) 40 katından fazlasına ve sıvı hidrojenin üç katına sahiptir. Çoğu uygulamada helyumdan daha ucuz bir soğutucu akışkandır. ⓘ

Neon plazması, tüm soy gazlar arasında normal voltaj ve akımlarda en yoğun ışık deşarjına sahiptir. Bu ışığın insan gözündeki ortalama rengi, bu aralıktaki birçok çizgi nedeniyle kırmızı-turuncudur; ayrıca görsel bileşenler bir spektroskop tarafından dağıtılmadıkça gizlenen güçlü bir yeşil çizgi içerir. ⓘ
Oldukça farklı iki tür neon aydınlatma yaygın olarak kullanılmaktadır. Neon kızdırma lambaları genellikle küçüktür ve çoğu 100 ila 250 volt arasında çalışır. Güç açık göstergeleri olarak ve devre test ekipmanlarında yaygın olarak kullanılmışlardır, ancak artık bu uygulamalarda ışık yayan diyotlar (LED'ler) hakimdir. Bu basit neon cihazlar, plazma ekranların ve plazma televizyon ekranlarının öncüleriydi. Neon tabelalar tipik olarak çok daha yüksek voltajlarda (2-15 kilovolt) çalışır ve ışıklı tüpler genellikle metrelerce uzunluktadır. Cam borular genellikle tabelaların yanı sıra mimari ve sanatsal uygulamalar için şekil ve harflere dönüştürülür. ⓘ
Oluşum
Neonun kararlı izotopları yıldızlarda üretilir. Neon'un en bol bulunan izotopu 20Ne (%90,48), yıldız nükleosentezinin karbon yakma sürecinde karbon ve karbonun nükleer füzyonuyla oluşur. Bu, 8 güneş kütlesinden daha büyük yıldızların çekirdeklerinde meydana gelen 500 megakelvinin üzerindeki sıcaklıkları gerektirir. ⓘ
Neon evrensel ölçekte bol miktarda bulunur; hidrojen, helyum, oksijen ve karbondan sonra kütle olarak evrende en bol bulunan beşinci kimyasal elementtir (bkz. kimyasal element). Helyum gibi Dünya'daki göreceli nadirliği, göreceli hafifliği, çok düşük sıcaklıklarda yüksek buhar basıncı ve kimyasal inertliğinden kaynaklanmaktadır; tüm bu özellikler, Dünya gibi daha küçük ve daha sıcak katı gezegenleri oluşturan yoğunlaşan gaz ve toz bulutlarında sıkışmasını önleme eğilimindedir. Neon tek atomludur, bu da onu Dünya atmosferinin büyük kısmını oluşturan iki atomlu azot ve oksijen moleküllerinden daha hafif yapar; neonla dolu bir balon, helyum balonundan daha yavaş olsa da havada yükselecektir. ⓘ
Neon'un evrendeki bolluğu yaklaşık 750'de 1'dir; Güneş'te ve muhtemelen proto-güneş sistemi nebulasında ise 600'de 1'dir. Galileo uzay aracı atmosferik giriş sondası, Jüpiter'in üst atmosferinde bile neon bolluğunun kütlece 6.000'de 1 seviyesine kadar yaklaşık 10 kat azaldığını (tükendiğini) bulmuştur. Bu durum, neonu dış güneş sisteminden Jüpiter'e getiren buz-gezegenimsi maddelerin bile neon atmosferik bileşenini muhafaza edemeyecek kadar sıcak bir bölgede oluştuğuna işaret ediyor olabilir (Jüpiter'deki daha ağır asal gazların bolluğu Güneş'te bulunanın birkaç katıdır). ⓘ
Neon Dünya atmosferinde 55.000'de 1 ya da hacim olarak 18,2 ppm (bu yaklaşık olarak molekül ya da mol oranı ile aynıdır) ya da kütle olarak havanın 79.000'de 1'ini oluşturur. Kabukta daha küçük bir kısım oluşturur. Endüstriyel olarak sıvılaştırılmış havanın kriyojenik fraksiyonel damıtılmasıyla üretilir. ⓘ
17 Ağustos 2015 tarihinde, Ay Atmosferi ve Toz Ortamı Kaşifi (LADEE) uzay aracı ile yapılan çalışmalara dayanarak, NASA bilim insanları Ay'ın ekzosferinde neon tespit ettiklerini bildirmişlerdir. ⓘ
Kimya
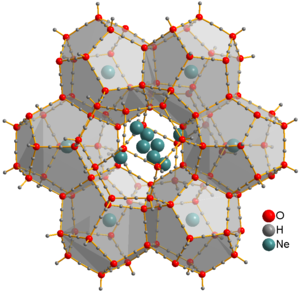
Neon ilk p-blok soy gaz ve gerçek sekiz elektrona sahip ilk elementtir. İnerttir: daha hafif analoğu olan helyumda olduğu gibi, neon içeren güçlü bir şekilde bağlı nötr moleküller tanımlanmamıştır. NeAr]+, [NeH]+ ve [HeNe]+ iyonları optik ve kütle spektrometrik çalışmalarda gözlemlenmiştir. Katı neon klatrat hidrat, 350-480 MPa basınçlarda ve yaklaşık -30 °C sıcaklıklarda su buzu ve neon gazından üretilmiştir. Ne atomları suya bağlı değildir ve bu malzeme içinde serbestçe hareket edebilir. Klatrat birkaç gün boyunca bir vakum odasına yerleştirilerek çıkarılabilir ve suyun en az yoğun kristal formu olan buz XVI elde edilir. ⓘ
Bilinen Pauling elektronegatiflik ölçeği kimyasal bağ enerjilerine dayanır, ancak bu değerler inert helyum ve neon için açıkça ölçülmemiştir. Yalnızca (ölçülebilir) atom enerjilerine dayanan Allen elektronegatiflik ölçeği, neonu en elektronegatif element olarak tanımlar ve hemen ardından flor ve helyum gelir. ⓘ
Neonun üçlü nokta sıcaklığı (24.5561 K) 1990 Uluslararası Sıcaklık Ölçeğinde tanımlayıcı bir sabit noktadır. ⓘ
Üretim
Neon, kriyojenik hava ayırma tesislerinde havadan üretilir. Esas olarak nitrojen, neon ve helyumdan oluşan bir gaz fazı karışımı, yüksek basınçlı hava ayırma kolonunun tepesindeki ana kondansatörden çekilir ve neonun rektifikasyonu için bir yan kolonun altına beslenir. Daha sonra helyumdan daha da saflaştırılabilir. ⓘ
Küresel neon arzının yaklaşık %70'i Rusya'daki çelik üretiminin bir yan ürünü olarak Ukrayna'da üretilmektedir. 2020 itibariyle, Odessa ve Moskova'da tesisleri bulunan Iceblick şirketi, dünya neon üretiminin %65'ini ve kripton ve ksenonun %15'ini tedarik etmektedir. ⓘ
2022 kıtlığı
Rusya'nın 2014 yılında Kırım'ı ilhak etmesinin ardından küresel neon fiyatları yaklaşık %600 oranında artarak bazı çip üreticilerinin Rus ve Ukraynalı tedarikçilerden Çin'deki tedarikçilere yönelmesine yol açmıştır. Rusya'nın 2022'de Ukrayna'yı işgali de Ukrayna'daki iki şirketi kapattı: Sırasıyla Odessa ve Mariupol'da bulunan LLC "Cryoin engineering" (Ukraynaca: ТОВ "Кріоін Інжинірінг") ve LLC "Ingaz" (Ukraynaca: ТОВ "ІНГАЗ"); küresel arzın yaklaşık yarısını üretiyordu. Kapanmanın COVID-19 çip kıtlığını daha da kötüleştireceği ve neon üretiminin Çin'e kaymasına neden olabileceği tahmin ediliyor. ⓘ
Uygulamalar
Neon genellikle tabelalarda kullanılır ve belirgin parlak kırmızımsı-turuncu bir ışık üretir. Diğer renklere sahip tüp ışıklar genellikle "neon" olarak adlandırılsa da, farklı asal gazlar veya çeşitli floresan aydınlatma renkleri kullanırlar. ⓘ
Neon vakum tüplerinde, yüksek voltaj göstergelerinde, paratonerlerde, dalga ölçer tüplerinde, televizyon tüplerinde ve helyum-neon lazerlerde kullanılır. Sıvılaştırılmış neon ticari olarak, daha aşırı sıvı-helyum soğutma ile elde edilebilen daha düşük sıcaklık aralığı gerektirmeyen uygulamalarda kriyojenik soğutucu olarak kullanılır. ⓘ
Sıvı veya gaz olarak neon nispeten pahalıdır - küçük miktarlar için sıvı neonun fiyatı sıvı helyumun 55 katından fazla olabilir. Neonun pahalı olmasının nedeni, helyumun aksine, kullanılabilir miktarlarda ancak atmosferden filtrelenerek elde edilebilen neonun nadir bulunmasıdır. ⓘ
Yarı iletken endüstrisi
2022 itibariyle EUV litografi lazerlerine güç sağlamak için neon içeren gaz karışımları kullanılmaktadır. ⓘ

