Metal

| Bir serinin parçası olarak ⓘ |
| Periyodik tablo |
|---|
|
Eleman kümeleri |
|
Metal (Yunanca μέταλλον métallon, "maden, taş ocağı, metal"), yeni hazırlandığında, cilalandığında veya kırıldığında parlak bir görünüm sergileyen ve elektrik ve ısıyı nispeten iyi ileten bir malzemedir. Metaller tipik olarak dövülebilir (ince tabakalar halinde dövülebilir) veya sünektir (teller halinde çekilebilir). Bir metal, demir gibi kimyasal bir element; paslanmaz çelik gibi bir alaşım; veya polimerik sülfür nitrür gibi moleküler bir bileşik olabilir. ⓘ
Fizikte metal genellikle mutlak sıfır sıcaklıkta elektrik iletebilen herhangi bir madde olarak kabul edilir. Normalde metal olarak sınıflandırılmayan birçok element ve bileşik yüksek basınç altında metalik hale gelir. Örneğin, ametal olan iyot atmosfer basıncının 40 ila 170 bin katı arasında bir basınçta kademeli olarak metal haline gelir. Aynı şekilde, metal olarak kabul edilen bazı maddeler de ametal haline gelebilir. Örneğin sodyum, atmosfer basıncının iki milyon katından biraz daha düşük bir basınçta ametal haline gelir. ⓘ
Kimyada, aksi takdirde (fizikte) kırılgan metaller olarak nitelendirilebilecek iki element -arsenik ve antimon- kimyaları nedeniyle (arsenik için ağırlıklı olarak metalik olmayan ve antimon için metaliklik ve ametaliklik arasında dengeli) yaygın olarak metaloidler olarak kabul edilir. Periyodik tablodaki 118 elementin yaklaşık 95'i metaldir (ya da öyle olması muhtemeldir). Bu sayı kesin değildir çünkü metaller, ametaller ve metaloidler arasındaki sınırlar, ilgili kategorilerin evrensel olarak kabul edilmiş tanımlarının olmaması nedeniyle biraz dalgalanmaktadır. ⓘ
Astrofizikte "metal" terimi, sadece geleneksel metalleri değil, bir yıldızdaki helyumdan daha ağır olan tüm kimyasal elementleri ifade etmek için daha geniş bir şekilde kullanılır. Bu anlamda yıldız çekirdeklerinde nükleosentez yoluyla toplanan ilk dört "metal" karbon, nitrojen, oksijen ve neondur ve bunların hepsi kimyada kesinlikle metal değildir. Bir yıldız ömrü boyunca daha hafif atomları, çoğunlukla hidrojen ve helyumu, daha ağır atomlara dönüştürür. Bu anlamda kullanıldığında, bir astronomik nesnenin metalikliği, maddesinin daha ağır kimyasal elementlerden oluşan oranıdır. ⓘ
Kimyasal elementler olarak metaller yerkabuğunun %25'ini oluşturur ve modern yaşamın pek çok alanında yer alır. Bazı metallerin gücü ve esnekliği, örneğin yüksek bina ve köprü inşaatlarının yanı sıra çoğu araçta, birçok ev aletinde, aletlerde, borularda ve demiryolu raylarında sıkça kullanılmalarına yol açmıştır. Değerli metaller tarihsel olarak madeni para olarak kullanılmıştır, ancak modern çağda madeni para metalleri kimyasal elementlerin en az 23'üne kadar genişlemiştir. ⓘ
Rafine metallerin tarihinin yaklaşık 11.000 yıl önce bakırın kullanılmasıyla başladığı düşünülmektedir. Altın, gümüş, demir (meteorik demir olarak), kurşun ve pirinç de M.Ö. 5. binyılda bronzun bilinen ilk ortaya çıkışından önce aynı şekilde kullanılmaktaydı. Daha sonraki gelişmeler arasında çeliğin ilk formlarının üretimi; 1809 yılında ilk hafif metal olan sodyumun keşfi; modern alaşımlı çeliklerin yükselişi; ve İkinci Dünya Savaşı'nın sonundan bu yana daha sofistike alaşımların geliştirilmesi yer almaktadır. ⓘ
Metal (Latince: metallum, Yunanca: μέταλλον metallon), yüksek elektrik ve ısı iletkenliği, kendine özgü parlaklığı olan, şekillendirmeye yatkın, katyon oluşturma eğilimi yüksek, oksijenle birleşerek çoğunlukla bazik oksitler veren elementler. ⓘ
Metaller, kendi aralarında soy metaller (altın, gümüş, platin gibi) ve soy olmayan metaller (demir, çinko, alüminyum gibi) şeklinde sınıflandırılabilir. Yarı metaller, iyi metal özelliği göstermez. Bu elementler hem metal, hem de ametal özelliği gösterir. Silisyum, bor, antimon, arsenik gibi elementler yarı metaldir. ⓘ
Doğada ametaller daha çok bulunsa da periyodik tablodaki elementlerin çoğu metaldir. ⓘ
Özellikler
Biçim ve yapı

Metaller, en azından yeni hazırlandıklarında, cilalandıklarında veya kırıldıklarında parlak ve ışıltılıdır. Birkaç mikrometreden daha kalın metal levhalar opak görünür, ancak altın varak yeşil ışığı geçirir. ⓘ
Metallerin katı veya sıvı hali büyük ölçüde ilgili metal atomlarının dış kabuk elektronlarını kolayca kaybetme kapasitesinden kaynaklanır. Genel olarak, tek bir atomun dış kabuk elektronlarını yerinde tutan kuvvetler, katı veya sıvı metaldeki atomlar arasındaki etkileşimlerden kaynaklanan aynı elektronlar üzerindeki çekici kuvvetlerden daha zayıftır. İlgili elektronlar yer değiştirir ve bir metalin atomik yapısı, nispeten hareketli elektronlardan oluşan bir bulutun içine gömülmüş bir atomlar topluluğu olarak görselleştirilebilir. Bu tür bir etkileşime metalik bağ adı verilir. Farklı temel metaller için metalik bağların gücü, geçiş metali serisinin merkezi etrafında maksimuma ulaşır, çünkü bu elementler çok sayıda delokalize elektrona sahiptir. ⓘ
Çoğu temel metal, çoğu ametalden daha yüksek yoğunluğa sahip olsa da, yoğunluklarında geniş bir varyasyon vardır; lityum en az yoğun (0,534 g/cm3) ve osmiyum (22,59 g/cm3) en yoğun olanıdır. Magnezyum, alüminyum ve titanyum önemli ticari öneme sahip hafif metallerdir. Bunların 1.7, 2.7 ve 4.5 g/cm3 olan yoğunlukları, 7.9 g/cm3 demir ve 8.9 g/cm3 bakır gibi daha eski yapısal metallerin yoğunlukları ile karşılaştırılabilir. Dolayısıyla bir demir bilye yaklaşık olarak eşit hacimdeki üç alüminyum bilye kadar ağırlığa sahip olacaktır. ⓘ

Metaller tipik olarak dövülebilir ve sünektir, gerilim altında yarılmadan deforme olurlar. Metalik bağın yönsüz doğasının çoğu metalik katının sünekliğine önemli ölçüde katkıda bulunduğu düşünülmektedir. Buna karşılık, sofra tuzu gibi iyonik bir bileşikte, iyonik bir bağın düzlemleri birbirinin yanından geçtiğinde, ortaya çıkan konum değişikliği aynı yüke sahip iyonları birbirine yaklaştırarak kristalin yarılmasına neden olur. Böyle bir kayma, kırılma ve kristal parçalanmasının meydana geldiği elmas gibi kovalent bağlı bir kristalde gözlenmez. Metallerdeki tersinir elastik deformasyon, gerilimin gerinimle doğrusal olarak orantılı olduğu geri yükleme kuvvetleri için Hooke Yasası ile tanımlanabilir. ⓘ
Bir metalin elastik limitinden daha büyük ısı veya kuvvetler, plastik deformasyon veya plastisite olarak bilinen kalıcı (geri döndürülemez) bir deformasyona neden olabilir. Uygulanan bir kuvvet çekme (çekme) kuvveti, basma (itme) kuvveti veya kesme, eğme veya burma (bükme) kuvveti olabilir. Sıcaklık değişimi, hem kristal hem de kristal olmayan metallerde tane sınırları, nokta boşlukları, çizgi ve vida çıkıkları, istifleme hataları ve ikizler gibi metaldeki yapısal kusurların hareketini veya yer değiştirmesini etkileyebilir. İç kayma, sürünme ve metal yorgunluğu ortaya çıkabilir. ⓘ
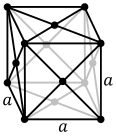
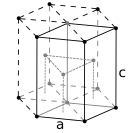
Metalik maddelerin atomları tipik olarak üç yaygın kristal yapıdan birinde düzenlenir: gövde merkezli kübik (bcc), yüz merkezli kübik (fcc) ve altıgen yakın paketlenmiş (hcp). Bcc'de her bir atom, diğer sekiz atomdan oluşan bir küpün merkezinde yer alır. Fcc ve hcp'de her atom on iki atomla çevrilidir, ancak katmanların istiflenmesi farklıdır. Bazı metaller sıcaklığa bağlı olarak farklı yapılar benimser. ⓘ
- Örneğin titanyum, kobalt ve çinkoda bulunan 6 atomlu birim hücreye sahip altıgen yakın paketlenmiş kristal yapıⓘ
Her kristal yapı için birim hücre, kristalin genel simetrisine sahip olan ve tüm kristal kafesin üç boyutta tekrarlanarak oluşturulabildiği en küçük atom grubudur. Yukarıda gösterilen gövde merkezli kübik kristal yapı durumunda, birim hücre merkezi atom artı sekiz köşe atomunun her birinin sekizde birinden oluşur. ⓘ
Elektriksel ve termal

Metallerin elektronik yapısı, nispeten iyi elektrik iletkenleri oldukları anlamına gelir. Maddedeki elektronlar değişken enerji seviyeleri yerine sadece sabit enerji seviyelerine sahip olabilir ve bir metalde elektron bulutundaki elektronların enerji seviyeleri, en azından bir dereceye kadar, elektrik iletiminin gerçekleşebileceği enerji seviyelerine karşılık gelir. Silikon gibi bir yarı iletkende veya sülfür gibi bir ametalde, maddedeki elektronlar ile elektrik iletiminin gerçekleşebileceği enerji seviyesi arasında bir enerji boşluğu vardır. Sonuç olarak, yarı iletkenler ve ametaller nispeten zayıf iletkenlerdir. ⓘ
Temel metaller, manganez için 6,9 × 103 S/cm'den gümüş için 6,3 × 105 S/cm'ye kadar elektrik iletkenlik değerlerine sahiptir. Buna karşılık, bor gibi yarı iletken bir metaloid 1,5 × 10-6 S/cm elektrik iletkenliğine sahiptir. Bir istisna dışında, metalik elementler ısıtıldıklarında elektrik iletkenliklerini azaltırlar. Plütonyum, yaklaşık -175 ila +125 °C sıcaklık aralığında ısıtıldığında elektrik iletkenliğini artırır. ⓘ
Metaller nispeten iyi ısı iletkenleridir. Bir metalin elektron bulutundaki elektronlar oldukça hareketlidir ve ısı kaynaklı titreşim enerjisini kolayca aktarabilirler. ⓘ
Bir metalin elektronlarının ısı kapasitesine ve termal iletkenliğine katkısı ve metalin elektrik iletkenliği serbest elektron modelinden hesaplanabilir. Ancak bu, metalin iyon kafesinin ayrıntılı yapısını dikkate almaz. İyon çekirdeklerinin düzenlenmesinden kaynaklanan pozitif potansiyelin hesaba katılması, bir metalin elektronik bant yapısının ve bağlanma enerjisinin dikkate alınmasını sağlar. En basiti neredeyse serbest elektron modeli olmak üzere çeşitli matematiksel modeller uygulanabilir. ⓘ
Kimyasal
Metaller genellikle elektron kaybı yoluyla katyon oluşturma eğilimindedir. Çoğu havadaki oksijenle tepkimeye girerek çeşitli zaman ölçeklerinde oksitler oluşturur (potasyum saniyeler içinde yanarken demir yıllar içinde paslanır). Paladyum, platin ve altın gibi bazıları ise atmosferle hiç reaksiyona girmez. Asidik veya nötr olan ametallerin aksine metallerin oksitleri genellikle baziktir. Bunun istisnaları CrO3, Mn2O7 ve OsO4 gibi çok yüksek oksidasyon durumlarına sahip olan ve kesinlikle asidik reaksiyonlar veren oksitlerdir. ⓘ
Metallerin boyanması, anotlanması veya kaplanması korozyonu önlemenin iyi yollarıdır. Ancak, özellikle kaplamanın ufalanması bekleniyorsa, kaplama için elektrokimyasal seride daha reaktif bir metal seçilmelidir. Su ve iki metal bir elektrokimyasal hücre oluşturur ve kaplama alttaki metalden daha az reaktifse, kaplama aslında korozyonu teşvik eder. ⓘ
En çok kullanılan metaller
Metallerin özellikleri
- Tel ve levha haline getirilebilirler.
- Cıva dışındaki tüm metaller oda sıcaklığında katıdır.
- Işığı yansıtma özellikleri vardır.
- Isı ve elektriği iletirler.
- Nispeten yoğunlukları fazladır.
- Vurulduklarında metal tınılı ses çıkarırlar.
- Gri ve kırmızı renk tonlarındadırlar.
- Yüksek mukavemet değerlerine sahiptirler.
- Kısa mesafeli düzenli atom dizilişine sahiptirler. Buna kristal yapı denilmektedir.
- Bileşik oluşturmazlar. (Alaşım yaparlar)
- Yüzeyleri Parlaktır. ⓘ
Periyodik tablo dağılımı
Kimyada, olağan koşullar altında genellikle metal olarak kabul edilen elementler aşağıdaki periyodik tabloda sarı renkle gösterilmiştir. Geri kalan elementler ya metaloid (B, Si, Ge, As, Sb ve Te yaygın olarak bu şekilde kabul edilir) ya da ametaldir. Astatin (At) genellikle ya ametal ya da metaloid olarak sınıflandırılır, ancak bazı tahminler onun bir metal olmasını beklemektedir; bu nedenle, deneysel bilginin kesin olmayan durumu nedeniyle boş bırakılmıştır. Bilinmeyen özelliklere sahip olarak gösterilen diğer elementlerin metal olması muhtemeldir, ancak kopernisyum (Cn) ve oganesson (Og) için bazı şüpheler vardır. ⓘ
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Grup → | ||||||||||||||||||||||||||||||||
| ↓ Dönem | ||||||||||||||||||||||||||||||||
| 1 | H | O | ||||||||||||||||||||||||||||||
| 2 | Li | Olmak | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | İçinde | Sn | Sb | Te | I | Xe | ||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Yeniden | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | Hayır | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
Alaşımlar
Alaşım, metalik özelliklere sahip olan ve en az biri metal olan iki veya daha fazla elementten oluşan bir maddedir. Bir alaşım değişken veya sabit bir bileşime sahip olabilir. Örneğin, altın ve gümüş, altın veya gümüş oranlarının serbestçe ayarlanabildiği bir alaşım oluşturur; titanyum ve silikon, iki bileşenin oranının sabit olduğu bir Ti2Si alaşımı oluşturur (metaller arası bileşik olarak da bilinir). ⓘ

Saf metallerin çoğu pratik kullanım için ya çok yumuşak, kırılgan ya da kimyasal olarak reaktiftir. Farklı oranlardaki metallerin alaşım olarak birleştirilmesi, saf metallerin özelliklerini değiştirerek arzu edilen özellikleri ortaya çıkarır. Alaşım yapmanın amacı genellikle onları daha az kırılgan, daha sert, korozyona karşı dirençli veya daha arzu edilen bir renk ve parlaklığa sahip hale getirmektir. Günümüzde kullanılan tüm metalik alaşımlar arasında demir alaşımları (çelik, paslanmaz çelik, dökme demir, takım çeliği, alaşımlı çelik) hem miktar hem de ticari değer olarak en büyük oranı oluşturmaktadır. Çeşitli oranlarda karbon ile alaşımlandırılmış demir düşük, orta ve yüksek karbonlu çelikler verir, artan karbon seviyeleri sünekliği ve tokluğu azaltır. Silisyum ilavesi dökme demirler üretirken, karbon çeliklerine krom, nikel ve molibden ilavesi (%10'dan fazla) paslanmaz çeliklerle sonuçlanır. ⓘ
Diğer önemli metalik alaşımlar alüminyum, titanyum, bakır ve magnezyum alaşımlarıdır. Bakır alaşımları tarih öncesinden beri bilinmektedir - Bronz Çağı'na adını veren bronzdur - ve günümüzde en önemlisi elektrik kablolarında olmak üzere birçok uygulama alanına sahiptir. Diğer üç metalin alaşımları nispeten yakın zamanda geliştirilmiştir; kimyasal reaktiviteleri nedeniyle elektrolitik ekstraksiyon işlemleri gerektirirler. Alüminyum, titanyum ve magnezyum alaşımları yüksek mukavemet/ağırlık oranları nedeniyle değerlidir; magnezyum ayrıca elektromanyetik kalkan da sağlayabilir. Bu malzemeler, havacılık ve bazı otomotiv uygulamaları gibi yüksek mukavemet/ağırlık oranının malzeme maliyetinden daha önemli olduğu durumlar için idealdir. ⓘ
Jet motorları gibi son derece zorlu uygulamalar için özel olarak tasarlanmış alaşımlar ondan fazla element içerebilir. ⓘ
Kategoriler
- Bakır yumuşak bir metal olmasının yanı sıra iyi de bir iletkendir. Bu sebepten dolayı bakır, elektrik kablolarında kullanılmaktadır.
- Altın ve gümüş, işlenebilir, iletken ve inaktif metallerdir. Bu nedenle bu iki metal mücevher olarak kullanılmaktadır. Altın kimi zamanlarda elektrik kablolarında kullanılmaktadır.
- Demir ve çeliğin her ikisi de serttir. Bu nedenle bu metaller yapılarda kullanılmaktadır. Ancak demir paslanabildiği için paslanmaz çelik formülleri üretilmiştir.
- Alüminyum yumuşak ve ısı iletkeni bir metaldir. Bu nedenle bu metal folyo ve tencerelerde kullanılmaktadır. Ayrıca uçak gövdelerinde hafif olmasından dolayı tercih edilmektedir. ⓘ
Demir ve demir dışı metaller
"Demirli" terimi Latince "demir içeren" anlamına gelen kelimeden türetilmiştir. Bu, dövme demir gibi saf demiri veya çelik gibi bir alaşımı içerebilir. Demir içeren metaller genellikle manyetiktir, ancak sadece manyetik değildir. Demir içermeyen metaller ve alaşımlarda kayda değer miktarda demir bulunmaz. ⓘ
Kırılgan metal
Neredeyse tüm metaller dövülebilir veya sünek iken, birkaçı -berilyum, krom, manganez, galyum ve bizmut- kırılgandır. Arsenik ve antimon, metal olarak kabul edilirse, kırılgandır. Yığın elastik modülünün kayma modülüne oranının düşük değerleri (Pugh kriteri) içsel kırılganlığın göstergesidir. ⓘ
Refrakter metal
Malzeme bilimi, metalurji ve mühendislikte refrakter metal, ısıya ve aşınmaya karşı olağanüstü dirençli bir metaldir. Hangi metallerin bu kategoriye ait olduğu değişir; en yaygın tanım niyobyum, molibden, tantal, tungsten ve renyum içerir. Hepsinin erime noktası 2000 °C'nin üzerindedir ve oda sıcaklığında yüksek sertliğe sahiptirler. ⓘ
Beyaz metal
Beyaz metal, nispeten düşük erime noktasına sahip beyaz renkli metallerden (veya alaşımlarından) herhangi biridir. Bu metaller arasında çinko, kadmiyum, kalay, antimon (burada bir metal olarak sayılmıştır), kurşun ve bizmut yer alır ve bunlardan bazıları oldukça zehirlidir. İngiltere'de güzel sanatlar ticareti, müzayede kataloglarında İngiliz Tahlil Ofisi işaretleri taşımayan, ancak yine de gümüş olduğu anlaşılan ve buna göre fiyatlandırılan yabancı gümüş eşyaları tanımlamak için "beyaz metal" terimini kullanır. ⓘ
Ağır ve hafif metaller
Ağır metal, nispeten yoğun herhangi bir metal veya metaloiddir. Daha spesifik tanımlar önerilmiştir, ancak hiçbiri yaygın kabul görmemiştir. Bazı ağır metaller niş kullanım alanlarına sahiptir veya özellikle toksiktir; bazıları ise eser miktarda gereklidir. Diğer tüm metaller hafif metallerdir. ⓘ
Baz, asil ve değerli metaller
Kimyada baz metal terimi, seyreltik hidroklorik asit (HCl) ile kolayca reaksiyona girerek metal klorür ve hidrojen oluşturmak gibi kolayca oksitlenen veya aşınan bir metali ifade etmek için gayri resmi olarak kullanılır. Örnekler arasında demir, nikel, kurşun ve çinko yer alır. Bakır, HCl ile reaksiyona girmemesine rağmen nispeten kolay oksitlendiği için baz metal olarak kabul edilir. ⓘ

Asil metal terimi genellikle ana metalin karşıtı olarak kullanılır. Asil metaller çoğu baz metalin aksine korozyona veya oksidasyona karşı dirençlidir. Genellikle algılanan nadirlik nedeniyle değerli metaller olma eğilimindedirler. Örnek olarak altın, platin, gümüş, rodyum, iridyum ve paladyum verilebilir. ⓘ
Simya ve nümizmatikte baz metal terimi değerli metallerle, yani yüksek ekonomik değere sahip olanlarla karşılaştırılır. Simyacıların uzun süreli hedeflerinden biri, ana metallerin gümüş ve altın gibi sikke metalleri de dahil olmak üzere değerli metallere dönüştürülmesiydi. Günümüzde madeni paraların çoğu içsel değeri düşük olan baz metallerden yapılmaktadır; geçmişte madeni paralar değerlerini çoğunlukla değerli metal içeriklerinden alırlardı. ⓘ
Kimyasal olarak, değerli metaller (soy metaller gibi) çoğu elementten daha az reaktiftir, yüksek parlaklığa ve yüksek elektrik iletkenliğine sahiptir. Tarihsel olarak, değerli metaller para birimi olarak önemliydi, ancak şimdi esas olarak yatırım ve endüstriyel emtia olarak kabul edilmektedir. Altın, gümüş, platin ve paladyumun her birinin ISO 4217 para birimi kodu vardır. En iyi bilinen değerli metaller altın ve gümüştür. Her ikisinin de endüstriyel kullanımları olsa da, daha çok sanat, mücevher ve madeni para kullanımlarıyla bilinirler. Diğer değerli metaller platin grubu metalleri içerir: rutenyum, rodyum, paladyum, osmiyum, iridyum ve platin, bunlardan en yaygın olarak platin ticareti yapılır. ⓘ
Değerli metallere olan talep yalnızca pratik kullanımlarından değil, aynı zamanda yatırım ve değer saklama aracı olarak oynadıkları rolden de kaynaklanmaktadır. Paladyum ve platin, 2018 sonbaharı itibariyle, altın fiyatının yaklaşık dörtte üçü değerindeydi. Gümüş bu metallerden önemli ölçüde daha ucuzdur, ancak sikke ve mücevherlerdeki rolü nedeniyle genellikle geleneksel olarak değerli bir metal olarak kabul edilir. ⓘ
Valf metalleri
Elektrokimyada valf metali, akımı sadece bir yönde geçiren metaldir. ⓘ
Yaşam döngüsü
Oluşum
| ağırlıkça bolluk ve ana oluşum veya kaynak | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
| 1 | H | O | |||||||||||||||||
| 2 | Li | Olmak | B | C | N | O | F | Ne | |||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Ru | Rh | Pd | Ag | Cd | İçinde | Sn | Sb | Te | I | Xe | ||
| 6 | Cs | Ba | Lu | Hf | Ta | W | Yeniden | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | ||||
| 7 | |||||||||||||||||||
| La | Ce | Pr | Nd | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | |||||||
| Th | U | ||||||||||||||||||
En bol bulunan (82000 ppm'e kadar)
| |||||||||||||||||||
Bol miktarda (100-999 ppm)
| |||||||||||||||||||
Yaygın olmayan (1-99 ppm)
| |||||||||||||||||||
Nadir (0,01-0,99 ppm)
| |||||||||||||||||||
Çok nadir (0,0001-0,0099 ppm)
| |||||||||||||||||||
| Ayrım çizgisinin solundaki metaller esas olarak litofil olarak ortaya çıkar (veya kaynaklanır); sağdakiler ise altın (bir siderofil) ve kalay (bir litofil) hariç kalkofil olarak ortaya çıkar. | |||||||||||||||||||
- Bu alt bölüm periyodik tablo element metallerinin oluşumunu ele almaktadır çünkü bunlar bu makalede tanımlandığı şekliyle metalik malzemelerin temelini oluşturmaktadır. ⓘ
Periyodik tabloda demir civarına kadar olan metaller büyük ölçüde yıldız nükleosentezi yoluyla oluşur. Bu süreçte, hidrojenden silikona kadar daha hafif elementler yıldızların içinde art arda füzyon reaksiyonlarına girerek ışık ve ısı açığa çıkarır ve daha yüksek atom numaralarına sahip daha ağır elementler oluşturur. ⓘ
Daha ağır metaller genellikle bu şekilde oluşmaz, çünkü bu tür çekirdekleri içeren füzyon reaksiyonları enerji açığa çıkarmak yerine tüketir. Bunun yerine, büyük ölçüde nötron yakalama yoluyla (daha düşük atom numarasına sahip elementlerden) sentezlenirler; bu tekrarlayan yakalamanın iki ana modu s-süreci ve r-sürecidir. S-sürecinde ("s" "yavaş" anlamına gelir), tekil yakalamalar yıllar veya on yıllar boyunca ayrılır ve daha az kararlı çekirdeklerin beta bozunmasına izin verirken, r-sürecinde ("hızlı"), yakalamalar çekirdeklerin bozunabileceğinden daha hızlı gerçekleşir. Bu nedenle, s-süreci az ya da çok net bir yol izler: örneğin, kararlı kadmiyum-110 çekirdekleri, kararsız olan kadmiyum-115 çekirdeklerini oluşturana kadar bir yıldızın içindeki serbest nötronlar tarafından art arda bombardımana tutulur ve indiyum-115 (neredeyse kararlıdır, yarı ömrü evrenin yaşının 30000 katıdır) oluşturmak üzere bozunur. Bu çekirdekler nötronları yakalar ve kararsız olan indiyum-116'yı oluşturur ve kalay-116'yı oluşturmak üzere bozunur ve bu böyle devam eder. Buna karşılık, r-sürecinde böyle bir yol yoktur. Bizmut veya kurşuna bozunan sonraki iki element olan polonyum ve astatinin kısa yarı ömürleri nedeniyle s-süreci bizmutta durur. R süreci o kadar hızlıdır ki bu kararsızlık bölgesini atlayabilir ve toryum ve uranyum gibi daha ağır elementleri oluşturmaya devam edebilir. ⓘ
Metaller, yıldız evrimi ve yıkım süreçlerinin bir sonucu olarak gezegenlerde yoğunlaşır. Yıldızlar yaşamlarının sonlarına doğru ve bazen de nötron yıldızlarının birleşmesi sonucunda kütlelerinin büyük bir kısmını kaybederler ve böylece yıldızlararası ortamda helyumdan daha ağır elementlerin bolluğu artar. Kütleçekimsel çekim bu maddenin birleşmesine ve çökmesine neden olduğunda yeni yıldızlar ve gezegenler oluşur. ⓘ
Bolluk ve oluşum

Yerkabuğunun ağırlıkça yaklaşık %25'i metallerden oluşur ve bunların %80'i sodyum, magnezyum ve alüminyum gibi hafif metallerdir. Kabuğun geri kalanını ametaller (~%75) oluşturur. Bakır gibi bazı ağır metallerin genel kıtlığına rağmen, dağ inşası, erozyon veya diğer jeolojik süreçlerin bir sonucu olarak ekonomik olarak çıkarılabilir miktarlarda yoğunlaşabilirler. ⓘ
Metaller öncelikle litofil (kaya seven) veya kalkofil (cevher seven) olarak bulunur. Litofil metaller çoğunlukla s-blok elementler, d-blok elementlerin daha reaktif olanları ve f-blok elementlerdir. Oksijene karşı güçlü bir yakınlıkları vardır ve çoğunlukla nispeten düşük yoğunluklu silikat mineralleri olarak bulunurlar. Kalkofil metaller esas olarak daha az reaktif d-blok elementleri ve 4-6 p-blok metalleridir. Genellikle (çözünmeyen) sülfit minerallerinde bulunurlar. Litofillerden daha yoğun olan, dolayısıyla katılaşma sırasında kabuğa daha az batan kalkofiller, litofillerden daha az bol olma eğilimindedir. ⓘ
Öte yandan, altın siderofil ya da demir seven bir elementtir. Oksijen ya da sülfür ile kolayca bileşik oluşturmaz. Dünya'nın oluşumu sırasında ve metallerin en soylusu (inert) olarak altın, yüksek yoğunluklu metalik alaşımlar oluşturma eğilimi nedeniyle çekirdeğe batmıştır. Sonuç olarak, nispeten nadir bulunan bir metaldir. Diğer bazı (daha az) asil metaller - molibden, renyum, platin grubu metaller (rutenyum, rodyum, paladyum, osmiyum, iridyum ve platin), germanyum ve kalay - siderofil olarak sayılabilir, ancak yalnızca Dünya'da (çekirdek, manto ve kabuk), daha ziyade kabukta birincil oluşumları açısından. Bu metaller aksi takdirde kabukta küçük miktarlarda, esas olarak kalkofil olarak (doğal formlarında daha az) ortaya çıkar. ⓘ
Çoğunlukla demirden oluşan Dünya'nın iç kısmındaki dönen akışkan dış çekirdeğin, Dünya'nın koruyucu manyetik alanının kaynağı olduğu düşünülmektedir. Çekirdek, Dünya'nın katı iç çekirdeğinin üzerinde ve mantosunun altında yer alır. Eğer 5 m2'lik (54 sq ft) bir alana sahip bir sütun şeklinde yeniden düzenlenebilseydi, yaklaşık 700 ışık yılı yüksekliğe sahip olurdu. Manyetik alan, Dünya'yı güneş rüzgarının yüklü parçacıklarından ve aksi takdirde üst atmosferi (ultraviyole radyasyonun geçişini sınırlayan ozon tabakası da dahil olmak üzere) soyacak olan kozmik ışınlardan korur. ⓘ
Ekstraksiyon
Metaller genellikle boksit gibi gerekli elementlerin zengin kaynakları olan maden cevherleri aracılığıyla yeryüzünden çıkarılır. Cevher, maden arama teknikleri ve ardından yatakların araştırılması ve incelenmesi ile bulunur. Maden kaynakları genellikle ağır ekipmanlar kullanılarak kazı yoluyla çıkarılan yüzey madenleri ve yeraltı madenleri olarak ikiye ayrılır. Bazı durumlarda, ilgili metal(ler)in satış fiyatı, daha düşük konsantrasyonlu kaynakların çıkarılmasını ekonomik olarak uygun hale getirir. ⓘ
Cevher çıkarıldıktan sonra, metallerin genellikle kimyasal veya elektrolitik indirgeme yoluyla çıkarılması gerekir. Pirometalurji cevheri ham metale dönüştürmek için yüksek sıcaklıklar kullanırken, hidrometalurji aynı amaçla sulu kimya kullanır. Kullanılan yöntemler metale ve kirleticilerine bağlıdır. ⓘ
Bir metal cevheri, o metalin ve metal olmayan bir maddenin iyonik bir bileşiği olduğunda, saf metali çıkarmak için cevherin genellikle eritilmesi (indirgeyici bir madde ile ısıtılması) gerekir. Demir gibi birçok yaygın metal, indirgeyici madde olarak karbon kullanılarak eritilir. Alüminyum ve sodyum gibi bazı metallerin ticari olarak pratik bir indirgeyici maddesi yoktur ve bunun yerine elektroliz kullanılarak çıkarılır. ⓘ
Sülfür cevherleri doğrudan metale indirgenmez, ancak oksitlere dönüştürmek için havada kavrulur. ⓘ
Kullanım Alanları

Metaller modern yaşamın neredeyse her alanında mevcuttur. Ağır bir metal olan demir, tüm rafine metallerin %90'ını oluşturduğundan en yaygın olanı olabilir; hafif bir metal olan alüminyum ise bir sonraki en yaygın rafine metaldir. Saf demir, gram başına yaklaşık 0,07 ABD doları maliyetiyle en ucuz metalik element olabilir. Cevherleri yaygındır; rafine edilmesi kolaydır ve ilgili teknoloji yüzlerce yılda geliştirilmiştir. Dökme demir daha da ucuzdur, gram başına 0,01 ABD dolarının altındadır, çünkü daha sonra saflaştırmaya gerek yoktur. Gramı yaklaşık 27 ABD doları olan platin, çok yüksek erime noktası, korozyona karşı direnci, elektrik iletkenliği ve dayanıklılığı göz önüne alındığında en yaygın olanı olabilir. Tüm tüketim mallarının %20'sinde bulunduğu ya da üretiminde kullanıldığı söylenmektedir. Polonyum, kıtlığı ve mikro ölçekli üretimi nedeniyle gram başına yaklaşık 100.000.000 $'lık nominal maliyetiyle muhtemelen en pahalı metal olacaktır. ⓘ
Bazı metaller ve metal alaşımları birim kütle başına yüksek yapısal mukavemete sahiptir, bu da onları büyük yükleri taşımak veya darbe hasarına direnmek için kullanışlı malzemeler haline getirir. Metal alaşımları kesme, tork ve deformasyona karşı yüksek direnç gösterecek şekilde tasarlanabilir. Ancak aynı metal, tekrarlanan kullanımdan veya yük kapasitesi aşıldığında ani stres arızasından kaynaklanan yorulma hasarına karşı da savunmasız olabilir. Metallerin gücü ve esnekliği, yüksek bina ve köprü inşaatlarının yanı sıra çoğu araçta, birçok cihazda, alette, borularda ve demiryolu raylarında sıkça kullanılmalarına yol açmıştır. ⓘ
Metaller iyi iletkenlerdir, bu da onları elektrikli cihazlarda ve elektrik akımını az enerji kaybıyla belli bir mesafeye taşımak için değerli kılar. Elektrik şebekeleri elektriği dağıtmak için metal kabloları kullanır. Evlerdeki elektrik sistemleri, çoğunlukla, iyi iletkenlik özellikleri nedeniyle bakır telle bağlanır. ⓘ
Metallerin termal iletkenliği, malzemeleri alev üzerinde ısıtmak için kaplar için kullanışlıdır. Metaller ayrıca hassas ekipmanları aşırı ısınmadan korumak için ısı alıcıları olarak da kullanılır. ⓘ
Bazı metallerin yüksek yansıtma özelliği, hassas astronomik aletler de dahil olmak üzere aynalarda kullanılmalarını sağlar ve metalik mücevherlerin estetiğine katkıda bulunur. ⓘ
Bazı metallerin özel kullanımları vardır; cıva oda sıcaklığında bir sıvıdır ve anahtar kontakları üzerinden aktığı zaman bir devreyi tamamlamak için anahtarlarda kullanılır. Uranyum ve plütonyum gibi radyoaktif metaller, nükleer fisyon yoluyla enerji üreten nükleer enerji santralleri için yakıttır. Şekil hafızalı alaşımlar borular, bağlantı elemanları ve vasküler stentler gibi uygulamalar için kullanılır. ⓘ
Metaller yabancı moleküllerle -organik, inorganik, biyolojik ve polimerlerle- katkılanabilir. Bu katkılama, metale konuk moleküller tarafından indüklenen yeni özellikler kazandırır. Kataliz, tıp, elektrokimyasal hücreler, korozyon ve daha birçok alanda uygulamalar geliştirilmiştir. ⓘ
Geri Dönüşüm

Metallere olan talep, altyapı, inşaat, imalat ve tüketim mallarında kullanılmaları nedeniyle ekonomik büyüme ile yakından bağlantılıdır. 20. yüzyıl boyunca toplumda kullanılan metallerin çeşitliliği hızla artmıştır. Bugün, Çin ve Hindistan gibi büyük ulusların gelişimi ve teknolojik ilerlemeler, daha fazla talebi körüklemektedir. Sonuç olarak madencilik faaliyetleri genişlemekte ve dünyadaki metal stoklarının giderek daha büyük bir kısmı kullanılmayan rezervler olarak yer altında değil, kullanımda olan yer üstünde bulunmaktadır. Kullanımdaki bakır stoku buna bir örnektir. 1932 ve 1999 yılları arasında ABD'de kullanılan bakır miktarı kişi başına 73 g'dan 238 g'a yükselmiştir. ⓘ
Metaller doğaları gereği geri dönüştürülebilir, dolayısıyla prensip olarak tekrar tekrar kullanılabilir, bu da bu olumsuz çevresel etkileri en aza indirir ve enerji tasarrufu sağlar. Örneğin, boksit cevherinden alüminyum elde etmek için kullanılan enerjinin %95'i geri dönüştürülmüş malzeme kullanılarak tasarruf edilmektedir. ⓘ
Küresel olarak metal geri dönüşümü genellikle düşüktür. 2010 yılında Birleşmiş Milletler Çevre Programı tarafından düzenlenen Uluslararası Kaynak Paneli, toplumda var olan metal stokları ve bunların geri dönüşüm oranları hakkında bir rapor yayınlamıştır. Raporun yazarları, toplumdaki metal stoklarının yer üstünde büyük madenler olarak işlev görebileceğini gözlemlemişlerdir. Cep telefonları, hibrid arabalar için batarya paketleri ve yakıt hücreleri gibi uygulamalarda kullanılan bazı nadir metallerin geri dönüşüm oranlarının o kadar düşük olduğu konusunda uyarıda bulunmuşlardır ki, gelecekte kullanım ömrü sonu geri dönüşüm oranları önemli ölçüde artırılmazsa bu kritik metaller modern teknolojide kullanılamaz hale gelecektir. ⓘ
Biyolojik etkileşimler
Metalik elementlerin hücre biyokimyasının evrimindeki rolü, kalsiyumun redoks enzimlerindeki rolüne ilişkin ayrıntılı bir bölüm de dahil olmak üzere gözden geçirilmiştir. ⓘ
Demir, kobalt, nikel, bakır ve çinko elementlerinden biri veya daha fazlası tüm yüksek yaşam formları için gereklidir. Molibden, B12 vitamininin temel bir bileşenidir. Antimon ve kalayın bazı bileşikleri gibi birkaç istisna dışında, diğer tüm geçiş elementlerinin ve geçiş sonrası elementlerin bileşikleri az ya da çok toksiktir. Potansiyel metal zehirlenmesi kaynakları arasında madencilik, atık, endüstriyel atıklar, tarımsal yüzey akışı, mesleki maruziyet, boyalar ve işlenmiş kereste yer almaktadır. ⓘ
Tarihçe
Tarih Öncesi
Doğal halde bulunan bakır, kendine özgü görünümü, ağırlığı ve diğer taş ya da çakıllara kıyasla işlenebilirliği nedeniyle keşfedilen ilk metal olabilir. Altın, gümüş ve demir (meteorik demir olarak) ve kurşun da aynı şekilde tarih öncesinde keşfedilmiştir. Bu metallerin cevherlerinin aynı anda eritilmesiyle elde edilen bakır ve çinko alaşımı olan pirinç formları bu döneme aittir (saf çinko 13. yüzyıla kadar izole edilmemiş olsa da). Katı metallerin işlenebilirliği, metal süs eşyaları, aletler ve silahlar üretmeye yönelik ilk girişimlere yol açmıştır. Zaman zaman nikel içeren meteorik demir keşfedilmiştir ve bazı açılardan alaşımlı çeliklerin öne çıktığı 1880'lere kadar üretilen tüm endüstriyel çeliklerden daha üstündür. ⓘ
- oksitlenmiş kurşun
nodüller ve 1 cm3 küp
Antik Çağ
Bronzun (bakırın arsenik veya kalayla alaşımı) keşfi, insanların daha önce mümkün olandan daha sert ve daha dayanıklı metal nesneler yaratmasını sağlamıştır. Bronz aletler, silahlar, zırhlar ve dekoratif kiremitler gibi yapı malzemeleri, taş ve bakır ("Kalkolitik") öncüllerinden daha sert ve daha dayanıklıydı. Başlangıçta bronz, doğal veya yapay olarak karıştırılmış bakır ve arsenik cevherlerinin eritilmesiyle bakır ve arsenikten (arsenik bronzu oluşturarak) yapılmıştır. Şimdiye kadar bilinen en eski eserler M.Ö. 5. binyılda İran platosundan gelmektedir. Kalay ancak daha sonra kullanılmaya başlanmış ve M.Ö. 3. binyılın sonlarında bronzun bakır içermeyen ana maddesi haline gelmiştir. Saf kalayın kendisi ilk kez M.Ö. 1800 yılında Çinli ve Japon metal işçileri tarafından izole edilmiştir. ⓘ
Cıva, M.Ö. 2000'den önce eski Çinliler ve Hintliler tarafından biliniyordu ve M.Ö. 1500'den kalma Mısır mezarlarında bulundu. ⓘ
Demir-karbon alaşımı olan çeliğin bilinen en eski üretimi, Anadolu'daki bir arkeolojik alandan (Kaman-Kalehöyük) çıkarılan ve M.Ö. 1800'lerden kalma yaklaşık 4.000 yıllık demir eşya parçalarında görülmektedir. ⓘ
M.Ö. 500'lerden itibaren İspanya'nın Toledo kentindeki kılıç yapımcıları, demir cevherine (ve karbona) tungsten ve manganez içeren wolframit adlı bir mineral ekleyerek alaşımlı çeliğin ilk formlarını üretiyorlardı. Elde edilen Toledo çeliği, Pön Savaşları'nda Hannibal tarafından kullanıldığında Roma'nın dikkatini çekti. Kısa süre içinde Roma lejyonlarının silahlarının temeli haline geldi; kılıçlarının "o kadar keskin olduğu söylenir ki, kesemeyeceği miğfer yoktur". ⓘ
Kolomb öncesi Amerika'da, bakır ve altın alaşımı olan tumbagadan yapılmış nesneler MS 300 ile 500 yılları arasında Panama ve Kosta Rika'da üretilmeye başlandı. Küçük metal heykeller yaygındı ve çok çeşitli tumbaga (ve altın) süs eşyaları yüksek statüdeki kişilerin olağan kıyafetlerini oluşturuyordu. ⓘ
Yaklaşık aynı zamanlarda yerli Ekvadorlular altını az miktarda paladyum, rodyum ve iridyum içeren ve doğal olarak oluşan bir platin alaşımıyla birleştirerek beyaz altın-platin alaşımından minyatürler ve maskeler üretiyorlardı. Metal işçileri, altın eriyene kadar altını platin alaşımı taneleriyle ısıtmış ve bu noktada platin grubu metaller altın içinde bağlanmıştır. Soğuduktan sonra, ortaya çıkan yığıntı, ilgili tüm metaller birlikte eritilmiş gibi homojen hale gelene kadar tekrar tekrar dövüldü ve ısıtıldı (ilgili platin grubu metallerin erime noktalarına ulaşmak o günün teknolojisinin ötesindeydi). ⓘ
Orta Çağ
Altın hanım içindir-gümüş hizmetçi için-
Zanaatında kurnaz bir zanaatkâr için bakır.
Salonunda oturan Baron, "Güzel!" dedi,
"Ama Demir -Soğuk Demir- hepsinin efendisidir."
Rudyard Kipling'in Soğuk Demir'inden
Arap ve Ortaçağ simyacıları tüm metallerin ve maddenin, tüm metallerin babası olan ve yanıcı özelliği taşıyan kükürt ilkesi ile tüm metallerin anası olan ve sıvılık, eriyebilirlik ve uçuculuk özelliklerinin taşıyıcısı olan cıva ilkesinden oluştuğuna inanıyordu. Bu ilkeler, çoğu laboratuvarda bulunan yaygın maddeler olan kükürt ve cıva değildi. Bu teori, tüm metallerin, simya bilgisi ve yöntemleriyle geliştirilebilecek ve hızlandırılabilecek uygun ısı, sindirim, zaman ve kirleticilerin ortadan kaldırılması kombinasyonları yoluyla dünyanın bağırsaklarında altın haline gelmeye mahkum olduğu inancını güçlendirdi. ⓘ
Arsenik, çinko, antimon ve bizmut bilinmeye başlandı, ancak bunlar ilk başta yarı metaller ya da işlenemezlikleri nedeniyle piç metaller olarak adlandırıldı. Dördü de daha önceki zamanlarda doğalarının farkına varılmadan tesadüfen kullanılmış olabilir. Albertus Magnus'un 1250 yılında arsenik trisülfür ile birlikte sabunu ısıtarak arseniği bir bileşikten izole eden ilk kişi olduğuna inanılmaktadır. Saf olmadığında kırılgan olan metalik çinko, MS 1300 yılında Hindistan'da izole edilmiştir. Antimon izolasyonu için bir prosedürün ilk tanımı Vannoccio Biringuccio'nun 1540 tarihli De la pirotechnia kitabında yer almaktadır. Bizmut, Agricola tarafından De Natura Fossilium'da (yaklaşık 1546) tanımlanmıştır; bu elementlere benzerliği nedeniyle erken dönemlerde kalay ve kurşun ile karıştırılmıştır. ⓘ
Rönesans




Madencilik ve metalürji sanatları üzerine ilk sistematik metin, Vannoccio Biringuccio'nun metallerin incelenmesi, eritilmesi ve işlenmesini ele alan De la Pirotechnia (1540) adlı eseridir. ⓘ
On altı yıl sonra Georgius Agricola 1556'da De Re Metallica'yı yayınladı; bu eser madencilik, metalürji ve yardımcı sanat ve bilimlerin açık ve eksiksiz bir anlatımı olmasının yanı sıra on altıncı yüzyıl boyunca kimya endüstrisi üzerine yazılmış en büyük eser olarak nitelendirilebilir. ⓘ
De Natura Fossilium (1546) adlı eserinde bir metalin aşağıdaki tanımını vermiştir:
Metal, doğası gereği sıvı ya da biraz sert olan mineral bir cisimdir. İkincisi ateşin ısısıyla eriyebilir, ancak tekrar soğuduğunda ve tüm ısısını kaybettiğinde, tekrar sertleşir ve uygun formuna geri döner. Bu bakımdan ateşte eriyen taştan farklıdır, çünkü ateşte eriyen taş sertliğini yeniden kazansa da ilk günkü biçimini ve özelliklerini kaybeder.
Geleneksel olarak altın, gümüş, bakır, demir, kalay ve kurşun olmak üzere altı farklı metal türü vardır. Aslında başkaları da vardır, çünkü simyacılar bu konuda bizimle aynı fikirde olmasalar da civa da bir metaldir ve bizmut da öyledir. Eski Yunan yazarları bizmuttan habersizmiş gibi görünmektedir, bu nedenle Ammonius haklı olarak bizim bilmediğimiz pek çok metal, hayvan ve bitki türü olduğunu belirtmektedir. Stibium potada eritildiğinde ve rafine edildiğinde, yazarlar tarafından kurşuna atfedildiği kadar uygun bir metal olarak görülmeye hakkı vardır. Eritildiğinde belli bir kısmı kalaya eklenirse, kitapçı alaşımı elde edilir ve bu alaşımdan kağıda kitap basanlar tarafından kullanılan yazı yapılır.
Her metalin, kendisiyle karıştırılmış olan metallerden ayrıldığında koruduğu kendi biçimi vardır. Bu nedenle ne elektrum ne de Stannum [bizim kalayımızı kastetmiyor] kendi başına gerçek bir metaldir, daha ziyade iki metalin alaşımıdır. Elektrum altın ve gümüşün, Stannum ise kurşun ve gümüşün bir alaşımıdır. Yine de elektrumdan gümüş ayrılırsa geriye elektrum değil altın kalır; Stannumdan gümüş alınırsa geriye Stannum değil kurşun kalır.
Bununla birlikte, pirincin doğal bir metal olarak bulunup bulunmadığı kesin olarak tespit edilemez. Yalnızca kalamin mineralinin rengiyle renklendirilmiş bakırdan oluşan yapay pirinci biliyoruz. Yine de eğer herhangi biri çıkarılacak olursa, bu uygun bir metal olacaktır. Siyah ve beyaz bakır, kırmızı türden farklı görünmektedir.
Dolayısıyla metal, doğası gereği ya belirttiğim gibi katıdır ya da cıvık gümüş örneğinde olduğu gibi akışkandır.
Ama şimdi basit türlerle ilgili bu kadar yeter. ⓘ
Altın ve gümüşten sonra üçüncü değerli metal olan platin, İspanyol astronom Antonio de Ulloa ve meslektaşı matematikçi Jorge Juan y Santacilia tarafından 1736 ile 1744 yılları arasında Ekvador'da keşfedilmiştir. Ulloa, 1748 yılında metalin bilimsel bir tanımını yazan ilk kişiydi. ⓘ
1789'da Alman kimyager Martin Heinrich Klaproth, metalin kendisi olduğunu düşündüğü bir uranyum oksitini izole etti. Klaproth daha sonra uranyumun kaşifi olarak anıldı. Ancak 1841 yılında Fransız kimyager Eugène-Melchior Péligot ilk uranyum metali örneğini hazırladı. Henri Becquerel daha sonra 1896 yılında uranyum kullanarak radyoaktiviteyi keşfetti. ⓘ
1790'larda Joseph Priestley ve Hollandalı kimyager Martinus van Marum, metal yüzeylerin alkolün dehidrojenasyonu üzerindeki dönüştürücü etkisini gözlemledi; bu gelişme daha sonra 1831'de platin katalizör kullanılarak sülfürik asidin endüstriyel ölçekte sentezlenmesine yol açtı. ⓘ
1803 yılında seryum, İsveç'in Bastnäs şehrinde Jöns Jakob Berzelius ve Wilhelm Hisinger tarafından ve bağımsız olarak Almanya'da Martin Heinrich Klaproth tarafından keşfedilen ilk lantanit metaliydi. Lantanit metaller, 1960'larda onları birbirinden daha verimli bir şekilde ayırmak için yöntemler geliştirilinceye kadar büyük ölçüde tuhaflıklar olarak görülüyordu. Daha sonra cep telefonlarında, mıknatıslarda, lazerlerde, aydınlatmada, pillerde, katalitik dönüştürücülerde ve modern teknolojilere olanak sağlayan diğer uygulamalarda kullanım alanı buldular. ⓘ
Bu dönemde keşfedilen ve hazırlanan diğer metaller arasında kobalt, nikel, manganez, molibden, tungsten ve krom; ve platin grubu metallerinden bazıları, paladyum, osmiyum, iridyum ve rodyum yer almaktadır. ⓘ
Hafif metaller
1809'a kadar keşfedilen tüm metallerin yoğunlukları nispeten yüksekti; ağırlıkları tek başına ayırt edici bir kriter olarak kabul ediliyordu. 1809'dan itibaren sodyum, potasyum ve stronsiyum gibi hafif metaller izole edildi. Düşük yoğunlukları, metallerin doğasına ilişkin geleneksel bilgeliğe meydan okudu. Ancak kimyasal olarak metaller gibi davrandılar ve daha sonra bu şekilde kabul edildiler. ⓘ
Alüminyum 1824 yılında keşfedildi ancak 1886 yılına kadar endüstriyel büyük ölçekli bir üretim yöntemi geliştirilemedi. Alüminyum fiyatları düştü ve alüminyum 1890'larda ve 20. yüzyılın başlarında mücevherlerde, günlük eşyalarda, gözlük çerçevelerinde, optik aletlerde, sofra takımlarında ve folyoda yaygın olarak kullanılmaya başlandı. Alüminyumun diğer metallerle sert ama hafif alaşımlar oluşturma yeteneği, metalin o dönemde birçok kullanım alanı bulmasını sağladı. Birinci Dünya Savaşı sırasında, büyük hükümetler hafif ve güçlü uçak gövdeleri için büyük miktarlarda alüminyum sevkiyatı talep etti. Günümüzde elektrik enerjisi iletiminde kullanılan en yaygın metal alüminyum-iletken çelik takviyelidir. Ayrıca tamamen alüminyum alaşımlı iletken de çok kullanılmaktadır. Alüminyum, benzer dirençteki bakır kablonun yaklaşık yarısı kadar ağırlığa sahip olduğu (daha düşük özgül iletkenlik nedeniyle daha büyük çaplı olmasına rağmen) ve daha ucuz olduğu için kullanılmaktadır. Bakır geçmişte daha popülerdi ve özellikle düşük voltajlarda ve topraklama için hala kullanılmaktadır. ⓘ
Saf metalik titanyum (%99,9) ilk kez 1910 yılında hazırlanırken, 1932 yılına kadar laboratuvar dışında kullanılmamıştır. 1950'lerde ve 1960'larda Sovyetler Birliği, Soğuk Savaş ile ilgili programların bir parçası olarak titanyumun askeri ve denizaltı uygulamalarında kullanılmasına öncülük etmiştir. 1950'lerin başından itibaren titanyum, F-100 Super Sabre ve Lockheed A-12 ve SR-71 gibi uçaklardan başlayarak askeri havacılıkta, özellikle de yüksek performanslı jetlerde yaygın olarak kullanılmaya başlandı. ⓘ
Metalik skandiyum ilk kez 1937 yılında üretilmiştir. 99 saflıkta skandiyum metalinin ilk poundu 1960 yılında üretilmiştir. Alüminyum-skandiyum alaşımlarının üretimi 1971 yılında bir ABD patentini takiben başladı. Alüminyum-skandiyum alaşımları SSCB'de de geliştirilmiştir. ⓘ
Çelik Çağı

Çelik üretiminde modern çağ, hammaddesi pik demir olan Henry Bessemer'in Bessemer prosesini 1855 yılında uygulamaya koymasıyla başladı. Bessemer'in yöntemi büyük miktarlarda çeliği ucuza üretmesini sağladı ve böylece yumuşak çelik, daha önce dövme demirin kullanıldığı çoğu amaç için kullanılmaya başlandı. Gilchrist-Thomas prosesi (ya da temel Bessemer prosesi), fosforu gidermek için konvertörün bazik bir malzeme ile kaplanmasıyla Bessemer prosesinde yapılan bir iyileştirmeydi. ⓘ
Yüksek gerilme mukavemeti ve düşük maliyeti nedeniyle çelik, binalarda, altyapıda, aletlerde, gemilerde, otomobillerde, makinelerde, cihazlarda ve silahlarda kullanılan önemli bir bileşen haline geldi. ⓘ
1872 yılında İngiliz Clark ve Woods, bugün paslanmaz çelik olarak kabul edilen bir alaşımın patentini aldı. Demir-krom alaşımlarının korozyon direnci 1821 yılında Fransız metalürjist Pierre Berthier tarafından fark edilmişti. Bazı asitlerin saldırısına karşı dirençlerine dikkat çekmiş ve çatal bıçak takımlarında kullanılmalarını önermiştir. 19'uncu yüzyılın metalürji uzmanları, modern paslanmaz çeliklerin çoğunda bulunan düşük karbon ve yüksek krom kombinasyonunu üretemiyorlardı ve üretebildikleri yüksek kromlu alaşımlar da pratik olamayacak kadar kırılgandı. Paslanmaz çelik alaşımlarının sanayileşmesi 1912 yılına kadar İngiltere, Almanya ve Amerika Birleşik Devletleri'nde gerçekleşmemiştir. ⓘ
Son kararlı metalik elementler
1900 yılına gelindiğinde, atom numarası en ağır kararlı metal olan kurşundan (#82) daha düşük olan üç metal keşfedilmeyi bekliyordu: 71, 72, 75 numaralı elementler. ⓘ
Von Welsbach, 1906'da eski iterbiyumun da yeni bir element (#71) içerdiğini kanıtladı ve buna kasiyopiyum adını verdi. Urbain bunu eşzamanlı olarak kanıtladı, ancak onun örnekleri çok saf değildi ve yeni elementten sadece eser miktarda içeriyordu. Buna rağmen onun seçtiği lutesyum ismi kabul edildi. ⓘ
1908'de Ogawa, torianitte 75 elementini buldu ancak bunu 75 yerine 43 elementi olarak atadı ve nipponyum olarak adlandırdı. 1925'te Walter Noddack, Ida Eva Tacke ve Otto Berg gadolinitten ayrıldığını duyurdular ve ona bugünkü renyum adını verdiler. ⓘ
Georges Urbain 72 elementini nadir toprak kalıntılarında bulduğunu iddia ederken, Vladimir Vernadsky bağımsız olarak ortitte buldu. Her iki iddia da I. Dünya Savaşı nedeniyle doğrulanmadı ve daha sonra da doğrulanamadı, çünkü rapor ettikleri kimya şu anda hafniyum için bilinenle eşleşmiyor. Savaştan sonra, 1922'de Coster ve Hevesy, Norveç zirkonunda X-ışını spektroskopik analizi ile buldular. Hafniyum böylece keşfedilen son kararlı element oldu. ⓘ
İkinci Dünya Savaşı'nın sonunda bilim adamları, hepsi radyoaktif (kararsız) metaller olan dört post-uranyum elementi sentezlemişti: neptünyum (1940'ta), plütonyum (1940-41) ve 93 ila 96 elementlerini temsil eden küriyum ve amerikyum (1944). Bunlardan ilk ikisi sonunda doğada da bulundu. Küriyum ve amerikyum, 1945 yılında dünyanın ilk atom bombasını üreten Manhattan projesinin yan ürünleriydi. Bomba, ilk olarak yaklaşık 150 yıl önce keşfedildiği düşünülen bir metal olan uranyumun nükleer fisyonuna dayanıyordu. ⓘ
İkinci Dünya Savaşı sonrası gelişmeler
Süper alaşımlar
Fe, Ni, Co ve Cr ile daha az miktarda W, Mo, Ta, Nb, Ti ve Al kombinasyonlarından oluşan süper alaşımlar, İkinci Dünya Savaşı'ndan kısa bir süre sonra, yüksek sıcaklıklarda (650 °C'nin (1.200 °F) üzerinde) çalışan yüksek performanslı motorlarda kullanılmak üzere geliştirilmiştir. Bu koşullar altında, uzun süreler boyunca güçlerinin çoğunu korurlar ve iyi düşük sıcaklık sünekliğini korozyona veya oksidasyona karşı dirençle birleştirirler. Süper alaşımlar artık kara, deniz ve havacılık türbinleri ile kimya ve petrol tesisleri dahil olmak üzere çok çeşitli uygulamalarda bulunabilir. ⓘ
Transcurium metalleri
Dünya Savaşı'nın sonunda atom bombasının başarıyla geliştirilmesi, neredeyse tamamı metal olan ya da metal olması beklenen ve tamamı radyoaktif olan yeni elementlerin sentezlenmesine yönelik çabaların artmasına yol açmıştır. Ancak 1949 yılında, 96. elementten (küriyum) sonra 97. element (berkelyum), bir amerikyum hedefine alfa parçacıkları gönderilerek sentezlendi. 1952 yılında, ilk hidrojen bombası patlamasının enkazında 100 numaralı element (fermiyum) bulundu; ametal olan hidrojen yaklaşık 200 yıl önce bir element olarak tanımlanmıştı. 1952'den bu yana 101 (mendelevium) ila 118 (oganesson) elementleri sentezlenmiştir. ⓘ
Dökme metalik camlar
Metalik cam (amorf veya camsı metal olarak da bilinir), düzensiz atomik ölçekli bir yapıya sahip, genellikle bir alaşım olan katı bir metalik malzemedir. Saf ve alaşımlı metallerin çoğu, katı hallerinde, oldukça düzenli bir kristal yapıda düzenlenmiş atomlara sahiptir. Amorf metaller kristal olmayan cam benzeri bir yapıya sahiptir. Ancak, tipik olarak elektrik yalıtkanı olan pencere camı gibi yaygın camların aksine, amorf metaller iyi elektrik iletkenliğine sahiptir. Amorf metaller aşırı hızlı soğutma, fiziksel buhar biriktirme, katı hal reaksiyonu, iyon ışınlama ve mekanik alaşımlama gibi çeşitli yollarla üretilir. Rapor edilen ilk metalik cam 1960 yılında Caltech'te üretilen bir alaşımdır (Au75Si25). Daha yakın zamanlarda, geleneksel çelik alaşımlarının üç katı mukavemete sahip amorf çelik partileri üretilmiştir. Şu anda en önemli uygulamalar bazı ferromanyetik metalik camların özel manyetik özelliklerine dayanmaktadır. Düşük mıknatıslanma kaybı yüksek verimli transformatörlerde kullanılmaktadır. Hırsızlık kontrolü kimlik etiketleri ve diğer eşya gözetim planları, bu manyetik özellikler nedeniyle genellikle metalik camları kullanır. ⓘ
Şekil hafızalı alaşımlar
Şekil hafızalı alaşım (SMA), orijinal şeklini "hatırlayan" ve deforme olduğunda ısıtıldığında önceden deforme olmuş şekline geri dönen bir alaşımdır. Şekil hafızası etkisi ilk olarak 1932 yılında bir Au-Cd alaşımında gözlemlenmiş olsa da, bu etkinin bir Ni-Ti alaşımında tesadüfen keşfedilmesiyle 1962 yılına kadar ciddi araştırmalar yapılmamış ve ticari uygulamaların ortaya çıkması için on yıl daha geçmesi gerekmiştir. SMA'ların robotik, otomotiv, havacılık ve biyomedikal sektörlerinde uygulamaları bulunmaktadır. Ferromanyetik şekil hafızalı alaşım (FSMA) olarak adlandırılan ve güçlü manyetik alanlar altında şekil değiştiren bir başka SMA türü daha vardır. Manyetik tepki, sıcaklık kaynaklı tepkilerden daha hızlı ve daha verimli olma eğiliminde olduğu için bu malzemeler özellikle ilgi çekicidir. ⓘ
Quasicyrstalline alaşımlar

1984 yılında İsrailli kimyager Dan Shechtman, kristal yapıların yalnızca iki, üç, dört veya altı kat simetriye sahip olabileceğini söyleyen o zamanki kristalografik konvansiyonu ihlal ederek beş kat simetriye sahip bir alüminyum-manganez alaşımı buldu. Bilim camiasının tepkisinden korktuğu için, 2011 yılında Nobel Kimya Ödülü'ne layık görüldüğü sonuçları yayınlaması iki yılını aldı. Bu zamandan beri yüzlerce kuasikristal rapor edilmiş ve doğrulanmıştır. Birçok metal alaşımında (ve bazı polimerlerde) bulunurlar. Kuasikristaller en sık alüminyum alaşımlarında (Al-Li-Cu, Al-Mn-Si, Al-Ni-Co, Al-Pd-Mn, Al-Cu-Fe, Al-Cu-V, vb.) bulunur, ancak çok sayıda başka bileşim de bilinmektedir (Cd-Yb, Ti-Zr-Ni, Zn-Mg-Ho, Zn-Mg-Sc, In-Ag-Yb, Pd-U-Si, vb.) Kuasikristaller etkin bir şekilde sonsuz büyüklükte birim hücrelere sahiptir. Doğada bulunan ilk kuasikristal olan Icosahedrite Al63Cu24Fe13 2009 yılında keşfedilmiştir. Çoğu kuasikristal, düşük elektrik iletkenliği (yalıtkanlarda görülen değerlere yaklaşma) ve düşük ısı iletkenliği, yüksek sertlik, kırılganlık ve korozyona karşı direnç ve yapışmazlık özellikleri dahil olmak üzere seramik benzeri özelliklere sahiptir. Kuasikristaller ısı yalıtımı, LED'ler, dizel motorlar ve ısıyı elektriğe dönüştüren yeni malzemeler geliştirmek için kullanılmıştır. Yeni uygulamalar düşük sürtünme katsayısından ve bazı kuasikristal malzemelerin sertliğinden faydalanabilir; örneğin güçlü, dayanıklı, düşük sürtünmeli plastik dişliler yapmak için parçacıkları plastik içine gömmek gibi. Diğer potansiyel uygulamalar arasında güç dönüşümü için seçici güneş emiciler, geniş dalga boylu reflektörler ve biyouyumluluk, düşük sürtünme ve korozyon direncinin gerekli olduğu kemik onarımı ve protez uygulamaları yer almaktadır. ⓘ
Karmaşık metalik alaşımlar
Karmaşık metalik alaşımlar (CMA'lar), onlarca ila binlerce atomdan oluşan büyük birim hücreler; iyi tanımlanmış atom kümelerinin varlığı (sıklıkla ikosahedral simetriye sahip) ve kristal kafeslerinde kısmi düzensizlik ile karakterize edilen metaller arası bileşiklerdir. İki veya daha fazla metalik elementten oluşurlar, bazen metaloidler veya kalkojenitler de eklenir. Örneğin, birim hücresinde 348 sodyum atomu ve 768 kadmiyum atomu bulunan NaCd2'yi içerirler. Linus Pauling 1923 yılında NaCd2'nin yapısını tanımlamaya çalışmış, ancak 1955 yılına kadar başarılı olamamıştır. İlk başta "dev birim hücre kristalleri" olarak adlandırılan CMA'lara olan ilgi, 8. Uluslararası Kuasikristaller Konferansı'nda verilen "Yapısal Olarak Karmaşık Alaşım Fazları" adlı bir bildirinin yayınlanmasıyla 2002 yılına kadar artmamıştır. CMA'ların potansiyel uygulamaları arasında ısı yalıtımı; güneş enerjisi ile ısıtma; manyetik buzdolapları; elektrik üretmek için atık ısı kullanımı; ve askeri motorlardaki türbin kanatları için kaplamalar yer almaktadır. ⓘ
Yüksek entropili alaşımlar
AlLiMgScTi gibi yüksek entropili alaşımlar (HEA'lar) eşit veya neredeyse eşit miktarlarda beş veya daha fazla metalden oluşur. Sadece bir veya iki ana metal içeren geleneksel alaşımlarla karşılaştırıldığında, HEA'lar önemli ölçüde daha iyi mukavemet-ağırlık oranlarına, daha yüksek gerilme mukavemetine ve kırılma, korozyon ve oksidasyona karşı daha fazla dirence sahiptir. HEA'lar 1981 gibi erken bir tarihte tanımlanmış olmasına rağmen, 2010'lara kadar önemli bir ilgi görmemiştir; arzu edilen özellikler için potansiyelleri nedeniyle malzeme bilimi ve mühendisliği araştırmalarının odak noktası olmaya devam etmektedirler. ⓘ
MAX faz alaşımları
| MAX | M | A | X ⓘ |
|---|---|---|---|
| Hf2SnC | Hf | Sn | C |
| Ti4AlN3 | Ti | Al | N |
| Ti3SiC2 | Ti | Si | C |
| Ti2AlC | Ti | Al | C |
| Cr2AlC2 | Cr | Al | C |
| Ti3AlC2 | Ti | Al | C |
Bir MAX faz alaşımında, M bir erken geçiş metali, A bir A grubu elementi (çoğunlukla grup IIIA ve IVA veya grup 13 ve 14) ve X ya karbon ya da azottur. Örnekler Hf2SnC ve Ti4AlN3'tür. Bu tür alaşımlar metal ve seramiklerin en iyi özelliklerinden bazılarına sahiptir. Bu özellikler arasında yüksek elektrik ve termal iletkenlik, termal şok direnci, hasar toleransı, işlenebilirlik, yüksek elastik sertlik ve düşük termal genleşme katsayıları yer alır</ref> Mükemmel elektrik iletkenlikleri nedeniyle metalik bir parlaklığa parlatılabilirler. Mekanik testler sırasında, polikristalin Ti3SiC2 silindirlerinin oda sıcaklığında 1 GPa gerilmelere kadar tekrar tekrar sıkıştırılabildiği ve yükün kaldırılmasıyla tamamen iyileştiği bulunmuştur. Bazı MAX fazları ayrıca kimyasal saldırılara (örneğin Ti3SiC2) ve havada yüksek sıcaklıkta oksidasyona (Ti2AlC, Cr2AlC2 ve Ti3AlC2) karşı oldukça dirençlidir. MAX faz alaşımları için potansiyel uygulamalar şunları içerir: sert, işlenebilir, termal şoka dayanıklı refrakterler; yüksek sıcaklıkta ısıtma elemanları; elektrik kontakları için kaplamalar; ve nükleer uygulamalar için nötron ışınlarına dayanıklı parçalar. MAX faz alaşımları 1960'larda keşfedilmiş olsa da, konuyla ilgili ilk makale 1996 yılına kadar yayınlanmamıştır. ⓘ