Mitokondri

(1) Çekirdekçik
(2) Çekirdek
(3) Ribozomlar (küçük noktalar)
(4) Vezikül
(5) Granüllü endoplazmik retikulum (ER) (Kaba ER)
(6) Golgi aygıtı
(7) Hücre iskeleti
(8) Granülsüz endoplazmik retikulum (Düz ER)
(9) Mitokondriler
(10) Koful
(11) Sitoplazma
(12) Lizozom
(13) Sentrozom içindeki Sentriyoller ⓘ
Mitokondri, hücre organellerinden biridir. Yunanca mitos (iplik) ve khondrion (tane) sözcüklerinden türetilmiştir. Boyları 0,2-5 mikron arasında değişir. Şekilleri ise ovalden çubuğa kadar değişkenlik göstermektedir. Bazı hücreler tek bir büyük mitokondri içerebilse de mitokondriler hücrelerde çoğunlukla fazla sayılardadır. Sayıları hücrenin enerji ihtiyacına göre değişir. Özellikle kas ve sinir hücreleri gibi enerji ihtiyacı fazla olan hücrelerde çok sayıda mitokondri bulunur. Bir karaciğer hücresinde sayıları 2500 civarına ulaşabilir. ⓘ
- Bölünüp çoğalma özelliğine sahiptirler.
- Solunum sırasında monomer organik besinler,inorganik besinlere dönüşürler.
- Görevi;02 'li solunum ile ATP sentezini gerçekleştirmek
- Mitokondriler, oksijenli solunum yapan ökaryotik hücrelerde bulunur. Prokaryotik hücrelerde ve memelilerin alyuvarlarında bulunmaz.
- Solunum sırasında monomer organik besinler,inorganik besinlere dönüşürler.
- Mitokondri hücrede enerji üreten organeldir.
- Mitokondrilerin büyüklük ve şekilleri bakterilerinkiyle benzerlik gösterir.
- Kendilerine ait ribozom,DNA ve RNA ları vardır. Mitokondri ribozomları yaklaşık olarak bakteri ribozomlarının büyüklüğündedir. Mitokondriyal DNA bakterilerde olduğu gibi daireseldir.Tüm bunlar Endosimbiyoz Kuramını desteklemektedir. Endosimbiyoz Kuramına göre mitokondri bir aerob prokaryotun ökaryotik hücre içine girerek simbiyotik olarak yaşayamaya başlaması sonucu gelişmiş bir organeldir.
- Mitokondriler kloroplastlar gibi çift zara sahip organellerdir. ⓘ
Mitokondride 4 kısım vardır. Bunlar dış zar, iç zar, zarlararası (periferal) bölge ve matriksdir. Dış zar iç zara göre daha kalındır ve porin denilen taşıyıcı proteinler bulundururlar. Mitokondri içerisine girecek maddeler porinlerle alınırlar. İç zar dış zara göre daha seçici geçirgen yapıdadır. Dış ve iç zar arasındaki bölgeye periferal bölge adı verilir. İç zar mitokondri matriksine doğru girintiler yaparak krista denilen yapıları oluşturur. Kristalar kese, boru, tüpçük, zigzag gibi çeşitli şekillerde olabilirler. Kristaların mitokondri eksenine uzanma biçimleri genelde enine olmakla birlikte, boyuna ve çapraz olarak da olabilir. İç zar üzerinde solunumda görev alan ETS proteinleri bulunur. Bu sebeple enerji ihtiyacı fazla olan hücrelerin mitokondrilerindeki krista sayısı daha fazladır. İç zar üzerinde elementer partikül ( Racker partikülü) denilen yapılar vardır. Bu yapıların iç zarla bağlantılı olan bir sap bölgesi ve buna bağlı baş bölgesi vardır. Baş bölgesinde kimyasal enerjiden ATP sentezi gerçekleştiğinden bu bölgeye ATPozom ismi verilmektedir. Matrikste organel proteinlerinin 2/3'ü bulunur. ⓘ
Endosimbiyoz Kurama göre mitokondriler, uzun zaman önce, büyük hücrelere geçebilen tek canlı organizmalardı. Fakat hücre içindekilere göre enerjiyi daha verimli ayrıştırabildiklerinden dolayı içine geçtikleri hücrelere çok fayda sağladılar ve zamanla hücrelerin kalıcı birer parçası haline dönüştüler. Buna rağmen, kendi genetik bilgilerini taşır ve içinde bulundukları hücrelerden bağımsız bir şekilde bölünürler. Yani mitokondri, kendini çekirdek bilgisi dahilinde eşleyebilir. ⓘ
Mitokondriler kalıtımsal olarak yavruya annesinden geçer, babadan gelen spermlerin bu konuda yavruya hiçbir katkısı yoktur. ⓘ
| Hücre biyolojisi ⓘ | |
|---|---|
| Hayvan hücresi diyagramı | |
 Tipik bir hayvan hücresinin bileşenleri:
|
Mitokondri (/ˌmaɪtəˈkɒndriən/; çoğ. mitokondri) ökaryotik organizmaların çoğunda bulunan çift zara bağlı bir organeldir. Mitokondri, hücrenin adenozin trifosfat (ATP) kaynağının çoğunu üretmek için aerobik solunum kullanır ve bu daha sonra hücre boyunca bir kimyasal enerji kaynağı olarak kullanılır. Albert von Kölliker tarafından 1857 yılında böceklerin istemli kaslarında keşfedilmiştir. Mitokondriyon terimi 1898 yılında Carl Benda tarafından ortaya atılmıştır. Mitokondriyon, Philip Siekevitz tarafından 1957 yılında aynı adı taşıyan bir makalede kullanılan bir deyim olan "hücrenin güç merkezi" olarak adlandırılır. ⓘ
Bazı çok hücreli organizmalarda bazı hücreler mitokondriden yoksundur (örneğin, olgun memeli kırmızı kan hücreleri). Mikrosporidia, parabasalidler ve diplomonadlar gibi çok sayıda tek hücreli organizma mitokondrilerini azaltmış ya da başka yapılara dönüştürmüştür. Bir ökaryot olan Monocercomonoides'in mitokondrilerini tamamen kaybettiği ve bir çok hücreli organizma olan Henneguya salminicola'nın mitokondriyal genomlarının tamamen kaybıyla birlikte mitokondriyle ilişkili organelleri koruduğu bilinmektedir. ⓘ
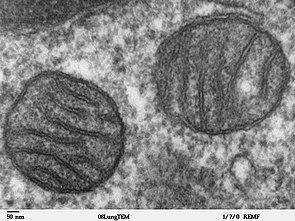
Mitokondrilerin alanı genellikle 0,75 ila 3 μm2 arasındadır, ancak boyut ve yapı bakımından önemli ölçüde değişiklik gösterir. Özel olarak boyanmadıkları sürece görünür değildirler. Mitokondri, hücresel enerji sağlamanın yanı sıra sinyal verme, hücresel farklılaşma ve hücre ölümü gibi diğer görevlerde de yer alır ve hücre döngüsünün ve hücre büyümesinin kontrolünü sağlar. Mitokondriyal biyogenez de bu hücresel süreçlerle zamansal olarak koordine edilir. Mitokondri, mitokondriyal hastalıklar, kardiyak disfonksiyon, kalp yetmezliği ve otizm gibi çeşitli insan hastalıklarında ve durumlarında rol oynar. ⓘ
Bir hücrenin DNA'sının çoğu hücre çekirdeğinde bulunmasına rağmen, mitokondriyonun bakteriyel genomlara büyük ölçüde benzeyen kendi genomu ("mitojenom") vardır. Mitokondriyal proteinler (mitokondriyal DNA'dan kopyalanan proteinler) dokuya ve türe bağlı olarak değişir. İnsanlarda, kalp mitokondrisinden 615 farklı protein türü tanımlanırken, sıçanlarda 940 protein rapor edilmiştir. Mitokondriyal proteomun dinamik olarak düzenlendiği düşünülmektedir. ⓘ
Yapı
Mitokondri bir dizi farklı şekle sahip olabilir. Bir mitokondriyon fosfolipid çift tabakalar ve proteinlerden oluşan dış ve iç zarlar içerir. Bu iki zar farklı özelliklere sahiptir. Bu çift membranlı organizasyon nedeniyle, bir mitokondriyonun beş farklı bölümü vardır:
- Dış mitokondriyal membran,
- Membranlar arası boşluk (dış ve iç membranlar arasındaki boşluk),
- İç mitokondriyal membran,
- Krista boşluğu (iç zarın katlanmasıyla oluşur) ve
- Bir sıvı olan matris (iç zar içindeki boşluk).
Mitokondriler yüzey alanını artırmak için katlanır ve bu da ATP (adenozin trifosfat) üretimini artırır. Dış zarından sıyrılmış mitokondrilere mitoplast denir. ⓘ
Dış zar
Tüm organeli çevreleyen dış mitokondriyal membran 60 ila 75 angstrom (Å) kalınlığındadır. Hücre zarına benzer bir protein-fosfolipid oranına sahiptir (ağırlıkça yaklaşık 1:1). Porin adı verilen çok sayıda integral membran proteini içerir. Önemli bir kaçakçılık proteini, gözenek oluşturan voltaja bağlı anyon kanalıdır (VDAC). VDAC, sitozol ile zarlar arası boşluk arasında nükleotidlerin, iyonların ve metabolitlerin birincil taşıyıcısıdır. Gram-negatif bakteri membranındakine benzer şekilde dış membrana yayılan bir beta fıçı olarak oluşur. Daha büyük proteinler, N-terminuslarındaki bir sinyal dizisi dış membrandaki translokaz adı verilen büyük bir multisubunit proteine bağlanırsa mitokondriyona girebilir ve bu da onları aktif olarak membran boyunca hareket ettirir. Mitokondriyal pro-proteinler özelleşmiş translokasyon kompleksleri aracılığıyla içe aktarılır. ⓘ
Dış zar ayrıca yağ asitlerinin uzaması, epinefrinin oksidasyonu ve triptofanın parçalanması gibi çeşitli faaliyetlerde yer alan enzimleri de içerir. Bu enzimler arasında monoamin oksidaz, rotenona duyarsız NADH-sitokrom c-redüktaz, kinürenin hidroksilaz ve yağ asidi Co-A ligaz bulunur. Dış zarın bozulması, zarlar arası boşluktaki proteinlerin sitozole sızmasına izin vererek hücre ölümüne yol açar. Dış mitokondriyal membran, MAM (mitokondri ile ilişkili ER-membran) adı verilen bir yapıda endoplazmik retikulum (ER) membranı ile birleşebilir. Bu, ER-mitokondri kalsiyum sinyalizasyonunda önemlidir ve ER ile mitokondri arasında lipitlerin transferinde rol oynar. Dış zarın dışında Parson'un alt birimleri olarak adlandırılan küçük (çap: 60 Å) parçacıklar bulunur. ⓘ
Membranlar arası boşluk
Mitokondriyal membranlar arası boşluk, dış membran ile iç membran arasındaki boşluktur. Perimitokondriyal boşluk olarak da bilinir. Dış membran küçük moleküllere karşı serbestçe geçirgen olduğundan, iyonlar ve şekerler gibi küçük moleküllerin intermembran boşluktaki konsantrasyonları sitozoldekiyle aynıdır. Bununla birlikte, büyük proteinlerin dış zar boyunca taşınması için belirli bir sinyal dizisine sahip olması gerekir, bu nedenle bu boşluğun protein bileşimi sitozolün protein bileşiminden farklıdır. Bu şekilde intermembran boşluğa lokalize olan bir protein sitokrom c'dir. ⓘ
İç zar
İç mitokondriyal membran üç tip fonksiyona sahip proteinler içerir:
- Elektron taşıma zinciri redoks reaksiyonlarını gerçekleştirenler
- Matrikste ATP üreten ATP sentaz
- Metabolitlerin mitokondriyal matriks içine ve dışına geçişini düzenleyen spesifik taşıma proteinleri ⓘ
151'den fazla farklı polipeptit içerir ve çok yüksek bir protein-fosfolipit oranına sahiptir (ağırlıkça 3:1'den fazla, yani 15 fosfolipit için yaklaşık 1 protein). İç zar, bir mitokondriondaki toplam proteinin yaklaşık 1/5'ine ev sahipliği yapar. Ayrıca, iç zar alışılmadık bir fosfolipid olan kardiyolipin bakımından da zengindir. Bu fosfolipid ilk olarak 1942 yılında inek kalplerinde keşfedilmiştir ve genellikle mitokondriyal ve bakteriyel plazma membranlarının karakteristik özelliğidir. Kardiyolipin iki yerine dört yağ asidi içerir ve iç zarı geçirimsiz hale getirmeye yardımcı olabilir. Dış zarın aksine, iç zar porin içermez ve tüm moleküllere karşı oldukça geçirimsizdir. Neredeyse tüm iyonlar ve moleküller matrise girmek veya matristen çıkmak için özel membran taşıyıcılarına ihtiyaç duyar. Proteinler matrikse iç membran translokaz (TIM) kompleksi veya OXA1L aracılığıyla taşınır. Buna ek olarak, iç zar boyunca elektron taşıma zinciri enzimlerinin etkisiyle oluşan bir zar potansiyeli vardır. İç membran füzyonuna iç membran proteini OPA1 aracılık eder. ⓘ
Cristae

İç mitokondriyal membran, iç mitokondriyal membranın yüzey alanını genişleterek ATP üretme kabiliyetini artıran krista adı verilen çok sayıda kıvrıma bölünmüştür. Tipik karaciğer mitokondrisi için iç zarın alanı dış zarın yaklaşık beş katıdır. Bu oran değişkendir ve kas hücreleri gibi ATP'ye daha fazla ihtiyaç duyan hücrelerin mitokondrileri daha da fazla krista içerir. Aynı hücre içindeki mitokondriler önemli ölçüde farklı krista yoğunluğuna sahip olabilir, daha fazla enerji üretmek için gerekli olanlar çok daha fazla krista-zar yüzeyine sahiptir. Bu kıvrımlar F1 partikülleri veya oksisomlar olarak bilinen küçük yuvarlak cisimlerle süslenmiştir. ⓘ
Matris
Matris, iç zar tarafından çevrelenen boşluktur. Bir mitokondriondaki toplam proteinlerin yaklaşık 2/3'ünü içerir. Matriks, iç membranda bulunan ATP sentaz yardımıyla ATP üretiminde önemlidir. Matriks, yüzlerce enzim, özel mitokondriyal ribozomlar, tRNA ve mitokondriyal DNA genomunun birkaç kopyasından oluşan yüksek konsantrasyonlu bir karışım içerir. Enzimlerin başlıca işlevleri arasında piruvat ve yağ asitlerinin oksidasyonu ve sitrik asit döngüsü yer alır. DNA molekülleri, biri TFAM olmak üzere proteinler tarafından nükleoidler halinde paketlenir. ⓘ
Fonksiyon
Mitokondrinin en belirgin rolleri, solunum yoluyla hücrenin enerji para birimi olan ATP'yi (yani ADP'nin fosforilasyonu) üretmek ve hücresel metabolizmayı düzenlemektir. ATP üretiminde yer alan merkezi reaksiyonlar topluca sitrik asit döngüsü veya Krebs döngüsü ve oksidatif fosforilasyon olarak bilinir. Bununla birlikte, mitokondriyonun ATP üretimine ek olarak başka birçok işlevi daha vardır. ⓘ
Enerji dönüşümü
Mitokondri için baskın bir rol, bu görev için iç membrandaki çok sayıda proteinin yansıttığı gibi ATP üretimidir. Bu, sitozolde üretilen başlıca glikoz ürünleri olan piruvat ve NADH'nin oksitlenmesiyle yapılır. Aerobik solunum olarak bilinen bu tür hücresel solunum, oksijenin varlığına bağlıdır. Oksijen sınırlı olduğunda, glikolitik ürünler mitokondriden bağımsız bir süreç olan anaerobik fermantasyon ile metabolize edilecektir. Glikoz ve oksijenden ATP üretimi, aerobik solunum sırasında fermantasyona kıyasla yaklaşık 13 kat daha yüksek bir verime sahiptir. Bitki mitokondrileri ayrıca fotosentez sırasında üretilen şekeri parçalayarak ya da alternatif substrat nitrit kullanarak oksijen olmadan sınırlı miktarda ATP üretebilir. ATP, spesifik bir protein yardımıyla iç zardan ve porinler aracılığıyla dış zardan geçer. ADP aynı yolla geri döner. ⓘ
Piruvat ve sitrik asit döngüsü
Glikoliz ile üretilen piruvat molekülleri iç mitokondriyal membran boyunca aktif olarak taşınır ve ya oksitlenip CO2, asetil-CoA ve NADH oluşturmak üzere koenzim A ile birleştirilebilecekleri ya da oksaloasetat oluşturmak üzere (piruvat karboksilaz tarafından) karboksile edilebilecekleri matrise taşınır. Bu son reaksiyon sitrik asit döngüsündeki oksaloasetat miktarını "doldurur" ve bu nedenle anaplerotik bir reaksiyondur, dokunun enerji ihtiyacı (örneğin kasta) aktivite ile aniden arttığında döngünün asetil-CoA'yı metabolize etme kapasitesini artırır. ⓘ
Sitrik asit döngüsünde, tüm ara ürünler (örneğin sitrat, izo-sitrat, alfa-ketoglutarat, süksinat, fumarat, malat ve oksaloasetat) döngünün her dönüşü sırasında yeniden üretilir. Bu nedenle mitokondriyona bu ara maddelerden herhangi birinin daha fazla eklenmesi, ek miktarın döngü içinde tutulduğu ve biri diğerine dönüştürülürken diğer tüm ara maddelerin arttığı anlamına gelir. Dolayısıyla, bunlardan herhangi birinin döngüye eklenmesi anaplerotik bir etkiye sahiptir ve çıkarılması kataplerotik bir etkiye sahiptir. Bu anaplerotik ve kataplerotik reaksiyonlar, döngü boyunca, sitrik asit oluşturmak üzere asetil-CoA ile birleşmek için mevcut oksaloasetat miktarını artıracak veya azaltacaktır. Bu da mitokondriyon tarafından ATP üretim oranını ve dolayısıyla hücre için ATP kullanılabilirliğini artırır veya azaltır. ⓘ
Öte yandan, piruvat oksidasyonundan veya yağ asitlerinin beta oksidasyonundan elde edilen asetil-CoA, sitrik asit döngüsüne giren tek yakıttır. Döngünün her dönüşünde mitokondriyal matrikste bulunan her bir oksaloasetat molekülü için bir asetil-CoA molekülü tüketilir ve asla yeniden üretilmez. CO2 ve su üreten asetil-CoA'nın asetat kısmının oksidasyonudur ve bu şekilde açığa çıkan enerji ATP şeklinde yakalanır. ⓘ
Karaciğerde, sitozolik piruvatın mitokondri içi okzaloasetata karboksilasyonu, kandaki yüksek glukagon ve/veya epinefrin seviyelerinin etkisi altında laktat ve de-aminlenmiş alanini glukoza dönüştüren glukoneojenik yolun erken bir adımıdır. Burada, mitokondriyona oksaloasetat eklenmesinin net bir anaplerotik etkisi yoktur, çünkü başka bir sitrik asit döngüsü ara ürünü (malat), glikolizin neredeyse tersi olan bir süreçte sitozolik oksaloasetata ve nihayetinde glikoza dönüştürülmek üzere hemen mitokondriyondan uzaklaştırılır. ⓘ
Sitrik asit döngüsünün enzimleri, Kompleks II'nin bir parçası olarak iç mitokondriyal membrana bağlı olan süksinat dehidrojenaz haricinde mitokondriyal matrikste bulunur. Sitrik asit döngüsü asetil-CoA'yı karbondioksite okside eder ve bu süreçte elektron taşıma zinciri için elektron kaynağı olan indirgenmiş kofaktörler (üç molekül NADH ve bir molekül FADH2) ve bir molekül GTP (kolayca ATP'ye dönüştürülür) üretir. ⓘ
O2 ve NADH: Enerji açığa çıkaran reaksiyonlar

NADH ve FADH2'den gelen elektronlar, bir elektron taşıma zinciri aracılığıyla birkaç adımda oksijen (O2) ve hidrojene (protonlar) aktarılır. NADH ve FADH2 molekülleri sitrik asit döngüsü yoluyla matriks içinde ve glikoliz yoluyla sitoplazmada üretilir. Sitoplazmadan indirgeyici eşdeğerler antiporter proteinlerin malat-aspartat mekik sistemi yoluyla alınabilir veya bir gliserol fosfat mekiği kullanılarak elektron taşıma zincirine beslenebilir. ⓘ
Mitokondriyonu "hücrenin güç merkezi" yapan başlıca enerji açığa çıkaran reaksiyonlar, iç mitokondriyal membrandaki protein kompleksleri I, III ve IV'te (NADH dehidrojenaz (ubikinon), sitokrom c redüktaz ve sitokrom c oksidaz) meydana gelir. Kompleks IV'te O2, sitokrom c'deki indirgenmiş demir formuyla reaksiyona girer: ⓘ
Organik bir yakıtın bağlarını koparmadan reaktanlardan çok fazla serbest enerjinin serbest bırakılması. Fe2+'den bir elektron çıkarmak için harcanan serbest enerji, sitokrom c'nin Fe3+'ü ubikinolü (QH2) oksitlemek için reaksiyona girdiğinde kompleks III'te serbest bırakılır: ⓘ
Oluşan ubikinon (Q), kompleks I içinde NADH ile reaksiyona girer: ⓘ
Reaksiyonlar bir elektron taşıma zinciri tarafından kontrol edilirken, serbest elektronlar gösterilen üç reaksiyonda reaktanlar veya ürünler arasında yer almaz ve bu nedenle protonları (H+) zarlar arası boşluğa pompalamak için kullanılan serbest enerjiyi etkilemez. Bu süreç etkilidir, ancak elektronların küçük bir yüzdesi oksijeni erken indirgeyerek süperoksit gibi reaktif oksijen türleri oluşturabilir. Bu durum mitokondride oksidatif strese neden olabilir ve yaşlanma ile ilişkili mitokondriyal fonksiyonun azalmasına katkıda bulunabilir. ⓘ
Membranlar arası boşlukta proton konsantrasyonu arttıkça, iç membran boyunca güçlü bir elektrokimyasal gradyan oluşur. Protonlar ATP sentaz kompleksi aracılığıyla matrise geri dönebilir ve potansiyel enerjileri ADP ve inorganik fosfattan (Pi) ATP sentezlemek için kullanılır. Bu süreç kemiyozmoz olarak adlandırılır ve ilk kez Peter Mitchell tarafından tanımlanmış ve bu çalışmasıyla 1978 Nobel Kimya Ödülü'ne layık görülmüştür. Daha sonra, 1997 Nobel Kimya Ödülü'nün bir kısmı, ATP sentazın çalışma mekanizmasını açıklığa kavuşturdukları için Paul D. Boyer ve John E. Walker'a verildi. ⓘ
Isı üretimi
Belirli koşullar altında protonlar, ATP sentezine katkıda bulunmadan mitokondriyal matrise yeniden girebilir. Bu süreç proton sızıntısı veya mitokondriyal ayrılma olarak bilinir ve protonların matrikse difüzyonunun kolaylaşmasından kaynaklanır. Süreç, proton elektrokimyasal gradyanının kullanılmayan potansiyel enerjisinin ısı olarak açığa çıkmasıyla sonuçlanır. Bu sürece termogenin veya UCP1 adı verilen bir proton kanalı aracılık eder. Termogenin öncelikle kahverengi yağ dokusunda veya kahverengi yağda bulunur ve titremeyen termojenezden sorumludur. Kahverengi yağ dokusu memelilerde bulunur ve yaşamın erken dönemlerinde ve kış uykusuna yatan hayvanlarda en yüksek seviyededir. İnsanlarda kahverengi yağ dokusu doğumda mevcuttur ve yaşla birlikte azalır. ⓘ
Kalsiyum iyonlarının depolanması

Hücredeki serbest kalsiyum konsantrasyonları bir dizi reaksiyonu düzenleyebilir ve hücredeki sinyal iletimi için önemlidir. Mitokondri geçici olarak kalsiyum depolayabilir, bu da hücrenin kalsiyum homeostazına katkıda bulunan bir süreçtir.
Daha sonra salınmak üzere hızla kalsiyum alma yetenekleri onları kalsiyum için iyi birer "sitozolik tampon" haline getirir. Endoplazmik retikulum (ER) kalsiyumun en önemli depolandığı yerdir ve mitokondriyon ile ER arasında kalsiyum açısından önemli bir etkileşim vardır. Kalsiyum, iç mitokondriyal membrandaki mitokondriyal kalsiyum uniporter tarafından matrikse alınır. Öncelikle mitokondriyal membran potansiyeli tarafından yönlendirilir. Bu kalsiyumun hücrenin içine geri salınması bir sodyum-kalsiyum değişim proteini veya "kalsiyum kaynaklı kalsiyum salınımı" yolları ile gerçekleşebilir. Bu, membran potansiyelinde büyük değişikliklerle kalsiyum sivri uçlarını veya kalsiyum dalgalarını başlatabilir. Bunlar, sinir hücrelerinde nörotransmitter salınımı ve endokrin hücrelerde hormon salınımı gibi süreçleri koordine edebilen bir dizi ikinci haberci sistem proteinini aktive edebilir. ⓘ
Mitokondriyal matrise Ca2+ akışı, son zamanlarda, membran boyunca elektrokimyasal potansiyelin geçici olarak ΔΨ baskınlığından pH baskınlığına "atmasına" izin vererek, oksidatif stresin azalmasını kolaylaştırarak solunum biyoenerjetiklerini düzenleyen bir mekanizma olarak gösterilmiştir. Nöronlarda, sitozolik ve mitokondriyal kalsiyumdaki eşzamanlı artışlar, nöronal aktiviteyi mitokondriyal enerji metabolizması ile senkronize etmek için hareket eder. Mitokondriyal matriks kalsiyum seviyeleri, Krebs döngüsünün temel düzenleyici enzimlerinden biri olan izositrat dehidrojenazın aktivasyonu için gerekli olan onlarca mikromolar seviyeye ulaşabilir. ⓘ
Hücresel proliferasyon düzenlemesi
Hücresel proliferasyon ve mitokondri arasındaki ilişki araştırılmıştır. Tümör hücreleri, hızlı çoğalma için lipidler, proteinler ve nükleotidler gibi biyoaktif bileşikleri sentezlemek üzere bol miktarda ATP'ye ihtiyaç duyar. Tümör hücrelerindeki ATP'nin büyük kısmı oksidatif fosforilasyon yolu (OxPhos) aracılığıyla üretilir. OxPhos ile etkileşim hücre döngüsünün durmasına neden olarak mitokondrinin hücre proliferasyonunda rol oynadığını düşündürmektedir. Mitokondriyal ATP üretimi, hücre hacmi, solüt konsantrasyonu ve hücresel mimarinin düzenlenmesi dahil olmak üzere hücredeki temel işlevlere ek olarak enfeksiyonda hücre bölünmesi ve farklılaşması için de hayati önem taşır. ATP seviyeleri hücre döngüsünün çeşitli aşamalarında farklılık gösterir, bu da ATP bolluğu ile hücrenin yeni bir hücre döngüsüne girme yeteneği arasında bir ilişki olduğunu gösterir. ATP'nin hücrenin temel işlevlerindeki rolü, hücre döngüsünü mitokondriyal kaynaklı ATP'nin mevcudiyetindeki değişikliklere duyarlı hale getirir. Hücre döngüsünün farklı aşamalarında ATP seviyelerindeki değişim, mitokondrinin hücre döngüsü düzenlemesinde önemli bir rol oynadığı hipotezini desteklemektedir. Mitokondri ve hücre döngüsü düzenlemesi arasındaki spesifik mekanizmalar iyi anlaşılmamış olsa da, çalışmalar düşük enerjili hücre döngüsü kontrol noktalarının başka bir hücre bölünmesi turuna başlamadan önce enerji kapasitesini izlediğini göstermiştir. ⓘ
Ek işlevler
Mitokondri, aşağıdakiler gibi diğer birçok metabolik görevde merkezi bir rol oynar:
- Mitokondriyal reaktif oksijen türleri aracılığıyla sinyal verme
- Membran potansiyelinin düzenlenmesi
- Apoptoz programlı hücre ölümü
- Kalsiyum sinyali (kalsiyumla uyarılmış apoptoz dahil)
- Hücresel metabolizmanın düzenlenmesi
- Bazı hem sentezi reaksiyonları (ayrıca bkz: porfirin)
- Steroid sentezi.
- Hormonal sinyal Mitokondri, kısmen mitokondriyal östrojen reseptörlerinin (mtER'ler) etkisiyle hormonlara karşı hassas ve duyarlıdır. Bu reseptörler beyin ve kalp dahil olmak üzere çeşitli dokularda ve hücre tiplerinde bulunmuştur
- Bağışıklık sinyali
- Nöronal mitokondri ayrıca özelleşmiş somatik bağlantılar aracılığıyla nöronal durumu mikroglialara bildirerek hücresel kalite kontrolüne katkıda bulunur. ⓘ
Bazı mitokondriyal işlevler yalnızca belirli hücre türlerinde gerçekleştirilir. Örneğin, karaciğer hücrelerindeki mitokondriler, protein metabolizmasının bir atık ürünü olan amonyağı detoksifiye etmelerini sağlayan enzimler içerir. Bu işlevlerden herhangi birini düzenleyen genlerdeki bir mutasyon mitokondriyal hastalıklara neden olabilir. ⓘ
Organizasyon ve dağılım

Mitokondri (veya ilgili yapılar) tüm ökaryotlarda bulunur (ikisi hariç - Oxymonad Monocercomonoides ve Henneguya salminicola). Genellikle fasulye benzeri yapılar olarak tasvir edilmelerine rağmen, hücrelerin çoğunda sürekli olarak fisyon ve füzyona uğradıkları oldukça dinamik bir ağ oluştururlar. Belirli bir hücrenin tüm mitokondri popülasyonu kondriomu oluşturur. Mitokondrilerin sayısı ve konumu hücre tipine göre değişir. Tek hücreli organizmalarda genellikle tek bir mitokondriyon bulunurken, insan karaciğer hücrelerinde hücre başına yaklaşık 1000-2000 mitokondri bulunur ve hücre hacminin 1/5'ini oluşturur. Aksi takdirde benzer hücrelerin mitokondriyal içeriği, boyut ve membran potansiyeli açısından önemli ölçüde değişebilir; farklılıklar, hücre bölünmesi sırasında eşit olmayan bölünme gibi kaynaklardan kaynaklanır ve ATP seviyelerinde ve aşağı akış hücresel süreçlerinde dışsal farklılıklara yol açar. Mitokondri, kas miyofibrilleri arasında veya sperm kamçısının etrafına sarılmış halde bulunabilir. Genellikle, hücre iskeleti ile hücre içinde karmaşık bir 3D dallanma ağı oluştururlar. Hücre iskeleti ile olan ilişki mitokondrinin şeklini belirler ve bu da işlevi etkileyebilir: mitokondriyal ağın farklı yapıları popülasyona çeşitli fiziksel, kimyasal ve sinyal avantaj veya dezavantajları sağlayabilir. Hücrelerdeki mitokondriler her zaman mikrotübüller boyunca dağılır ve bu organellerin dağılımı endoplazmik retikulum ile de ilişkilidir. Son kanıtlar, hücre iskeletinin bileşenlerinden biri olan vimentinin de hücre iskeleti ile ilişkide kritik öneme sahip olduğunu göstermektedir. ⓘ
Mitokondri ile ilişkili ER membranı (MAM)
Mitokondri ile ilişkili ER membranı (MAM), hücresel fizyoloji ve homeostazdaki kritik rolü giderek daha fazla kabul gören bir başka yapısal unsurdur. Bir zamanlar hücre fraksiyonlama tekniklerinde teknik bir engel olarak görülen, mitokondriyal fraksiyonda değişmez bir şekilde ortaya çıkan ER vezikül kontaminantları, mitokondri ve ER arasındaki arayüz olan MAM'dan türetilen membranöz yapılar olarak yeniden tanımlanmıştır. Bu iki organel arasındaki fiziksel bağlantı daha önce elektron mikrograflarında gözlemlenmiş ve daha yakın zamanda floresan mikroskobu ile incelenmiştir. Bu tür çalışmalar, mitokondriyal dış zarın %20'sine kadarını oluşturabilen MAM'da ER ve mitokondrinin sadece 10-25 nm ile ayrıldığını ve protein bağlama kompleksleri tarafından bir arada tutulduğunu tahmin etmektedir. ⓘ
Hücre altı fraksiyonlamadan elde edilen saflaştırılmış MAM, Ca2+ sinyali ile ilişkili kanallara ek olarak fosfolipid değişiminde yer alan enzimler bakımından zenginleştirilmiştir. Hücresel lipid depolarının ve sinyal iletiminin düzenlenmesinde MAM için önemli bir rolün bu ipuçları, aşağıda tartışıldığı gibi mitokondriyal ilişkili hücresel fenomenler için önemli sonuçlarla birlikte ortaya çıkmıştır. MAM, içsel apoptoz ve kalsiyum sinyalinin yayılması gibi fizyolojik süreçlerin altında yatan mekanistik temele dair içgörü sağlamakla kalmamış, aynı zamanda mitokondriye dair daha rafine bir bakış açısını da desteklemiştir. Genellikle eski bir endosimbiyotik olayla hücresel metabolizma için kaçırılmış statik, izole 'güç merkezleri' olarak görülse de, MAM'ın evrimi, mitokondrinin endomembran sistemiyle yakın fiziksel ve işlevsel bağlantı ile genel hücresel fizyolojiye ne ölçüde entegre edildiğinin altını çizmektedir. ⓘ
Fosfolipid transferi
MAM, ER yüzünde fosfatidilserin sentaz ve mitokondriyal yüzünde fosfatidilserin dekarboksilaz gibi lipid biyosentezinde yer alan enzimler bakımından zenginleşmiştir. Mitokondri sürekli olarak fisyon ve füzyon olaylarına maruz kalan dinamik organeller olduğundan, membran bütünlüğü için sürekli ve iyi düzenlenmiş bir fosfolipid kaynağına ihtiyaç duyarlar. Ancak mitokondri sadece sentezini tamamladıkları fosfolipidler için bir varış noktası değildir; aksine bu organel aynı zamanda fosfolipid biyosentetik yollarının, seramid ve kolesterol metabolizmasının ve glikosfingolipid anabolizmasının ara ürünlerinin ve ürünlerinin organeller arası trafiğinde de rol oynar. ⓘ
Bu kaçakçılık kapasitesi, organeller arasında lipid ara ürünlerinin transferini kolaylaştırdığı gösterilen MAM'a bağlıdır. Lipid transferinin standart veziküler mekanizmasının aksine, kanıtlar ER ve mitokondriyal membranların MAM'daki fiziksel yakınlığının karşıt çift katmanlar arasında lipid dönüşümüne izin verdiğini göstermektedir. Bu alışılmadık ve görünüşte enerjik olarak elverişsiz mekanizmaya rağmen, bu tür bir taşıma ATP gerektirmez. Bunun yerine, mayada, ER-mitokondri karşılaşma yapısı veya ERMES olarak adlandırılan çok proteinli bir bağlama yapısına bağlı olduğu gösterilmiştir, ancak bu yapının doğrudan lipid transferine aracılık edip etmediği veya lipid çevirme için enerji bariyerini düşürmek için membranları yeterince yakın tutmak için gerekli olup olmadığı belirsizliğini korumaktadır. ⓘ
MAM, hücre içi lipid trafiğindeki rolüne ek olarak salgı yolunun da bir parçası olabilir. Özellikle MAM, çok düşük yoğunluklu lipoprotein veya VLDL'nin bir araya gelmesine ve salgılanmasına yol açan yolda kaba ER ile Golgi arasında bir ara hedef olarak görünmektedir. Bu nedenle MAM, lipid metabolizmasında kritik bir metabolik ve kaçakçılık merkezi olarak hizmet vermektedir. ⓘ
Kalsiyum sinyali
Kalsiyum sinyalizasyonunda ER için kritik bir rol olduğu, mitokondri için böyle bir rolün yaygın olarak kabul edilmesinden önce kabul edilmiştir, çünkü dış mitokondriyal membrana lokalize olan Ca2+ kanallarının düşük afinitesi, bu organelin hücre içi Ca2+ akışındaki değişikliklere karşı iddia edilen duyarlılığı ile çelişiyor gibi görünmektedir. Ancak MAM'ın varlığı bu görünür çelişkiyi çözmektedir: iki organel arasındaki yakın fiziksel ilişki, ER'den mitokondriye etkili Ca2+ iletimini kolaylaştıran temas noktalarında Ca2+ mikro alanlarıyla sonuçlanır. İletim, kanonik bir ER membran Ca2+ kanalı olan IP3R'nin spontan kümelenmesi ve aktivasyonu ile üretilen "Ca2+ puflarına" yanıt olarak gerçekleşir. ⓘ
Bu pufların kaderi, özellikle de izole bölgelerle sınırlı kalıp kalmayacakları veya hücre boyunca yayılmak üzere Ca2+ dalgalarına entegre olup olmayacakları, büyük ölçüde MAM dinamikleri tarafından belirlenir. Ca2+'nın ER tarafından geri alımı (salınımıyla eş zamanlı olarak) pufların yoğunluğunu modüle etse de, böylece mitokondriyi yüksek Ca2+ maruziyetinden belirli bir dereceye kadar izole etse de, MAM genellikle sitozole salınan serbest iyonların içine akabileceği bir lavabo görevi görerek Ca2+ puflarını esasen tamponlayan bir güvenlik duvarı görevi görür. Bu Ca2+ tünellemesi, son zamanlarda ER membranındaki IP3R kümelerine fiziksel olarak bağlı olduğu ve MAM'da zenginleştiği gösterilen düşük afiniteli Ca2+ reseptörü VDAC1 aracılığıyla gerçekleşir. Mitokondrinin Ca2+ yutağı olarak hizmet etme kabiliyeti, oksidatif fosforilasyon sırasında oluşan elektrokimyasal gradyanın bir sonucudur, bu da katyonun tünellemesini ekzergonik bir süreç haline getirir. Sitozolden mitokondriyal matrikse normal, hafif kalsiyum akışı protonların dışarı pompalanmasıyla düzeltilen geçici depolarizasyona neden olur. ⓘ
Ancak Ca2+ iletimi tek yönlü değildir; daha ziyade iki yönlü bir yoldur. ER membranında bulunan Ca2+ pompası SERCA ve kanal IP3R'nin özellikleri, MAM işlevi tarafından koordine edilen geri besleme düzenlemesini kolaylaştırır. Özellikle, Ca2+'nın MAM tarafından temizlenmesi Ca2+ sinyalinin uzaysal-zamansal olarak düzenlenmesini sağlar çünkü Ca2+ IP3R aktivitesini iki fazlı bir şekilde değiştirir. SERCA da aynı şekilde mitokondriyal geri beslemeden etkilenir: MAM tarafından Ca2+ alımı ATP üretimini uyarır, böylece SERCA'nın MAM'da devam eden Ca2+ çıkışı için ER'yi Ca2+ ile yeniden yüklemesini sağlayan enerji sağlar. Dolayısıyla MAM, Ca2+ pufları için pasif bir tampon değildir; bunun yerine ER dinamiklerini etkileyen geri bildirim döngüleri yoluyla daha fazla Ca2+ sinyalinin modüle edilmesine yardımcı olur. ⓘ
MAM'da ER Ca2+ salınımının düzenlenmesi özellikle kritiktir çünkü sadece belirli bir Ca2+ alım penceresi mitokondriyi ve dolayısıyla hücreyi homeostazda tutar. Sitrik asit döngüsü boyunca akış için kritik olan dehidrojenaz enzimlerini aktive ederek metabolizmayı uyarmak için yeterli intraorganel Ca2+ sinyali gereklidir. Bununla birlikte, mitokondride Ca2+ sinyali belirli bir eşiği geçtiğinde, metabolizma için gerekli mitokondriyal membran potansiyelini çökertmek suretiyle kısmen apoptozun intrinsik yolunu uyarır. Pro- ve anti-apoptotik faktörlerin rolünü inceleyen çalışmalar bu modeli desteklemektedir; örneğin anti-apoptotik faktör Bcl-2'nin ER'nin Ca2+ dolumunu azaltmak için IP3R'lerle etkileşime girdiği, MAM'de akışın azalmasına yol açtığı ve apoptotik uyaranlar sonrası mitokondriyal membran potansiyelinin çökmesini önlediği gösterilmiştir. Ca2+ sinyalinin bu kadar hassas bir şekilde düzenlenmesine duyulan ihtiyaç göz önüne alındığında, düzensiz mitokondriyal Ca2+'nın çeşitli nörodejeneratif hastalıklarda rol oynaması ve tümör baskılayıcılar kataloğunun MAM'da zenginleştirilmiş birkaçını içermesi belki de şaşırtıcı değildir. ⓘ
Bağlanmanın moleküler temeli
Mitokondriyal ve ER membranları arasındaki bağların tanımlanmasındaki son gelişmeler, ilgili moleküler unsurların iskele işlevinin diğer yapısal olmayan işlevlere ikincil olduğunu göstermektedir. Mayada, ER ve mitokondriyal yerleşik membran proteinlerinin etkileşiminden oluşan çok proteinli bir kompleks olan ERMES, MAM'da lipid transferi için gereklidir ve bu prensibi örneklendirir. Örneğin bileşenlerinden biri, aynı zamanda transmembran beta-barrel proteinlerinin lipid çift tabakasına yerleştirilmesi için gerekli olan protein kompleksinin bir bileşenidir. Ancak, memeli hücrelerinde ERMES kompleksinin bir homoloğu henüz tanımlanmamıştır. İskelede yer alan diğer proteinler de aynı şekilde MAM'da yapısal bağlanmadan bağımsız işlevlere sahiptir; örneğin, ER'de yerleşik ve mitokondride yerleşik mitofusinler, organeller arası temas bölgelerinin sayısını düzenleyen heterokompleksler oluşturur, ancak mitofusinler ilk olarak ayrı mitokondriler arasındaki fisyon ve füzyon olaylarındaki rolleri nedeniyle tanımlanmıştır. Glikozla ilişkili protein 75 (grp75) bir başka çift işlevli proteindir. Grp75'in matris havuzuna ek olarak, bir kısmı MAM'de etkili Ca2+ iletimi için mitokondriyal ve ER Ca2+ kanalları VDAC ve IP3R'yi fiziksel olarak bağlayan bir şaperon görevi görür. Bir diğer potansiyel bağlayıcı, ER'de yerleşik IP3R'nin stabilizasyonunun metabolik stres tepkisi sırasında MAM'deki iletişimi koruyabileceği opioid olmayan bir reseptör olan Sigma-1R'dir. ⓘ
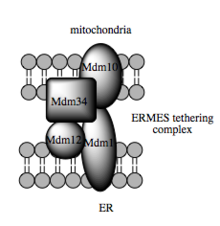
Perspektif
MAM, ER ve mitokondriyal fizyolojinin entegrasyonunu sağlayan hücredeki kritik bir sinyal, metabolik ve kaçakçılık merkezidir. Bu organeller arasındaki bağlantı sadece yapısal değil aynı zamanda işlevseldir ve genel hücresel fizyoloji ve homeostaz için kritik öneme sahiptir. Dolayısıyla MAM, mitokondri üzerine, bu organelin hücre tarafından metabolik kapasitesi için tahsis edilen statik, izole bir birim olarak geleneksel görüşünden farklı bir bakış açısı sunar. Bunun yerine, bu mitokondriyal-ER arayüzü, endosimbiyotik bir olayın ürünü olan mitokondrinin çeşitli hücresel süreçlere entegrasyonunu vurgular. Son zamanlarda, nöronlardaki mitokondri ve MAM-s'lerin özelleşmiş hücreler arası iletişim bölgelerine (somatik kavşaklar olarak adlandırılır) bağlandığı da gösterilmiştir. Mikroglial süreçler bu bölgelerdeki nöronal işlevleri izler ve korur ve MAM-s'lerin bu tür hücresel kalite kontrolünde önemli bir role sahip olduğu düşünülmektedir. ⓘ
Kökeni ve evrimi
Mitokondrinin kökeni hakkında iki hipotez vardır: endosimbiyotik ve otojen. Endosimbiyotik hipotez, mitokondrilerin başlangıçta ökaryotik hücreler için mümkün olmayan oksidatif mekanizmaları uygulayabilen prokaryotik hücreler olduğunu ve ökaryot içinde yaşayan endosimbiontlar haline geldiğini öne sürer. Otojen hipotezde mitokondri, prokaryotlarla farklılaşma sırasında DNA'nın bir kısmının ökaryotik hücrenin çekirdeğinden ayrılmasıyla doğmuştur; bu DNA kısmı proteinler tarafından geçilemeyen zarlarla çevrili olurdu. Mitokondrilerin bakterilerle birçok ortak özelliği olduğundan, endosimbiyotik hipotez daha yaygın olarak kabul görmektedir. ⓘ
Bir mitokondriyon, tek ve genellikle dairesel bir kromozomun birkaç kopyası olarak düzenlenen DNA içerir. Bu mitokondriyal kromozom, solunum zincirindekiler gibi redoks proteinleri için genler içerir. CoRR hipotezi, bu birlikte yerleşimin redoks düzenlemesi için gerekli olduğunu öne sürer. Mitokondriyal genom, ribozomların bazı RNA'larını ve mRNA'ların proteine çevrilmesi için gerekli 22 tRNA'yı kodlar. Dairesel yapı prokaryotlarda da bulunur. Proto-mitokondriyon muhtemelen Rickettsia ile yakından ilişkiliydi. Bununla birlikte, mitokondrinin atasının alfaproteobakterilerle kesin ilişkisi ve mitokondrinin çekirdekle aynı zamanda mı yoksa çekirdekten sonra mı oluştuğu tartışmalıdır. Örneğin, SAR11 bakteri kladının mitokondri ile nispeten yeni bir ortak atayı paylaştığı öne sürülürken, filogenomik analizler mitokondrinin alfaproteobakterilerle yakından ilişkili veya onların bir üyesi olan bir Pseudomonadota soyundan evrimleştiğini göstermektedir. Bazı makaleler mitokondriyi alphaproteobactera ile kardeş olarak tanımlamakta, birlikte marineproteo1 grubunun kardeşini oluşturmakta ve birlikte Magnetococcidae'nin kardeşini oluşturmaktadır. ⓘ
ⓘ| Proteobakteriler |
| ||||||||||||||||||||||||
Mitokondriyal DNA tarafından kodlanan ribozomlar, boyut ve yapı bakımından bakterilerdekilere benzer. Nükleer DNA tarafından kodlanan 80S sitoplazmik ribozomlara değil, bakteriyel 70S ribozomuna çok benzerler. ⓘ
Mitokondrilerin konak hücreleriyle endosimbiyotik ilişkisi Lynn Margulis tarafından popüler hale getirilmiştir. Endosimbiyotik hipotez, mitokondrilerin bir şekilde başka bir hücre tarafından endositozdan kurtulan ve sitoplazmaya dahil olan aerobik bakterilerden türediğini öne sürer. Bu bakterilerin, glikoliz ve fermantasyona dayanan konak hücrelerde solunum yapabilme yeteneği, önemli bir evrimsel avantaj sağlamış olabilir. Bu simbiyotik ilişki muhtemelen 1,7 ila 2 milyar yıl önce gelişmiştir. ⓘ

Birkaç tek hücreli ökaryot grubunda sadece körelmiş mitokondriler ya da türemiş yapılar bulunur: mikrosporidler, metamonadlar ve arkamoebler. Bu gruplar, rRNA bilgileri kullanılarak oluşturulan filogenetik ağaçlarda en ilkel ökaryotlar olarak görünür ve bu da bir zamanlar mitokondrinin kökeninden önce ortaya çıktıklarını düşündürmüştür. Ancak, bunun artık uzun dal çekiciliğinin bir eseri olduğu bilinmektedir - bunlar türetilmiş gruplardır ve mitokondriden türetilen genleri veya organelleri (örneğin, mitozomlar ve hidrojenozomlar) muhafaza ederler. Hidrojenozomlar, mitozomlar ve bazı loricifera (örn. Spinoloricus) ve myxozoa'da (örn. Henneguya zschokkei) bulunan ilgili organeller birlikte MRO'lar, mitokondriyle ilişkili organeller olarak sınıflandırılır. ⓘ
Monocercomonoides mitokondrilerini tamamen kaybetmiş gibi görünmektedir ve mitokondriyal işlevlerin en azından bir kısmı artık sitoplazmik proteinler tarafından yerine getiriliyor gibi görünmektedir. ⓘ
Genom

Mitokondriler kendi genomlarını içerirler. İnsan mitokondriyal genomu yaklaşık 16 kilobazlık dairesel çift sarmallı bir DNA molekülüdür. 37 gen kodlar: Solunum kompleksleri I, III, IV ve V'in alt birimleri için 13, mitokondriyal tRNA için 22 (20 standart amino asit için, ayrıca lösin ve serin için ekstra bir gen) ve rRNA için 2 (12S ve 16S rRNA). Bir mitokondriyon DNA'sının iki ila on kopyasını içerebilir. İki mitokondriyal DNA (mtDNA) ipliğinden biri orantısız olarak daha ağır nükleotid adenin ve guanin oranına sahiptir ve bu ağır iplik (veya H ipliği) olarak adlandırılırken, diğer iplik hafif iplik (veya L ipliği) olarak adlandırılır. Ağırlık farkı, iki ipliğin santrifüjleme ile ayrılmasını sağlar. mtDNA, kodlamayan bölge (NCR) olarak bilinen ve RNA transkripsiyonu için ağır iplikçik promotörü (HSP) ve hafif iplikçik promotörü (LSP), L ipliğinde lokalize olan H ipliği için replikasyon orijini (OriH), üç korunmuş sekans kutusu (CSB 1-3) ve bir sonlandırma ilişkili sekans (TAS) içeren uzun bir kodlamayan uzantıya sahiptir. L ipliği (OriL) için replikasyon orijini, tRNA'yı kodlayan bir gen kümesi içinde bulunan OriH'nin 11.000 bp aşağı akışında H ipliği üzerinde lokalizedir. ⓘ
Prokaryotlarda olduğu gibi, çok yüksek oranda kodlayıcı DNA vardır ve tekrarlar yoktur. Mitokondriyal genler, olgun mRNA'lar elde etmek için bölünen ve poliadenillenen multigenik transkriptler olarak transkribe edilir. Mitokondriyal işlev için gerekli proteinlerin çoğu hücre çekirdeğindeki genler tarafından kodlanır ve ilgili proteinler mitokondriyona aktarılır. Çekirdek ve mitokondriyal genom tarafından kodlanan genlerin tam sayısı türler arasında farklılık gösterir. Çoğu mitokondriyal genom daireseldir. Genel olarak mitokondriyal DNA, insan mitokondriyal genomunda olduğu gibi intronlardan yoksundur; ancak maya ve Dictyostelium discoideum gibi protistlerde olduğu gibi bazı ökaryotik mitokondriyal DNA'larda intronlar gözlenmiştir. Protein kodlayan bölgeler arasında tRNA'lar bulunur. Mitokondriyal tRNA genleri nükleer tRNA'lardan farklı dizilere sahiptir, ancak mitokondriyal tRNA'ların benzerleri nükleer kromozomlarda yüksek dizi benzerliği ile bulunmuştur. ⓘ
Hayvanlarda mitokondriyal genom tipik olarak yaklaşık 16 kb uzunluğunda ve 37 gene sahip tek bir dairesel kromozomdur. Genler, yüksek oranda korunmuş olsa da, konum olarak değişebilir. İlginçtir ki, bu model insan vücut bitinde (Pediculus humanus) bulunmaz. Bunun yerine, bu mitokondriyal genom, her biri 3-4 kb uzunluğunda olan ve bir ila üç gen içeren 18 mini dairesel kromozom halinde düzenlenmiştir. Bu model diğer emici bitlerde de bulunur, ancak çiğneyici bitlerde bulunmaz. Rekombinasyonun minikromozomlar arasında gerçekleştiği gösterilmiştir. ⓘ
Alternatif genetik kod
| Organizma | Kodon | Standart | Mitokondri |
|---|---|---|---|
| Memeliler | AGA, AGG | Arginin | Dur kodonu |
| Omurgasızlar | AGA, AGG | Arginin | Serin |
| Mantarlar | CUA | Lösin | Threonine |
| Yukarıdakilerin hepsi | AUA | İzolösin | Metiyonin |
| UGA | Dur kodonu | Triptofan |
Standart genetik kod üzerinde küçük varyasyonlar daha önce tahmin edilmiş olsa da, insan mitokondriyal genlerini inceleyen araştırmacıların alternatif bir kod kullandıklarını belirledikleri 1979 yılına kadar hiçbiri keşfedilmemiştir. Bununla birlikte, çoğu bitki de dahil olmak üzere diğer birçok ökaryotun mitokondrisi standart kodu kullanmaktadır. O zamandan beri çeşitli alternatif mitokondriyal kodlar da dahil olmak üzere birçok küçük varyant keşfedilmiştir. Ayrıca, AUA, AUC ve AUU kodonlarının hepsi izin verilen başlangıç kodonlarıdır. ⓘ
Bu farklılıklardan bazıları, mitokondride yaygın olan RNA düzenleme olgusu nedeniyle genetik kodda sözde değişiklikler olarak kabul edilmelidir. Yüksek bitkilerde, CGG'nin arginin değil triptofan kodladığı düşünülüyordu; ancak, işlenmiş RNA'daki kodonun triptofan için standart genetik kodla tutarlı olarak UGG kodonu olduğu keşfedildi. Eklembacaklı mitokondriyal genetik kodunun bir filum içinde paralel bir evrim geçirdiği ve bazı organizmaların AGG'yi lizine benzersiz bir şekilde çevirdiği de not edilmelidir. ⓘ
Çoğaltma ve kalıtım
Mitokondri, bakteriler tarafından da yapılan ikili fisyonun bir şekli olan mitokondriyal fisyon ile bölünür, ancak süreç ev sahibi ökaryotik hücre tarafından sıkı bir şekilde düzenlenir ve diğer birkaç organel arasında iletişim ve temas içerir. Bu bölünmenin düzenlenmesi ökaryotlar arasında farklılık gösterir. Birçok tek hücreli ökaryotta büyüme ve bölünme hücre döngüsüyle bağlantılıdır. Örneğin, tek bir mitokondriyon çekirdek ile eşzamanlı olarak bölünebilir. Bu bölünme ve ayrılma süreci, her yavru hücrenin en az bir mitokondriyon alması için sıkı bir şekilde kontrol edilmelidir. Diğer ökaryotlarda (örneğin memelilerde) mitokondriler DNA'larını kopyalayabilir ve hücre döngüsüyle aynı fazda değil, esas olarak hücrenin enerji ihtiyaçlarına yanıt olarak bölünebilir. Bir hücrenin enerji ihtiyacı yüksek olduğunda, mitokondri büyür ve bölünür. Enerji kullanımı düşük olduğunda, mitokondriler yok edilir veya inaktif hale gelir. Bu tür örneklerde mitokondri, sitoplazmanın bölünmesi sırasında yavru hücrelere rastgele dağılmış gibi görünür. Mitokondriyal dinamikler, mitokondriyal füzyon ve fisyon arasındaki denge, çeşitli hastalık durumlarıyla ilişkili patolojilerde önemli bir faktördür. ⓘ
Mitokondriyal ikili fisyon hipotezi, floresan mikroskobu ve geleneksel transmisyon elektron mikroskobu (TEM) ile görselleştirmeye dayanmaktadır. Floresan mikroskobunun çözünürlüğü (~200 nm), mitokondriyal bölünmede çift mitokondriyal membran gibi yapısal ayrıntıları ayırt etmek veya hatta birkaçı birbirine yakın olduğunda tek tek mitokondrileri ayırt etmek için yetersizdir. Geleneksel TEM de mitokondriyal bölünmeyi doğrulamada bazı teknik sınırlamalara sahiptir. Kriyo-elektron tomografi yakın zamanda dondurulmuş hidratlı sağlam hücrelerde mitokondriyal bölünmeyi görselleştirmek için kullanılmıştır. Mitokondrinin tomurcuklanma yoluyla bölündüğü ortaya çıkmıştır. ⓘ
Bir bireyin mitokondriyal genleri, nadir istisnalar dışında yalnızca anneden miras alınır. İnsanlarda, bir yumurta hücresi bir sperm tarafından döllendiğinde, mitokondri ve dolayısıyla mitokondriyal DNA genellikle sadece yumurtadan gelir. Spermin mitokondrisi yumurtaya girer, ancak embriyoya genetik bilgi katkısında bulunmaz. Bunun yerine, baba mitokondrisi, embriyo içinde daha sonra yok edilmek üzere seçilmeleri için ubikitin ile işaretlenir. Yumurta hücresi nispeten az sayıda mitokondri içerir, ancak bu mitokondriler bölünerek yetişkin organizmanın hücrelerini doldurur. Bu mod, hayvanların çoğunluğu da dahil olmak üzere çoğu organizmada görülür. Bununla birlikte, bazı türlerde mitokondri bazen babadan miras kalabilir. Bu, çam ağaçları ve porsuklarda olmasa da bazı iğne yapraklı bitkiler arasında bir normdur. Mytilidlerde babadan kalıtım sadece türün erkeklerinde görülür. İnsanlarda bunun çok düşük bir seviyede gerçekleştiği öne sürülmüştür. ⓘ
Tek ebeveynli kalıtım, farklı mitokondri soyları arasında genetik rekombinasyon için çok az fırsata yol açar, ancak tek bir mitokondriyon DNA'sının 2-10 kopyasını içerebilir. Gerçekleşen rekombinasyon, çeşitliliği korumaktan ziyade genetik bütünlüğü korur. Bununla birlikte, mitokondriyal DNA'da rekombinasyonun kanıtlarını gösteren çalışmalar vardır. Rekombinasyon için gerekli enzimlerin memeli hücrelerinde mevcut olduğu açıktır. Ayrıca, kanıtlar hayvan mitokondrilerinin rekombinasyona uğrayabileceğini göstermektedir. Rekombinasyonun dolaylı kanıtları mevcut olsa da, veriler insanlarda daha tartışmalıdır. ⓘ
Tek ebeveynli kalıtım geçiren ve rekombinasyonun çok az olduğu veya hiç olmadığı varlıkların, işlevsellik kaybolana kadar zararlı mutasyonların birikmesi olan Muller'in cırcırına maruz kalması beklenebilir. Mitokondrili hayvan popülasyonları, mtDNA darboğazı olarak bilinen gelişimsel bir süreç sayesinde bu birikimden kaçınır. Darboğaz, bir organizma geliştikçe mutant yükünde hücreden hücreye değişkenliği artırmak için hücredeki stokastik süreçlerden yararlanır: belirli bir oranda mutant mtDNA içeren tek bir yumurta hücresi, böylece farklı hücrelerin farklı mutant yüklerine sahip olduğu bir embriyo üretir. Hücre düzeyinde seçilim daha sonra daha fazla mutant mtDNA'ya sahip hücreleri ortadan kaldırarak nesiller arasında mutant yükünde bir stabilizasyona veya azalmaya yol açabilir. Darboğazın altında yatan mekanizma tartışılmaktadır; yakın zamanda yapılan bir matematiksel ve deneysel metastud çalışması, hücre bölünmelerinde mtDNA'ların rastgele bölünmesi ve hücre içinde mtDNA moleküllerinin rastgele dönüşümünün bir kombinasyonuna dair kanıtlar sunmaktadır. ⓘ
DNA onarımı
Mitokondri, hücre çekirdeğinde meydana gelenlere benzer mekanizmalarla oksidatif DNA hasarını onarabilir. MtDNA onarımında kullanılan proteinler nükleer genler tarafından kodlanır ve mitokondriye transloke edilir. Memeli mitokondrisindeki DNA onarım yolları baz eksizyon onarımı, çift sarmal kırılma onarımı, doğrudan tersine çevirme ve uyumsuzluk onarımını içerir. Alternatif olarak, DNA hasarı translesiyon sentezi ile onarılmak yerine bypass edilebilir. ⓘ
Mitokondrideki çeşitli DNA onarım süreçleri arasında, baz eksizyon onarım yolu en kapsamlı şekilde incelenmiştir. Baz eksizyon onarımı, hasarlı bir DNA bazının tanınması ve eksizyonu, ortaya çıkan abazik bölgenin çıkarılması, uç işleme, boşluk doldurma ve ligasyonu içeren bir dizi enzim katalizli adımla gerçekleştirilir. MtDNA'da baz eksizyon onarımı ile onarılan yaygın bir hasar, guaninin oksidasyonu ile üretilen 8-oksoguanindir. ⓘ
Çift iplikli kırıklar hem memeli mtDNA'sında hem de bitki mtDNA'sında homolog rekombinasyonel onarım ile onarılabilir. mtDNA'daki çift sarmal kırıkları ayrıca mikrohomoloji aracılı uç birleştirme ile de onarılabilir. mtDNA'da doğrudan tersine çevirme ve uyumsuzluk onarımı süreçleri için kanıtlar olmasına rağmen, bu süreçler iyi karakterize edilmemiştir. ⓘ
Mitokondriyal DNA eksikliği
Bazı organizmalar mitokondriyal DNA'yı tamamen kaybetmiştir. Bu durumlarda, mitokondriyal DNA tarafından kodlanan genler kaybolmuş ya da çekirdeğe aktarılmıştır. Cryptosporidium, muhtemelen tüm genleri kaybolduğu veya aktarıldığı için herhangi bir DNA'ya sahip olmayan mitokondrilere sahiptir. Cryptosporidium'da mitokondri, paraziti siyanür, azid ve atovaquone gibi birçok klasik mitokondriyal inhibitöre dirençli hale getiren değiştirilmiş bir ATP üretim sistemine sahiptir. Kendi DNA'larına sahip olmayan mitokondriler, Amoebophyra cinsinden bir deniz paraziti olan dinoflagellatta bulunmuştur. Bu mikroorganizma, A. cerati, genomu olmayan işlevsel mitokondrilere sahiptir. İlgili türlerde, mitokondriyal genom hala üç gene sahiptir, ancak A. cerati'de sadece tek bir mitokondriyal gen - sitokrom c oksidaz I geni (cox1) - bulunur ve bu gen çekirdeğin genomuna göç etmiştir. ⓘ
Popülasyon genetiği çalışmaları
Mitokondriyal DNA'da genetik rekombinasyonun neredeyse hiç olmaması, onu popülasyon genetiği ve evrimsel biyoloji çalışmaları için yararlı bir bilgi kaynağı haline getirmektedir. Tüm mitokondriyal DNA tek bir birim veya haplotip olarak kalıtıldığından, farklı bireylerden gelen mitokondriyal DNA arasındaki ilişkiler bir gen ağacı olarak temsil edilebilir. Bu gen ağaçlarındaki örüntüler, popülasyonların evrimsel geçmişini çıkarmak için kullanılabilir. Bunun klasik örneği, mitokondriyal Havva için yakın bir tarih sağlamak üzere moleküler saatin kullanılabildiği insan evrimsel genetiğidir. Bu genellikle modern insanın Afrika'dan yakın zamanda yayıldığına dair güçlü bir destek olarak yorumlanmaktadır. Bir başka insan örneği de Neandertal kemiklerinden elde edilen mitokondriyal DNA'nın sıralanmasıdır. Neandertallerin ve yaşayan insanların mitokondriyal DNA dizileri arasındaki nispeten büyük evrimsel mesafe, Neandertaller ve modern insanlar arasında melezleşme olmadığının kanıtı olarak yorumlanmıştır. ⓘ
Ancak mitokondriyal DNA sadece bir popülasyondaki dişilerin geçmişini yansıtır. Bu durum, Y-kromozomunun rekombinasyon yapmayan bölgesi gibi baba genetik dizilerinin kullanılmasıyla kısmen aşılabilir. ⓘ
Mitokondriyal DNA için moleküler saatin son ölçümleri, insanların ve maymunların en son ortak atasına kadar uzanan her 7884 yılda 1 mutasyon değerini bildirmiştir; bu da otozomal DNA'nın mutasyon oranlarının tahminleriyle tutarlıdır (nesil başına baz başına 10-8). ⓘ
İşlev bozukluğu ve hastalık
Mitokondriyal hastalıklar
Hücre metabolizmasındaki etkileri nedeniyle mitokondrideki hasar ve ardından gelen işlev bozukluğu, bir dizi insan hastalığında önemli bir faktördür. Mitokondriyal bozukluklar genellikle otizm de dahil olmak üzere nörolojik bozukluklar olarak ortaya çıkar. Ayrıca miyopati, diyabet, çoklu endokrinopati ve çeşitli diğer sistemik bozukluklar olarak da ortaya çıkabilirler. mtDNA'daki mutasyonun neden olduğu hastalıklar arasında Kearns-Sayre sendromu, MELAS sendromu ve Leber'in kalıtsal optik nöropatisi yer alır. Vakaların büyük çoğunluğunda, zigot mitokondrisini ve dolayısıyla mtDNA'sını yumurtadan aldığı için bu hastalıklar bir kadın tarafından çocuklarına aktarılır. Kearns-Sayre sendromu, Pearson sendromu ve ilerleyici dış oftalmopleji gibi hastalıkların büyük ölçekli mtDNA yeniden düzenlemelerine bağlı olduğu düşünülürken, MELAS sendromu, Leber'in kalıtsal optik nöropatisi, MERRF sendromu ve diğerleri gibi diğer hastalıkların mtDNA'daki nokta mutasyonlarına bağlı olduğu düşünülmektedir. ⓘ
Ayrıca, ilaca toleranslı kanser hücrelerinin mitokondri sayısında ve boyutunda artış olduğu ve bunun da mitokondriyal biyogenezde bir artışa işaret ettiği bildirilmiştir. İlginç bir şekilde, Nature Nanotechnology'de yakın zamanda yapılan bir çalışma, kanser hücrelerinin fiziksel tünelleme nanotüpleri aracılığıyla bağışıklık hücrelerinden mitokondriyi kaçırabileceğini bildirmiştir. ⓘ
Diğer hastalıklarda, nükleer genlerdeki kusurlar mitokondriyal proteinlerin işlevsizliğine yol açar. Friedreich ataksisi, kalıtsal spastik parapleji ve Wilson hastalığında durum böyledir. Bu hastalıklar, diğer genetik hastalıkların çoğunda olduğu gibi baskınlık ilişkisi içinde kalıtılır. Koenzim Q10 eksikliği ve Barth sendromu gibi oksidatif fosforilasyon enzimlerinin nükleer mutasyonları çeşitli bozukluklara neden olabilir. Çevresel etkiler kalıtsal yatkınlıklarla etkileşime girebilir ve mitokondriyal hastalığa neden olabilir. Örneğin, pestisit maruziyeti ile Parkinson hastalığının daha geç başlaması arasında bir bağlantı olabilir. Mitokondriyal disfonksiyonu içeren etiyolojiye sahip diğer patolojiler arasında şizofreni, bipolar bozukluk, demans, Alzheimer hastalığı, Parkinson hastalığı, epilepsi, inme, kardiyovasküler hastalık, kronik yorgunluk sendromu, retinitis pigmentosa ve diabetes mellitus bulunur. ⓘ
Mitokondri aracılı oksidatif stres, tip 2 diyabet hastalarında kardiyomiyopatide rol oynar. Kalbe artan yağ asidi iletimi, kardiyomiyositler tarafından yağ asidi alımını artırarak bu hücrelerde yağ asidi oksidasyonunun artmasına neden olur. Bu süreç mitokondrinin elektron taşıma zinciri için mevcut indirgeyici eşdeğerleri artırır ve sonuçta reaktif oksijen türleri (ROS) üretimini artırır. ROS, ayrışma proteinlerini (UCP'ler) artırır ve adenin nükleotid translokatörü (ANT) yoluyla proton sızıntısını güçlendirir, bunların kombinasyonu mitokondriyi ayrıştırır. Ayrılma daha sonra mitokondri tarafından oksijen tüketimini artırarak yağ asidi oksidasyonundaki artışı artırır. Bu da bir kısır döngü yaratır; ayrıca oksijen tüketimi artsa da mitokondriler ayrılmadığı için ATP sentezi orantılı olarak artmaz. Daha az ATP kullanılabilirliği, sonuçta azalmış kardiyak verimlilik ve kontraktil disfonksiyon olarak ortaya çıkan bir enerji açığı ile sonuçlanır. Sorunu daha da karmaşık hale getirmek için, bozulmuş sarkoplazmik retikulum kalsiyum salınımı ve azalmış mitokondriyal geri alım, kas kasılması sırasında önemli sinyal iyonunun pik sitozolik seviyelerini sınırlar. Azalan mitokondriyal kalsiyum konsantrasyonu dehidrojenaz aktivasyonunu ve ATP sentezini artırır. Dolayısıyla, yağ asidi oksidasyonuna bağlı düşük ATP sentezine ek olarak, ATP sentezi de zayıf kalsiyum sinyali ile bozulur ve diyabet hastalarında kalp sorunlarına neden olur. ⓘ
Yaşlanma ile ilişkiler
Reaktif oksijen türleri oluşturmak için solunum zincirinde aktarılan elektronlarda bir miktar sızıntı olabilir. Bu durumun mitokondriyal DNA'da yüksek mutasyon oranları ile mitokondride önemli oksidatif strese yol açtığı düşünülmektedir. Yaşlanma ve oksidatif stres arasında varsayılan bağlantılar yeni değildir ve 1956'da önerilmiş ve daha sonra mitokondriyal serbest radikal yaşlanma teorisine dönüştürülmüştür. Oksidatif stres mitokondriyal DNA mutasyonlarına yol açtığından ve bu da enzimatik anormalliklere ve daha fazla oksidatif strese yol açabileceğinden bir kısır döngü oluştuğu düşünülmüştür. ⓘ
Yaşlanma sürecinde mitokondride bir dizi değişiklik meydana gelebilir. Yaşlı insanlardan alınan dokular, solunum zinciri proteinlerinin enzimatik aktivitesinde bir azalma gösterir. Bununla birlikte, mutasyona uğramış mtDNA çok yaşlı hücrelerin yalnızca yaklaşık %0,2'sinde bulunabilir. Mitokondriyal genomdaki büyük delesyonların Parkinson hastalığında yüksek düzeyde oksidatif strese ve nöronal ölüme yol açtığı varsayılmıştır. Mitokondriyal disfonksiyonun amiyotrofik lateral sklerozda da ortaya çıktığı gösterilmiştir. ⓘ
Mitokondri, germinal vezikülden olgun oosite gelişim için gerekli ATP'yi sağlayarak yumurtalık fonksiyonunda çok önemli bir rol oynadığından, mitokondri fonksiyonunun azalması inflamasyona yol açarak erken yumurtalık yetmezliği ve hızlandırılmış yumurtalık yaşlanması ile sonuçlanabilir. Ortaya çıkan işlev bozukluğu daha sonra kantitatif (mtDNA kopya sayısı ve mtDNA delesyonları gibi), kalitatif (mutasyonlar ve iplikçik kırılmaları gibi) ve oksidatif hasara (ROS'a bağlı işlevsiz mitokondri gibi) yansır, bunlar sadece yumurtalık yaşlanmasıyla ilgili değildir, aynı zamanda yumurtalıkta oosit-kümülüs çapraz iletişimini bozar, genetik bozukluklarla (Fragile X gibi) bağlantılıdır ve embriyo seçimine müdahale edebilir. ⓘ
Tarihçe
Muhtemelen mitokondriyi temsil eden hücre içi yapılara ilişkin ilk gözlemler 1857 yılında fizyolog Albert von Kolliker tarafından yayımlanmıştır. Richard Altmann, 1890'da bunları hücre organelleri olarak tanımlamış ve "biyoblast" olarak adlandırmıştır. 1898 yılında Carl Benda, Yunanca μίτος, mitos, "iplik" ve χονδρίον, chondrion, "granül" kelimelerinden "mitokondri" terimini türetmiştir. Leonor Michaelis 1900 yılında Janus yeşilinin mitokondri için supravital bir boya olarak kullanılabileceğini keşfetmiştir. 1904 yılında Friedrich Meves, beyaz nilüfer Nymphaea alba'nın hücrelerinde bitkilerde mitokondrinin kaydedilen ilk gözlemini yaptı ve 1908 yılında Claudius Regaud ile birlikte protein ve lipid içerdiklerini öne sürdü. Benjamin F. Kingsbury, 1912'de bunları ilk kez hücre solunumu ile ilişkilendirdi, ancak neredeyse sadece morfolojik gözlemlere dayanıyordu. 1913 yılında, Otto Heinrich Warburg tarafından kobay karaciğeri ekstraktlarından elde edilen ve "grana" olarak adlandırılan partiküller solunumla ilişkilendirilmiştir. Warburg ve Heinrich Otto Wieland, benzer bir partikül mekanizması öne sürmüş olsalar da solunumun kimyasal doğası konusunda anlaşmazlığa düşmüşlerdir. David Keilin'in sitokromları keşfettiği 1925 yılına kadar solunum zinciri tanımlanmamıştı. ⓘ
1939 yılında kıyılmış kas hücreleri kullanılarak yapılan deneyler, bir oksijen molekülü kullanılarak yapılan hücresel solunumun dört adenozin trifosfat (ATP) molekülü oluşturabildiğini göstermiş ve 1941 yılında ATP'nin fosfat bağlarının hücresel metabolizmada bir enerji biçimi olduğu kavramı Fritz Albert Lipmann tarafından geliştirilmiştir. Takip eden yıllarda, mitokondri ile bağlantısı bilinmemesine rağmen, hücresel solunumun arkasındaki mekanizma daha da detaylandırıldı. Albert Claude tarafından doku fraksiyonlama yönteminin kullanılmaya başlanması, mitokondrilerin diğer hücre fraksiyonlarından izole edilmesine ve biyokimyasal analizlerin yalnızca bunlar üzerinde yapılmasına olanak sağlamıştır. 1946 yılında, sitokrom oksidaz ve solunum zincirinden sorumlu diğer enzimlerin mitokondride izole edildiği sonucuna vardı. Eugene Kennedy ve Albert Lehninger 1948'de mitokondrinin ökaryotlarda oksidatif fosforilasyon bölgesi olduğunu keşfetti. Zaman içinde fraksiyonlama yöntemi daha da geliştirilerek izole edilen mitokondrilerin kalitesi artırıldı ve hücre solunumunun diğer unsurlarının mitokondride gerçekleştiği belirlendi. ⓘ
İlk yüksek çözünürlüklü elektron mikrografları 1952 yılında ortaya çıktı ve mitokondriyi görselleştirmenin tercih edilen yolu olarak Janus Green boyalarının yerini aldı. Bu, mitokondrinin bir zarla çevrili olduğunun doğrulanması da dahil olmak üzere mitokondrinin yapısının daha ayrıntılı bir şekilde analiz edilmesine yol açtı. Ayrıca mitokondrinin içinde, iç odayı bölen çıkıntılar halinde katlanan ikinci bir zar olduğunu ve mitokondrinin boyut ve şeklinin hücreden hücreye değiştiğini gösterdi. ⓘ
Popüler "hücrenin güç merkezi" terimi 1957 yılında Philip Siekevitz tarafından ortaya atılmıştır. ⓘ
1967'de mitokondrinin ribozom içerdiği keşfedildi. 1968'de mitokondriyal genlerin haritalanması için yöntemler geliştirildi ve 1976'da maya mitokondriyal DNA'sının genetik ve fiziksel haritası tamamlandı. ⓘ







