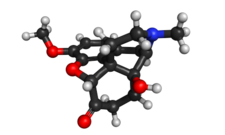
Oxycodone
 | |
 | |
| Klinik veriler | |
|---|---|
| Telaffuz | ɒksɪˈkəʊdəʊn |
| Ticari isimler | OxyContin, Endone, diğerleri |
| Diğer isimler | Eukodal, eucodal; dihidrohidroksikodeinon, 7,8-dihidro-14-hidroksikodeinon, 6-deoksi-7,8-dihidro-14-hidroksi-3-O-metil-6-oksomorfin |
| AHFS/Drugs.com | Monografi |
| MedlinePlus | a682132 |
| Lisans verileri |
|
| Hamilelik Kategori |
|
| Bağımlılık sorumluluk | Yüksek |
| Güzergahları YÖNETİM | Ağız yoluyla, dilaltı, kas içi, damar içi, burun içi, deri altı, transdermal, rektal, epidural |
| ATC kodu |
|
| Yasal statü | |
| Yasal statü |
|
| Farmakokinetik veriler | |
| Biyoyararlanım | Ağız yoluyla: %60-87 |
| Protein bağlama | 45% |
| Metabolizma | Karaciğer: esas olarak CYP3A ve çok daha az oranda CYP2D6 (~%5); %95 metabolize olur (yani, %5 değişmeden atılır) |
| Metabolitler | - Noroksikodon (%25) - Noroksimorfon (%15, serbest ve konjuge) - Oksimorfon (%11, konjuge) - Diğerleri (örn. minör metabolitler) |
| Etki başlangıcı | IR: 10-30 dakika CR: 1 saat |
| Eliminasyon yarı ömrü | Ağız yoluyla (IR): 2-3 saat (tüm ROA'lar için aynı t1/2) Ağız yoluyla (CR): 4,5 saat |
| Etki süresi | Ağız yoluyla (IR): 3-6 saat Ağız yoluyla (CR): 10-12 saat |
| Boşaltım | İdrar (%83) |
| Tanımlayıcılar | |
IUPAC adı
| |
| CAS Numarası | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Kimyasal ve fiziksel veriler | |
| Formül | C18H21NO4 |
| Molar kütle | 315.369 g-mol-1 |
| 3D model (JSmol) | |
| Erime noktası | 219 °C (426 °F) |
| Suda çözünürlük | 166 (HCl) |
GÜLÜMSEMELER
| |
InChI
| |
| (doğrulayın) | |
Diğerlerinin yanı sıra Roxicodone ve OxyContin (uzatılmış salım formu) markaları altında satılan oksikodon, orta ila şiddetli ağrı tedavisinde kullanılan yarı sentetik bir opioid ilaçtır. Oldukça bağımlılık yapıcıdır ve yaygın bir kötüye kullanım ilacıdır. Genellikle ağız yoluyla alınır ve hemen salınımlı ve kontrollü salınımlı formülasyonları mevcuttur. Ağrı kesici başlangıcı tipik olarak on beş dakika içinde başlar ve hemen salınımlı formülasyon ile altı saate kadar sürer. Birleşik Krallık'ta enjeksiyon yoluyla temin edilebilir. Parasetamol (asetaminofen), ibuprofen, nalokson, naltrekson ve aspirin ile kombinasyon ürünleri de mevcuttur. ⓘ
Yaygın yan etkiler arasında öfori, kabızlık, bulantı, kusma, iştah kaybı, uyuşukluk, baş dönmesi, kaşıntı, ağız kuruluğu ve terleme yer alır. Şiddetli yan etkiler arasında bağımlılık ve bağımlılık, madde kötüye kullanımı, sinirlilik, depresyon veya mani, deliryum, halüsinasyonlar, hipoventilasyon, gastroparezi, bradikardi ve hipotansiyon yer alabilir. Kodeine alerjisi olanlar oksikodona da alerjik olabilir. Gebeliğin erken dönemlerinde oksikodon kullanımı nispeten güvenli görünmektedir. Hızlı bir şekilde kesilirse opioid yoksunluğu oluşabilir. Oksikodon μ-opioid reseptörünü aktive ederek etki eder. Ağız yoluyla alındığında, eşdeğer miktardaki morfinin yaklaşık 1,5 katı etkiye sahiptir. ⓘ
Oksikodon ilk olarak 1916 yılında Almanya'da thebaine'den üretilmiştir. Dünya Sağlık Örgütü'nün Temel İlaçlar Listesi'nde yer almaktadır. Jenerik bir ilaç olarak mevcuttur. 2019 yılında, 14 milyondan fazla reçete ile Amerika Birleşik Devletleri'nde en sık reçete edilen 49. ilaç olmuştur. Nalokson veya naltrekson ile kombinasyon gibi bir dizi kötüye kullanım caydırıcı formülasyon mevcuttur. ⓘ

Oxycodone çok güçlü bir ağrı kesici olup genellikle ameliyat sonrası için verilir. Kırmızı reçete ile satılır. Bağımlılık yapabilir ve baş dönmesi gibi yan etkileri vardır. Böbrek taşı, sistit, bel ağrısı gibi durumlarda da kullanılır. Tebain'den sentez edilir. Kodein'e benzer fakat daha fazla bağımlılık yapma potansiyeline sahiptir. Ağız yoluyla ve Percodan gibi diğer ilaçlarla karıştırılarak ağrı kesici olarak kullanılır. Araç ve makine kullanımını etkiler. ⓘ
Tıbbi kullanımlar
Oksikodon, diğer tedaviler yeterli olmadığında orta ila şiddetli akut veya kronik ağrıyı yönetmek için kullanılır. Belirli ağrı türlerinde yaşam kalitesini artırabilir. Kronik ağrıda kullanımının yaşam kalitesinde iyileşme veya sürekli ağrı kesici ile sonuçlanıp sonuçlanmadığı belirsizdir. ⓘ
Oksikodon, her 12 saatte bir alınması amaçlanan kontrollü salımlı tablet olarak mevcuttur. İlacın üreticisi Purdue Pharma'dan bağımsız olarak Temmuz 1996'da yapılan bir çalışmada, kontrollü salım formülasyonunun 10 ila 12 saat arasında değişen değişken bir etki süresine sahip olduğu bulunmuştur. 2006 yılında yapılan bir incelemede, kontrollü salımlı oksikodonun orta ve şiddetli kanser ağrılarının tedavisinde hemen salımlı oksikodon, morfin ve hidromorfon ile karşılaştırılabilir olduğu ve morfinden daha az yan etkiye sahip olduğu bulunmuştur. Yazar, kontrollü salınımlı formun morfine geçerli bir alternatif ve kanser ağrısı için ilk basamak tedavi olduğu sonucuna varmıştır. 2014 yılında Avrupa Palyatif Bakım Derneği, kanser ağrısı için ağızdan morfine ikinci basamak alternatif olarak ağızdan oksikodonu önermiştir. ⓘ
ABD'de, uzatılmış salımlı oksikodon on bir yaşından küçük çocuklarda kullanım için onaylanmıştır. Onaylanan kullanım alanları, halihazırda opioidlerle tedavi edilen ve günde en az 20 mg oksikodonu tolere edebilen çocuklarda kanser ağrısı, travma ağrısı veya majör cerrahiye bağlı ağrının giderilmesidir; bu, çocuklar için onaylanan diğer tek uzatılmış salımlı opioid analjezik olan Duragesic'e (fentanil) bir alternatif sağlar. ⓘ
Mevcut formlar
Oksikodon ağızdan veya dil altından kullanılmak üzere çeşitli formülasyonlarda mevcuttur:
- Hemen salınan oksikodon (OxyFast, OxyIR, OxyNorm, Roxicodone)
- Kontrollü salınımlı oksikodon (OxyContin, Xtampza ER) - 10-12 saat süreli
- Oksikodon kurcalamaya dayanıklı (OxyContin OTR)
- Parasetamol (asetaminofen) ile birlikte hemen salınan oksikodon (Percocet, Endocet, Roxicet, Tylox)
- Aspirin ile hemen salınan oksikodon (Endodan, Oxycodan, Percodan, Roxiprin)
- İbuprofen ile birlikte hemen salınımlı oksikodon (Combunox)
- Naloksonlu kontrollü salımlı oksikodon (Targin, Targiniq, Targinact) - 10-12 saat süreli
- Naltrekson ile kontrollü salınımlı oksikodon (Troxyca) - 10-12 saat süreli ⓘ

ABD'de oksikodon sadece ağız yoluyla kullanım için onaylanmıştır, tabletler ve oral solüsyonlar olarak mevcuttur. Bununla birlikte, oksikodonun parenteral formülasyonları (marka adı OxyNorm) dünyanın diğer bölgelerinde de mevcuttur ve Avrupa Birliği'nde yaygın olarak kullanılmaktadır. İspanya, Hollanda ve Birleşik Krallık'ta oksikodon intravenöz (IV) ve intramüsküler (IM) kullanım için onaylanmıştır. Birinci Dünya Savaşı sırasında Almanya'da ilk kez kullanılmaya başlandığında, oksikodonun hem IV hem de IM uygulamaları Orta Güçler askerlerinin ameliyat sonrası ağrı tedavisi için yaygın olarak kullanılmıştır. ⓘ
Yan etkileri
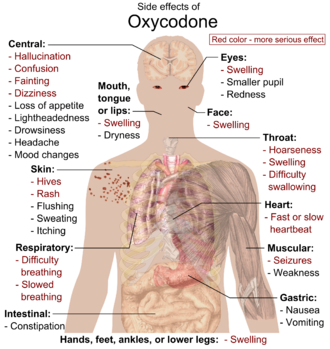
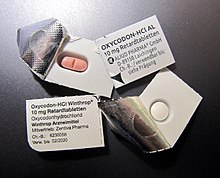
Oksikodonun en yaygın yan etkileri arasında ağrıya karşı duyarlılığın azalması, mide boşalmasının gecikmesi, öfori, anksiyoliz, rahatlama hissi ve solunum depresyonu yer alır. Oksikodonun yaygın yan etkileri arasında kabızlık (%23), bulantı (%23), kusma (%12), uyuklama (%23), baş dönmesi (%13), kaşıntı (%13), ağız kuruluğu (%6) ve terleme (%5) bulunmaktadır. Daha az görülen yan etkiler (hastaların %5'inden azında görülür) arasında iştahsızlık, sinirlilik, karın ağrısı, ishal, idrar retansiyonu, nefes darlığı ve hıçkırık yer alır. Çoğu yan etki genellikle zaman içinde daha az yoğun hale gelir, ancak kabızlıkla ilgili sorunların kullanım süresi boyunca devam etmesi muhtemeldir. Yönetilen salımlı tabletlerde nalokson ile birlikte oksikodon, hem kötüye kullanımı caydırmak hem de "opioid kaynaklı kabızlığı" azaltmak için formüle edilmiştir. ⓘ
Bağımlılık ve yoksunluk
Bir hasta fiziksel olarak bağımlı hale gelmişse ve oksikodonu aniden keserse şiddetli yoksunluk belirtileri yaşama riski yüksektir. Tıbbi olarak, ilaç uzun bir süre boyunca düzenli olarak alındığında, aniden değil kademeli olarak geri çekilir. Düzenli olarak eğlence amaçlı veya reçete edilenden daha yüksek dozlarda oksikodon kullanan kişilerde şiddetli yoksunluk belirtileri görülme riski daha da yüksektir. Oksikodon yoksunluğunun belirtileri, diğer opioidlerde olduğu gibi, "anksiyete, panik atak, bulantı, uykusuzluk, kas ağrısı, kas güçsüzlüğü, ateş ve diğer grip benzeri semptomları" içerebilir. ⓘ
Yoksunluk belirtileri, anneleri hamilelik sırasında oksikodon enjekte eden veya oral yolla alan yenidoğanlarda da bildirilmiştir. ⓘ
Hormon seviyeleri
Diğer opioidlerde olduğu gibi, oksikodonun kronik kullanımı (özellikle yüksek dozlarda) sıklıkla eş zamanlı hipogonadizme (düşük cinsiyet hormonu seviyeleri) neden olur. ⓘ
Aşırı Doz
Yüksek dozlarda, aşırı dozda veya opioidlere toleransı olmayan bazı kişilerde oksikodon sığ solunuma, kalp atış hızının yavaşlamasına, soğuk/nemli cilde, solunumun durmasına, düşük kan basıncına, göz bebeklerinin daralmasına, dolaşımın çökmesine, solunumun durmasına ve ölüme neden olabilir. ⓘ
2011 yılında ABD'de uyuşturucuya bağlı ölümlerin önde gelen nedeniydi. Ancak 2012'den itibaren eroin ve fentanil uyuşturucuya bağlı ölümlerin daha yaygın nedenleri haline gelmiştir. ⓘ
Oksikodon doz aşımının yüksek dozlarda omurilik enfarktüsüne ve baskılanmış solunumdan kaynaklanan uzun süreli hipoksiye bağlı olarak beyinde iskemik hasara neden olduğu da tanımlanmıştır. ⓘ
Etkileşimler
Oksikodon CYP3A4 ve CYP2D6 enzimleri tarafından metabolize edilir. Bu nedenle, klerensi bu enzimlerin inhibitörleri ve indükleyicileri tarafından değiştirilebilir, sırasıyla yarı ömrü artırabilir ve azaltabilir. (CYP3A4 ve CYP2D6 inhibitörleri ve indükleyicilerinin listeleri için sırasıyla buraya ve buraya bakınız). Bu enzimlerdeki doğal genetik varyasyon da oksikodonun klerensini etkileyebilir, bu da yarılanma ömrü ve etki gücündeki bireyler arası geniş değişkenlikle ilgili olabilir. ⓘ
Ritonavir veya lopinavir/ritonavir, CYP3A4 ve CYP2D6 inhibisyonu nedeniyle sağlıklı insan gönüllülerde oksikodonun plazma konsantrasyonlarını büyük ölçüde artırır. Rifampisin, CYP3A4'ün güçlü indüksiyonu nedeniyle oksikodonun plazma konsantrasyonlarını büyük ölçüde azaltır. Bir CYP3A4 indükleyicisi olan fosfenitoinin kronik ağrılı bir hastada oksikodonun analjezik etkilerini önemli ölçüde azalttığına dair bir vaka raporu da bulunmaktadır. Her vakada dozaj veya ilaç ayarlamaları gerekli olabilir. ⓘ
Farmakoloji
Farmakodinamik
| Bileşik | Yakınlıklar (Ki) | Oran | Ref. | ||
|---|---|---|---|---|---|
| MOR | DOR | KOR | MOR:DOR:KOR | ||
| Oksikodon | 18 nM | 958 nM | 677 nM | 1:53:38 | |
| Oksimorfon | 0,78 nM | 50 nM | 137 nM | 1:64:176 | |
| Bileşik | Rota | Doz |
|---|---|---|
| Kodein | PO | 200 mg |
| Hidrokodon | PO | 20-30 mg |
| Hidromorfon | PO | 7,5 mg |
| Hidromorfon | IV | 1,5 mg |
| Morfin | PO | 30 mg |
| Morfin | IV | 10 mg |
| Oksikodon | PO | 20 mg |
| Oksikodon | IV | 10 mg |
| Oksimorfon | PO | 10 mg |
| Oksimorfon | IV | 1 mg |
Yarı sentetik bir opioid olan oksikodon, μ-opioid reseptörünün (MOR) oldukça seçici bir tam agonistidir. Bu, endojen opioid nöropeptid β-endorfinin ana biyolojik hedefidir. Oksikodon, benzer şekilde agonist olduğu δ-opioid reseptörü (DOR) ve κ-opioid reseptörü (KOR) için düşük afiniteye sahiptir. Oksikodon MOR'a bağlandıktan sonra, üretilen cAMP miktarını azaltarak, kalsiyum kanallarını kapatarak ve potasyum kanallarını açarak hücre tarafından nörotransmitterlerin salınımını engelleyen bir G protein kompleksi salınır. Oksikodon gibi opioidlerin analjezik etkilerini orta beyin periaqueductal gri (PAG) ve rostral ventromedial medullada (RVM) MOR'un aktivasyonu yoluyla ürettiği düşünülmektedir. Tersine, ventral tegmental alan, nükleus akumbens ve ventral pallidum dahil olmak üzere mezolimbik ödül yolundaki MOR'un aktivasyonu yoluyla ödül ve bağımlılık ürettikleri düşünülmektedir. Opioidlerin analjezik ve ödüllendirici etkilerine tolerans karmaşıktır ve reseptör düzeyinde tolerans (örn. MOR downregülasyonu), hücresel düzeyde tolerans (örn. cAMP upregülasyonu) ve sistem düzeyinde tolerans (örn. ΔFosB ekspresyonunun indüksiyonuna bağlı nöral adaptasyon) nedeniyle oluşur. ⓘ
Ağızdan alınan 20 mg hemen salınımlı oksikodonun analjezik etki açısından 30 mg morfine eşdeğer olduğu düşünülürken, uzatılmış salınımlı oksikodonun oral morfinden iki kat daha güçlü olduğu düşünülmektedir. ⓘ
Diğer opioidlerin çoğuna benzer şekilde, oksikodon prolaktin salgısını artırır, ancak testosteron seviyeleri üzerindeki etkisi bilinmemektedir. Morfinin aksine, oksikodon immünosupresif aktiviteye sahip değildir (in vitro doğal öldürücü hücre aktivitesi ve interlökin 2 üretimi ile ölçülür); bunun klinik önemi açıklığa kavuşturulmamıştır. ⓘ
Aktif metabolitler
Oksikodonun birkaç metabolitinin de MOR agonistleri olarak aktif olduğu bulunmuştur; bunlardan bazıları MOR'a kıyasla çok daha yüksek afiniteye (ve aynı zamanda daha yüksek etkinliğe) sahiptir. Oksimorfon, MOR için oksikodondan 3 ila 5 kat daha yüksek afiniteye sahipken, noroksikodon ve noroksimorfon MOR için sırasıyla üçte bir ve 3 kat daha yüksek afiniteye sahiptir ve MOR aktivasyonu noroksikodon ile 5 ila 10 kat daha azdır, ancak oksikodona göre noroksimorfon ile 2 kat daha yüksektir. Noroksikodon, noroksimorfon ve oksimorfon ayrıca oksikodondan daha uzun biyolojik yarı ömre sahiptir. ⓘ
| Bileşik | Ki | EC50 | Cmaks | AUC |
|---|---|---|---|---|
| Oksikodon | 16.0 nM | 343 nM | 23,2 ± 8,6 ng/mL | 236 ± 102 ng/h/mL |
| Oksimorfon | 0,36 nM | 42,8 nM | 0,82 ± 0,85 ng/mL | 12,3 ± 12 ng/h/mL |
| Noroksikodon | 57,1 nM | 1930 nM | 15,2 ± 4,5 ng/mL | 233 ± 102 ng/h/mL |
| Noroksimorfon | 5,69 nM | 167 nM | ND | ND |
| Ki [3H] diprenorfin yer değiştirmesi içindir. (Diprenorfinin seçici olmayan bir opioid reseptör ligandı olduğuna dikkat edin, bu nedenle bu MOR'a özgü değildir). EC50, hMOR1 GTPyS bağlanması içindir. Cmax ve AUC seviyeleri 20 mg CR oksikodon içindir. | ||||
Bununla birlikte, bazı metabolitlerinin daha yüksek in vitro aktivitesine rağmen, oral ve intravenöz uygulamayı takiben analjezik etkisinin sırasıyla %83,0 ve %94,8'inden oksikodonun kendisinin sorumlu olduğu belirlenmiştir. Oksimorfon, oral ve intravenöz uygulamadan sonra oksikodonun analjezik etkisinin sırasıyla %15,8 ve %4,5'inden sorumlu olarak yalnızca küçük bir rol oynamaktadır. CYP2D6 genotipi ve uygulama yolu farklı oranlarda oksimorfon oluşumuna neden olsa da, değişmemiş ana bileşik oksikodonun genel analjezik etkisine en büyük katkıyı yapan bileşik olmaya devam etmektedir. Oksikodon ve oksimorfonun aksine, noroksikodon ve noroksimorfon da güçlü MOR agonistleri olmakla birlikte, kan-beyin bariyerini merkezi sinir sistemine zayıf bir şekilde geçer ve bu nedenle karşılaştırıldığında yalnızca minimal düzeyde analjeziktir. ⓘ
κ-opioid reseptörü
1997'de bir grup Avustralyalı araştırmacı (sıçanlarda yapılan bir çalışmaya dayanarak) oksikodonun, MOR'lar üzerinde etkili olan morfinin aksine KOR'lar üzerinde etkili olduğunu öne sürmüştür. Bu grup tarafından yapılan daha ileri araştırmalar, ilacın yüksek afiniteli bir κ2b-opioid reseptör agonisti gibi göründüğünü göstermiştir. Ancak bu sonuca, öncelikle oksikodonun MOR agonistlerine özgü etkiler ürettiği gerekçesiyle itiraz edilmiştir. 2006 yılında bir Japon grup tarafından yapılan araştırma, oksikodonun etkisine farklı durumlarda farklı reseptörlerin aracılık ettiğini öne sürmüştür. Özellikle diyabetik farelerde KOR, oksikodonun antinosiseptif etkilerinde rol oynarken, diyabetik olmayan farelerde μ1-opioid reseptörü bu etkilerden birincil olarak sorumlu gibi görünmektedir. ⓘ
Farmakokinetik
Anında salınan emilim profili
Oksikodon oral, intranazal, intravenöz, intramüsküler veya subkutan enjeksiyon yoluyla veya rektal olarak uygulanabilir. Oksikodonun oral yolla uygulanmasının biyoyararlanımı ortalama %60 ila %87 aralığındadır ve rektal yolla uygulama da aynı sonuçları verir; intranazal yolla uygulama ise ortalama %46 ile bireyler arasında farklılık gösterir. ⓘ
Bir doz geleneksel (hemen salınımlı) oral oksikodondan sonra, etki başlangıcı 10 ila 30 dakikadır ve ilacın en yüksek plazma seviyelerine yaklaşık 30 ila 60 dakika içinde ulaşılır; bunun aksine, bir doz OxyContin'den (oral kontrollü salınımlı bir formülasyon) sonra, oksikodonun en yüksek plazma seviyeleri yaklaşık üç saat içinde ortaya çıkar. Anında salınan oksikodonun etki süresi 3 ila 6 saattir, ancak bu süre kişiye göre değişebilir. ⓘ
Dağıtım
Oksikodon 2,6L/kg dağılım hacmine sahiptir, kanda iskelet kası, karaciğer, bağırsak sistemi, akciğerler, dalak ve beyne dağılır. Denge halinde beyindeki bağlanmamış konsantrasyon kandaki bağlanmamış konsantrasyondan üç kat daha fazladır Geleneksel oral preparatlar aç karnına 10 ila 15 dakika içinde ağrıyı azaltmaya başlar; buna karşılık OxyContin bir saat içinde ağrıyı azaltmaya başlar. ⓘ
Metabolizma
İnsanlarda oksikodonun metabolizması karaciğerde esas olarak sitokrom P450 sistemi aracılığıyla gerçekleşir ve birçok minör yol ve ortaya çıkan metabolitlerle kapsamlı (yaklaşık %95) ve karmaşıktır. Bir doz oksikodonun yaklaşık %10'u (%8-14 aralığında) idrarla esasen değişmeden (konjuge olmadan veya konjuge olarak) atılır. Oksikodonun başlıca metabolitleri noroksikodon (%70), noroksimorfon ("nispeten yüksek konsantrasyonlar") ve oksimorfondur (%5). Oksikodonun insanlardaki ani metabolizması aşağıdaki gibidir:
- Ağırlıklı olarak CYP3A4 aracılığıyla noroksikodona N-Demetilasyon
- Ağırlıklı olarak CYP2D6 üzerinden oksimorfona O-Demetilasyon
- 6-6α- ve 6β-oksikodole ketoredüksiyon
- Oksikodon-N-okside N-Oksidasyon ⓘ
İnsanlarda, oksikodonun CYP3A4 tarafından noroksikodona N-demetilasyonu, bir oksikodon dozunun %45 ± %21'ini oluşturan ana metabolik yoldur; oksikodonun CYP2D6 tarafından oksimorfona O-demetilasyonu ve oksikodonun 6-oksikodollere 6-ketoredüksiyonu, sırasıyla bir oksikodon dozunun %11 ± %6 ve %8 ± %6'sını oluşturan nispeten küçük metabolik yolları temsil eder. ⓘ
Oksikodonun acil metabolitlerinin birçoğu daha sonra glukuronik asit ile konjuge edilir ve idrarla atılır. 6α-Oksikodol ve 6β-oksikodol, N-demetilasyon yoluyla sırasıyla nor-6α-oksikodol ve nor-6β-oksikodole ve N-oksidasyon yoluyla 6α-oksikodol-N-oksit ve 6β-oksikodol-N-okside (daha sonra glukuronidasyona da uğrayabilir) metabolize olur. Oksimorfon ayrıca aşağıdaki gibi metabolize olur:
- 3-Oksimorfon-3-glukuronide glukuronidasyon ağırlıklı olarak UGT2B7 aracılığıyla
- 6α-oksimorfol ve 6β-oksimorfole ketoredüksiyon
- Noroksimorfona N-Demetilasyon ⓘ
Yukarıdaki üç yoldan ilki oksimorfon metabolizmasının %40'ını oluşturarak oksimorfon-3-glukuronidi oksimorfonun ana metaboliti haline getirirken, son iki yol oksimorfon metabolizmasının %10'undan azını oluşturur. Oksimorfonun N-demetilasyonundan sonra, noroksimorfon ayrıca noroksimorfon-3-glukuronide glukuronidlenir. ⓘ
Oksikodon karaciğerde sitokrom P450 sistemi tarafından metabolize edildiğinden, farmakokinetiği genetik polimorfizmler ve bu sistemle ilgili ilaç etkileşimlerinin yanı sıra karaciğer fonksiyonundan da etkilenebilir. Bazı insanlar oksikodonu hızlı metabolize ederken, diğerleri yavaş metabolize eder ve bu da göreceli analjezi ve toksisitede polimorfizme bağlı değişikliklere neden olur. Yüksek CYP2D6 aktivitesi oksikodonun etkilerini artırırken (oksimorfona dönüşümün artması nedeniyle), yüksek CYP3A4 aktivitesi ters etkiye sahiptir ve oksikodonun etkilerini azaltır (noroksikodon ve noroksimorfona metabolizmanın artması nedeniyle). Karaciğer fonksiyonu azalmış hastalarda oksikodon dozu azaltılmalıdır. ⓘ
Eliminasyon
Oksikodonun klerensi 0,8 L/dk'dır. Oksikodon ve metabolitleri esas olarak idrarla atılır. Bu nedenle, oksikodon böbrek yetmezliği olan hastalarda birikir. Oksikodon idrarla %10 oranında değişmemiş oksikodon, %45 ± %21 oranında N-demetillenmiş metabolitler (noroksikodon, noroksimorfon, noroksikodoller), %11 ± %6 oranında O-demetillenmiş metabolitler (oksimorfon, oksimorfoller) ve %8 ± %6 oranında 6-keto-redükte metabolitler (oksikodoller) olarak atılır. ⓘ
Etki süresi
Oksikodonun yarılanma ömrü 4,5 saattir. Jenerik bir ilaç olarak mevcuttur. Oksikodonun kontrollü salımlı bir preparatı olan OxyContin'in üreticisi Purdue Pharma, 1992 patent başvurusunda OxyContin'in etki süresinin "hastaların %90'ında" 12 saat olduğunu iddia etmiştir. OxyContin'in daha sık aralıklarla verildiği herhangi bir klinik çalışma gerçekleştirmemiştir. Purdue ayrı bir başvuruda, kontrollü salımlı oksikodonun "uygulamadan sonra en az 12 saat boyunca söz konusu hastada ağrı kesici sağladığını" iddia etmektedir. Ancak 2016 yılında Los Angeles Times tarafından yapılan bir araştırma, "ilacın birçok kişide saatler öncesinden etkisini yitirdiğini", opiat yoksunluğu semptomlarına ve OxyContin için yoğun isteklere neden olduğunu ortaya koymuştur. Lawrence Robbins adlı bir doktor gazetecilere hastalarının %70'inden fazlasının OxyContin'in sadece 4-7 saat rahatlama sağladığını bildirdiğini söylemiştir. 1990'lardaki doktorlar, OxyContin'in etki süresinin günde sadece iki kez alınamayacak kadar kısa olduğundan şikayet eden hastalarını genellikle sekiz saatte bir doz programına geçiriyorlardı. ⓘ
Purdue bu uygulamayı kesinlikle tavsiye etmemiştir: Purdue'nun tıbbi direktörü Robert Reder 1995 yılında bir doktora "OxyContin [12 saatlik] dozlama için geliştirilmiştir... [8 saatlik] dozlama rejimi kullanmamanızı rica ediyorum" diye yazmıştır. Purdue, satış temsilcilerine doktorlara 12 saatlik dozaj programından sapmamalarını hatırlatmalarını emreden notları defalarca yayınlamıştır. Bu notlardan birinde şöyle yazıyordu: "OxyContin ile Q8 dozajı yoktur... [8 saatlik dozajın] kökünden kesilmesi gerekiyor. ŞİMDİ!!" Soruşturmayı haberleştiren gazeteciler, Purdue Pharma'nın, aksi yöndeki kanıtlara rağmen, OxyContin'in 12 saatlik bir ilaç olarak itibarını ve morfin gibi jenerik opiatlara kıyasla yüksek maliyetine rağmen sağlık sigortası ve yönetilen bakım şirketlerinin OxyContin'i karşılama istekliliğini korumak için neredeyse tüm hastalar için 12 saatlik etki süresinde ısrar ettiğini savundu. ⓘ
Purdue satış temsilcilerine doktorları daha sık dozlama yerine daha büyük 12 saatlik dozlar için reçete yazmaya teşvik etmeleri talimatı verildi. Ağustos 1996'da Tennessee'deki Purdue satış temsilcilerine gönderilen "$$$$$$$$$$$$$ It's Bonus Time in the Neighborhood!" başlıklı bir notta, temsilcilerin doktorları daha yüksek dozlarda reçete yazmaya ikna etmede başarılı olmaları halinde komisyonlarının önemli ölçüde artacağı hatırlatılıyordu. Los Angeles Times muhabirleri, opioid bağımlılığı uzmanlarıyla yaptıkları röportajlara dayanarak, 12 saat arayla verilen bu kadar yüksek OxyContin dozlarının, opiat yoksunluğu sırasında acı veren bir kombinasyon yarattığını (daha düşük düşükler) ve bu acıyı hafifleten ve bağımlılığı teşvik eden bir takviye programı oluşturduğunu iddia ediyor. ⓘ
Kimya
Oksikodonun kimyasal adı kodeinden türetilmiştir. Kimyasal yapıları çok benzerdir, tek farkları ⓘ
- Oksikodonun karbon-14'te bir hidroksi grubu vardır (kodeinin yerinde sadece bir hidrojen vardır)
- Oksikodon 7,8-dihidro özelliğine sahiptir. Kodein bu iki karbon arasında bir çift bağa sahiptir; ve
- Oksikodon, kodeinin hidroksil grubu yerine bir karbonil grubuna (ketonlarda olduğu gibi) sahiptir. ⓘ
Aynı zamanda hidrokodona benzer, tek farkı karbon-14'te bir hidroksil grubuna sahip olmasıdır. ⓘ
Biyosentez
Biyosentez açısından, oksikodon, orkide ailesi Epipactis helleborine'den elde edilen nektar özlerinde doğal olarak bulunmuştur; başka bir opioid ile birlikte: 3-{2-{3-{3-benzyloxypropyl}-3-indol, 7,8-didehydro- 4,5-epoxy-3,6-d-morphinan. ⓘ
Biyolojik sıvılarda tespit
Oksikodon ve/veya başlıca metabolitleri, klerensi, tıbbi olmayan kullanımı izlemek, zehirlenme tanısını doğrulamak veya tıbbi bir ölüm soruşturmasına yardımcı olmak için kanda veya idrarda ölçülebilir. Birçok ticari opiyat tarama testi oksikodon ve metabolitleri ile kayda değer ölçüde çapraz reaksiyon verir, ancak kromatografik teknikler oksikodonu diğer opiyatlardan kolayca ayırt edebilir. ⓘ
Tarihçe
Almanya'daki Frankfurt Üniversitesi'nden Martin Freund ve (Jakob) Edmund Speyer, 1916 yılında tebainden ilk oksikodon sentezini yayınladı. Freund 1920'de öldüğünde Speyer onun ölüm ilanını yazdı. 1878'de Frankfurt am Main'de Yahudi bir ailenin çocuğu olarak dünyaya gelen Speyer, Holokost'un kurbanı oldu. Lodz Gettosu'ndan sürgünlerin ikinci günü olan 5 Mayıs 1942'de öldü; ölümü gettonun kayıtlarına geçti. ⓘ
İlacın ilk klinik kullanımı, ilk geliştirilmesinden bir yıl sonra, 1917'de belgelenmiştir. ABD pazarına ilk kez Mayıs 1939'da sunulmuştur. 1928'in başlarında Merck, skopolamin, oksikodon ve efedrin içeren bir kombinasyon ürününü SEE bileşenlerinin Almanca baş harfleri altında tanıttı ve daha sonra 1942'de Scophedal (SCOpolamine, ePHEDrine ve eukodAL) olarak yeniden adlandırıldı. En son 1987'de üretilmiştir, ancak bileşik haline getirilebilir. Bu kombinasyon esasen morfin bazlı "alacakaranlık uykusunun" bir oksikodon analoğudur ve dolaşım ve solunum etkilerini azaltmak için efedrin eklenmiştir. İlaç Kıta Avrupası'nda ve başka yerlerde "1930'ların Mucize İlacı" olarak tanındı ve bir süre Wehrmacht'ın savaş alanı analjeziği için tercihi oldu. İlaç, patent başvurusu ve prospektüsünde "çok derin analjezi ve derin ve yoğun öfori" sağlamanın yanı sıra ameliyat ve savaş alanı yaralanma vakaları için yararlı olan sakinleştirme ve anterograd amnezi sağlamak üzere açıkça tasarlanmıştı. İddiaya göre bu ürün için morfin, hidromorfon ve hidrokodon yerine oksikodon seçilmiştir çünkü oksikodonun yan etki profilinde kokaine benzer subjektif unsurlar bulunmaktadır. ⓘ
Himmler Operasyonu sırasında Skophedal'in, 1 Eylül 1939'da İkinci Dünya Savaşı'nı başlatan olayda Polonya Ordusu üniforması giymiş mahkumlara aşırı dozda enjekte edildiği de bildirilmiştir. ⓘ
Adolf Hitler'in doktoru Theodor Morell'in kişisel notları, Hitler'in "eukodal" (oksikodon) ve Scophedal'in yanı sıra Dolantin (pethidin) kodein ve daha seyrek olarak morfin enjeksiyonlarını tekrar tekrar aldığını göstermektedir; oksikodon Ocak 1945'in sonlarından sonra elde edilememiştir. ⓘ
1970'lerin başında ABD hükümeti oksikodonu II. derece uyuşturucu olarak sınıflandırmıştır. ⓘ
Stamford, Connecticut merkezli özel bir şirket olan Purdue Pharma, reçeteli ağrı kesici OxyContin'i geliştirdi. OxyContin 1995 yılında piyasaya sürüldüğünde, orta ila şiddetli ağrıları olan hastalara yardımcı olabilecek uzun süreli bir narkotik olan tıbbi bir atılım olarak selamlandı. İlaç gişe rekorları kırdı ve Purdue için yaklaşık 35 milyar ABD doları gelir elde ettiği bildirildi. ⓘ
Opioid salgını
Oksikodon, diğer opioid analjezikler gibi, ara sıra kullananlarda öfori, rahatlama ve azalmış anksiyete duygularına neden olma eğilimindedir. Bu etkileri onu Amerika Birleşik Devletleri'nde en sık suistimal edilen farmasötik ilaçlardan biri haline getirmektedir. Yönlendirilmiş oksikodon ağızdan alınabilir veya insüflasyon yoluyla yutulabilir; intravenöz olarak kullanılabilir veya ısıtılmış buharları solunabilir. ⓘ
Birleşik Devletler
Oksikodon, Amerika'da rekreasyonel olarak en yaygın kullanılan opioiddir. Amerika Birleşik Devletleri'nde 12 milyondan fazla kişi opioid ilaçları eğlence amaçlı olarak kullanmaktadır. ABD Sağlık ve İnsan Hizmetleri Bakanlığı, ABD'de yılda yaklaşık 11 milyon kişinin tıbbi olmayan bir şekilde oksikodon tükettiğini tahmin etmektedir. ⓘ
Opioidler, 2017 yılında ABD'de 72.000 aşırı dozda uyuşturucu ölümünün 49.000'inden sorumludur. 2007 yılında, oksikodon içeren "epizodlar" nedeniyle yaklaşık 42.800 acil servis ziyareti gerçekleşmiştir. 2008 yılında, oksikodon ve hidrokodonun eğlence amaçlı kullanımı 14.800 ölümde rol oynamıştır. Vakaların bir kısmı asetaminofen bileşeninin aşırı dozundan kaynaklanmış ve ölümcül karaciğer hasarına neden olmuştur. ⓘ
Eylül 2013'te FDA, uzun etkili ve uzatılmış salımlı opioidler için üreticilerin kullanım endikasyonu olarak orta şiddette ağrıyı kaldırmasını gerektiren yeni etiketleme kılavuzları yayınladı ve bunun yerine ilacın "günlük, günün her saati, uzun süreli opioid tedavisi gerektirecek kadar şiddetli ağrı" için olduğunu belirtti. Güncellenen etiketleme, hekimlerin opioidleri orta derecede, gerektiği gibi kullanım için reçete etmelerini kısıtlamayacaktır. ⓘ
Yeniden formüle edilen OxyContin, bazı eğlence amaçlı kullanıcıların daha ucuz ve elde edilmesi daha kolay olan eroine geçmesine neden oluyor. ⓘ
Davalar
Ekim 2017'de The New Yorker, Mortimer Sackler ve Purdue Pharma'nın oksikodon piyasalarının üretimi ve manipülasyonuyla olan bağlarına ilişkin bir haber yayınladı. Makale, Raymond ve Arthur Sackler'ın iş uygulamalarını doğrudan ilaç pazarlamasının yükselişiyle ve nihayetinde Amerika Birleşik Devletleri'nde oksikodon bağımlılığının artışıyla ilişkilendirmektedir. Makale, Sackler ailesinin Amerika Birleşik Devletleri'ndeki opioid salgınında bir miktar sorumluluk taşıdığını ima ediyor. 2019 yılında The New York Times, Raymond Sackler'ın oğlu Richard Sackler'ın 2008 yılında şirket yetkililerine "performansımızı Rx'lerin gücüne göre ölçün, daha yüksek güçlere daha yüksek ölçüler verin" dediğini doğrulayan bir haber yayınladı. Bu durum, Massachusetts başsavcısı Maura Healey tarafından açılan ve Purdue Pharma ile Sackler ailesi üyelerinin uzun süre yüksek dozda OxyContin kullanımının bağımlılık da dahil olmak üzere ciddi yan etki riskini artıracağını bildiklerini iddia eden bir davayla bağlantılı belgelerle doğrulanmıştır. Purdue Pharma'nın dava için 12 milyar ABD doları tutarında bir uzlaşma teklif etmesine rağmen, Massachusetts dahil 23 eyaletin başsavcısı Eylül 2019'da uzlaşma teklifini reddetti. ⓘ
Avustralya
Oksikodonun tıbbi olmayan kullanımı 1970'lerin başından beri mevcuttur, ancak 2015 yılı itibariyle Avustralya'da enjekte eden uyuşturucu kullanıcılarından oluşan ulusal bir örneklemin %91'i oksikodon kullandığını bildirmiş ve %27'si son altı ay içinde enjekte etmiştir. ⓘ
Kanada
Ontario'da opioid kaynaklı ölümler 1969'dan 2014'e kadar %242 oranında artmıştır. Ontario'da 2009 yılı itibariyle aşırı dozda oksikodondan ölenlerin sayısı aşırı dozda kokainden ölenlerin sayısından daha fazlaydı. Opioid ağrı kesicilerden kaynaklanan ölümler 1991 yılında bir milyon kişi başına 13,7 ölümden 2004 yılında bir milyon kişi başına 27,2 ölüme yükselmiştir. Kanada'da oksikodonun tıbbi olmayan kullanımı bir sorun haline gelmiştir. Oksikodonun en sorunlu olduğu bölgeler Atlantik Kanada ve Ontario'dur; buralardaki kırsal kasabalarda ve birçok küçük ila orta ölçekli şehirde tıbbi olmayan kullanımı yaygındır. Oksikodon Batı Kanada'da da yaygın olarak bulunmaktadır, ancak metamfetamin ve eroin büyük şehirlerde daha ciddi sorun teşkil ederken, oksikodon kırsal kasabalarda daha yaygındır. Oksikodon, doktor alışverişi, reçete sahteciliği, eczane hırsızlığı ve aşırı reçete yazma yoluyla saptırılmaktadır. ⓘ
Oksikodonun son formülasyonları, özellikle de Purdue Pharma'nın 2012 başlarında Kanada'da yasaklanan OxyContin ürününün yerini alan ezmeye, çiğnemeye, enjeksiyona ve çözünmeye dirençli OxyNEO, bu opiatın eğlence amaçlı kullanımında bir düşüşe yol açmış ancak daha güçlü bir ilaç olan fentanilin eğlence amaçlı kullanımını artırmıştır. Maclean's dergisinde yer alan Kanada Madde Bağımlılığı Merkezi'nin bir araştırmasına göre, Kanada'da beş yıllık bir dönemde fentanile bağlı en az 655 ölüm meydana gelmiştir. ⓘ
Alberta'da Blood Tribe polisi, 2014 sonbaharından 2015 Ocak ayına kadar, Alberta'nın Lethbridge kentinin güneybatısında yer alan Blood Reserve'de meydana gelen on ölümden, organize suç örgütü üyeleri tarafından yasadışı laboratuarlarda üretilen fentanil içeren oksikodon haplarının veya Oxy 80s olarak adlandırılan ölümcül sahte bir varyasyonun sorumlu olduğunu iddia etmiştir. Eyalet genelinde 2014 yılında yaklaşık 120 Albertalı fentanile bağlı aşırı dozdan ölmüştür. ⓘ
Birleşik Krallık
İskoçya'da Oksikodon reçeteleri 2002 ve 2008 yılları arasında %430 oranında artarak, kullanım sorunlarının Amerika Birleşik Devletleri'ndekilere benzemesinden korkulmasına yol açmıştır. Birleşik Krallık'ta aşırı doz nedeniyle bilinen ilk ölüm 2002 yılında meydana gelmiştir. ⓘ
Önleyici tedbirler
Ağustos 2010'da Purdue Pharma, OxyContin olarak pazarlanan uzun etkili oksikodon serisini, OxyContin'in tıbbi olmayan kullanımını azaltmak amacıyla hapların ezilmesini veya suda çözünmesini daha zor hale getirmek için Intac adlı bir polimer kullanarak yeniden formüle etmiştir. FDA, Nisan 2013'te yeniden formüle edilmiş versiyonun kötüye kullanıma dayanıklı olarak yeniden etiketlenmesini onaylamıştır. ⓘ
Pfizer, Oxecta olarak pazarlanan ve kurcalamaya dirençli Aversion Teknolojisi olarak adlandırılan inaktif bileşenler içeren kısa etkili bir oksikodon preparatı üretmektedir. Oral eğlence amaçlı kullanımı caydırmaz. Haziran 2011'de ABD'de FDA tarafından onaylanan yeni formülasyon, kimyasal özelliklerindeki değişiklik nedeniyle opioidin ezilmesini, çiğnenmesini, burundan çekilmesini veya enjekte edilmesini pratik olmaktan çıkarmaktadır. ⓘ
Yasal statü
Oksikodon, narkotik ilaçlara ilişkin uluslararası sözleşmelere tabidir. Buna ek olarak, oksikodon ülkeden ülkeye farklılık gösteren ulusal yasalara tabidir. Milletler Cemiyeti'nin 1931 tarihli Narkotik İlaçların Üretiminin Sınırlandırılması ve Dağıtımının Düzenlenmesi Sözleşmesi oksikodonu da içermektedir. 1931 tarihli sözleşmenin yerini alan 1961 tarihli Birleşmiş Milletler Narkotik Uyuşturucular Tek Sözleşmesi, oksikodonu Çizelge I'de kategorize etmiştir. I. Cetvel ilaçlara ilişkin küresel kısıtlamalar arasında bu ilaçların "üretiminin, imalatının, ihracatının, ithalatının, dağıtımının, ticaretinin, kullanımının ve bulundurulmasının yalnızca tıbbi ve bilimsel amaçlarla sınırlandırılması"; "[bu] ilaçların bireylere tedariki veya dağıtımı için tıbbi reçetelerin gerekli kılınması"; ve bu ilaçların "normal işlerin yürütülmesi için gerekli olandan fazla" miktarlarda "biriktirilmesinin önlenmesi" yer almaktadır. ⓘ
Avustralya
Oksikodon, Commonwealth'in 1967 tarihli Narkotik İlaçlar Yasası'nın (Narkotik İlaçlar Tek Sözleşmesi'nden türetilen) I sayılı Cetvelinde yer almaktadır. Buna ek olarak, Avustralya Uyuşturucu ve Zehirlerin Tek Tip Çizelgelendirilmesi Standardı ("Zehirler Standardı") Çizelge 8'de yer almaktadır, yani "kullanıma hazır olması gereken ancak kötüye kullanımı, suistimali ve fiziksel veya psikolojik bağımlılığı azaltmak için üretim, tedarik, dağıtım, bulundurma ve kullanımın kısıtlanmasını gerektiren kontrollü bir ilaçtır". ⓘ
Kanada
Oksikodon, Kontrollü İlaçlar ve Maddeler Yasası (CDSA) Çizelge I kapsamında kontrollü bir maddedir. ⓘ
Kanada mevzuat değişiklikleri

Şubat 2012'de Ontario, kamu tarafından finanse edilen ilaçlar için halihazırda mevcut olan ilaç takip sisteminin özel sigortalı ilaçları da kapsayacak şekilde genişletilmesine izin veren bir yasayı kabul etti. Bu veri tabanı, hastaların birden fazla doktordan reçete talep etme veya birden fazla eczaneden reçete alma girişimlerini tespit etme ve izleme işlevi görecektir. Diğer eyaletler de benzer mevzuat önerilerinde bulunurken Nova Scotia gibi bazı eyaletlerde reçeteli ilaç kullanımının izlenmesine yönelik mevzuat halihazırda yürürlüktedir. Bu değişiklikler, Ontario'nun ağrı kesicilerin kötüye kullanımı ve oksikodon gibi ilaçlara yüksek bağımlılık oranlarını hedef alan mevzuatındaki diğer değişikliklerle aynı zamana denk gelmiştir. 29 Şubat 2012 itibariyle Ontario, oksikodonu eyaletin kamu ilaç yardımı programından çıkaran yasayı kabul etti. Bu, herhangi bir eyaletin bağımlılık yapıcı özelliklerine dayanarak bir ilacı listeden çıkarması açısından bir ilkti. Yeni yasa, palyatif bakım ve diğer hafifletici koşullar da dahil olmak üzere İstisnai Erişim Programı kapsamındaki belirli hastalar dışında OxyNeo reçetelerini yasaklamaktadır. Halihazırda oksikodon reçete edilen hastalar OxyNeo için bir yıl daha teminat alacak ve bundan sonra, istisnai erişim programı kapsamında belirlenmediği sürece izin verilmeyecektir. ⓘ
Yasama faaliyetlerinin çoğu Purdue Pharma'nın 2011 yılında Oxycontin'in bileşiminde bir değişiklik yaparak burundan çekmek veya enjekte etmek için ezilmesini daha zor hale getirme kararından kaynaklanmaktadır. OxyNeo adlı yeni formülasyonun bu konuda önleyici olması ve bir ağrı kesici olarak etkinliğini koruması amaçlanmıştır. Ontario, Narkotik Güvenlik ve Farkındalık Yasası'nı yürürlüğe koymasından bu yana, özellikle sorunlu opioid reçetelerinin izlenmesi ve tespit edilmesinin yanı sıra hastaların, doktorların ve eczacıların eğitiminde uyuşturucu bağımlılığına odaklanmayı taahhüt etmiştir. 2010'da yürürlüğe giren bu Yasa, bu niyeti yerine getirmek için birleşik bir veri tabanı kurulmasını taahhüt etmektedir. Hem kamuoyu hem de tıp camiası mevzuatı olumlu karşılamış, ancak yasal değişikliklerin sonuçlarına ilişkin endişeler dile getirilmiştir. Yasalar büyük ölçüde il bazında düzenlendiğinden, birçok kişi daha gevşek kısıtlamalara sahip yargı bölgelerinden il sınırları boyunca kaçakçılığı önlemek için ulusal bir stratejiye ihtiyaç olduğunu düşünmektedir. ⓘ
2015 yılında Purdue Pharma'nın kötüye kullanıma dirençli OxyNEO ve OxyContin'in altı jenerik versiyonu 2012 yılından beri Kanada çapında reçeteler için onaylı listede yer alıyordu. Haziran 2015'te dönemin federal Sağlık Bakanı Rona Ambrose, üç yıl içinde Kanada'da satılan tüm oksikodon ürünlerinin kurcalamaya dayanıklı olması gerekeceğini duyurdu. Bazı uzmanlar, jenerik ürün üreticilerinin bu hedefe ulaşacak teknolojiye sahip olmayabileceği ve muhtemelen Purdue Pharma'ya bu opiat üzerinde bir tekel sağlayabileceği konusunda uyardı. ⓘ
Kanada'daki davalar
Kanada genelinde Purdue şirketler grubu ve iştiraklerine karşı çok sayıda toplu dava açılmıştır. Davacılar, ilaç üreticilerinin bir bakım standardını karşılamadığını ve bunu yaparken ihmalkar davrandıklarını iddia etmektedir. Bu davalar, Purdue'nun yanlış pazarlama uygulamaları ve yanlış markalamadan sorumlu olduğuna hükmeden Amerika Birleşik Devletleri'ndeki daha önceki kararlara atıfta bulunmaktadır. Purdue şirketleri 2007'den bu yana davaları çözmek ya da cezai yaptırımlarla karşı karşıya kalmak için 650 milyon CAN$'ın üzerinde ödeme yapmıştır. ⓘ
Almanya
İlaç, Narkotik Yasasının (Betäubungsmittelgesetz veya BtMG) Ek III'ünde yer almaktadır. Yasa sadece doktorların, diş hekimlerinin ve veterinerlerin oksikodon reçete etmesine ve federal hükümetin reçeteleri düzenlemesine (örneğin, raporlama zorunluluğu getirerek) izin vermektedir. ⓘ
Hong Kong
Oksikodon, Hong Kong'un 134. Bölüm Tehlikeli İlaçlar Yönetmeliğinin 1. Çizelgesinin I. Bölümü kapsamında düzenlenmektedir. ⓘ
Japonya
Oksikodon Japonya'da kısıtlanmış bir ilaçtır. İthalatı ve ihracatı, önceden ithal izni olan özel olarak belirlenmiş kuruluşlarla sıkı bir şekilde sınırlandırılmıştır. Yüksek profilli bir vakada, Tokyo'da yaşayan üst düzey bir Toyota yöneticisi olan ve yasadan haberi olmadığını iddia eden bir Amerikalı, Japonya'ya oksikodon ithal ettiği için tutuklanmıştır. ⓘ
Singapur
Oksikodon, Singapur Uyuşturucuların Kötüye Kullanımı Yasasında A Sınıfı bir uyuşturucu olarak listelenmiştir, bu da uyuşturucuyla ilgili suçların en ağır ceza seviyesini çektiği anlamına gelir. Uyuşturucunun izinsiz üretimine ilişkin bir mahkumiyet en az 10 yıl hapis ve 5 sopa darbesi, en fazla ise müebbet hapis veya 30 yıl hapis ve 15 sopa darbesi cezasını gerektirmektedir. Uyuşturucunun izinsiz ticareti için asgari ve azami cezalar sırasıyla 5 yıl hapis ve 5 sopa darbesi ve 20 yıl hapis ve 15 sopa darbesidir. ⓘ
Birleşik Krallık
Oksikodon, 1971 tarihli Uyuşturucuların Kötüye Kullanımı Yasası kapsamında A Sınıfı bir uyuşturucudur. "Zarar verme olasılığı en yüksek olan" A Sınıfı uyuşturucular için, reçetesiz bulundurma yedi yıla kadar hapis, sınırsız para cezası veya her ikisi ile cezalandırılabilir. İlacın yasadışı yollardan satılması ise ömür boyu hapis, sınırsız para cezası ya da her ikisiyle birden cezalandırılır. Buna ek olarak, oksikodon, "1971 tarihli Uyuşturucu Maddelerin Kötüye Kullanımı Yasası hükümlerinden belirli muafiyetler sağlayan" 2001 tarihli Uyuşturucu Maddelerin Kötüye Kullanımı Yönetmeliği'ne göre Çizelge 2'de yer alan bir ilaçtır. ⓘ
Birleşik Devletler
Kontrollü Maddeler Yasası uyarınca oksikodon, ister tek başına ister çok bileşenli bir ilacın parçası olsun, Çizelge II kontrollü bir maddedir. DEA, oksikodonu hem satış hem de diğer opioidlerin üretiminde kullanım için ACSCN 9143 olarak listelemektedir ve 2013 yılında aşağıdaki yıllık toplam üretim kotalarını onaylamıştır: 2012'de 153.75 olan satış için 131.5 metrik ton ve bir önceki yıla göre değişmeyen dönüşüm için 10.25 metrik ton. 2020 yılında ABD'nin Oregon eyaletinde oksikodon bulundurmak suç olmaktan çıkarılmıştır. ⓘ
Ekonomi
Uluslararası Narkotik Kontrol Kurulu 1998 yılında dünya çapında 11,5 kısa ton (10,4 t) oksikodon üretildiğini tahmin etmektedir; 2007 yılına gelindiğinde bu rakam 75,2 kısa tona (68,2 t) yükselmiştir. Amerika Birleşik Devletleri 2007 yılında 51.6 kısa ton (46.8 t) ile tüketimin %82'sini oluşturmuştur. Kanada, Almanya, Avustralya ve Fransa'nın toplamı 2007 yılında tüketimin %13'ünü oluşturmuştur. 2010 yılında, 1,3 kısa ton (1,2 t) oksikodon sahte hap baskısı kullanılarak yasadışı olarak üretilmiştir. Bu da tüketimin %0.8'ini oluşturmuştur. Uluslararası Narkotik Kontrol Kurulu'na göre bu yasadışı tabletler daha sonra ABD Uyuşturucuyla Mücadele İdaresi tarafından ele geçirilmiştir. Kurul ayrıca 2010 yılında 122.5 kısa ton (111.1 t) uyuşturucu üretildiğini bildirmiştir. Bu rakam 2009 yılındaki 135.9 kısa tonluk (123.3 t) rekor seviyeden düşüş göstermiştir. ⓘ
İsimler
Akademik literatürde oksikodon bileşiği için kullanılan genişletilmiş ifadeler arasında "dihidrohidroksikodeinon", "Eucodal", "Eukodal", "14-hidroksidihidrokodeinon" ve "Nucodan" yer almaktadır. UNESCO sözleşmesinde "oxycodone" kelimesinin çevirileri oxycodon (Hollandaca), oxycodone (Fransızca), oxicodona (İspanyolca), الأوكسيكودون (Arapça), 羟考酮 (Çince) ve оксикодон (Rusça) şeklindedir. "Oksikodon" kelimesi "oksandrolon", "oksazepam", "oksibutinin", "oksitosin" veya "Roxanol" ile karıştırılmamalıdır. ⓘ
Diğer marka isimleri arasında Longtec ve Shortec bulunmaktadır. ⓘ

