Morfin
 | |
 | |
| Klinik veriler | |
|---|---|
| Telaffuz | /ˈmoʊrfiːn/ |
| Ticari isimler | Statex, MS Contin, MST Continus, Oramorph, Sevredol ve diğerleri |
| AHFS/Drugs.com | Monografi |
| Hamilelik Kategori |
|
| Bağımlılık sorumluluk | Yüksek |
| Bağımlılık sorumluluk | Yüksek |
| Güzergahları YÖNETİM | İnhalasyon (sigara), insüflasyon (burundan çekme), ağız yoluyla (PO), rektal, subkutan (SC), intramüsküler (IM), intravenöz (IV), epidural ve intratekal (IT) |
| İlaç sınıfı | opioid |
| ATC kodu |
|
| Yasal statü | |
| Yasal statü |
|
| Farmakokinetik veriler | |
| Biyoyararlanım | 20-40 (ağızdan), %36-71 (rektal), %100 (IV/IM) |
| Protein bağlama | 30–40% |
| Metabolizma | Hepatik %90 |
| Etki başlangıcı | 5 dakika (IV), 15 dakika (IM), 20 dakika (PO) |
| Eliminasyon yarı ömrü | 2-3 saat |
| Etki süresi | 3-7 saat |
| Boşaltım | Renal %90, safra %10 |
| Tanımlayıcılar | |
IUPAC adı
| |
| CAS Numarası |
|
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| PDB ligandı |
|
| Kimyasal ve fiziksel veriler | |
| Formül | C17H19NO3 |
| Molar kütle | 285.343 g-mol-1 |
| 3D model (JSmol) | |
| Suda çözünürlük | HCl & sülf.: 60 mg/mL (20 °C) |
GÜLÜMSEMELER
| |
InChI
| |
| (doğrulayın) | |
Morfin, haşhaşta (Papaver somniferum) bulunan koyu kahverengi bir reçine olan afyonda doğal olarak bulunan opiat ailesinden bir ağrı kesici ilaçtır. Morfini uygulamak için kullanılan çok sayıda yöntem vardır: oral; dilaltı; inhalasyon yoluyla; kas içine enjeksiyon; deri altına enjeksiyon yoluyla; intravenöz olarak; omurilik etrafındaki boşluğa enjeksiyon; transdermal; veya rektal fitil yoluyla. Analjeziyi indüklemek ve ağrıya karşı algıyı ve duygusal tepkiyi değiştirmek için doğrudan merkezi sinir sistemi (MSS) üzerinde etkilidir. Tekrarlanan uygulama ile fiziksel ve psikolojik bağımlılık ve tolerans gelişebilir. Hem akut ağrı hem de kronik ağrı için alınabilir ve sıklıkla miyokard enfarktüsü, böbrek taşları ve doğum sırasındaki ağrılar için kullanılır. Maksimum etkisine damar yoluyla verildiğinde yaklaşık 20 dakika, ağız yoluyla verildiğinde ise 60 dakika sonra ulaşılır, etki süresi ise 3-7 saattir. Morfinin uzun etkili formülasyonları MS-Contin, Kadian ve diğer marka isimlerinin yanı sıra jenerik olarak da mevcuttur. ⓘ
Morfinin potansiyel olarak ciddi yan etkileri arasında solunum çabasında azalma, kusma, mide bulantısı ve düşük kan basıncı yer alır. Morfin bağımlılık yapar ve kötüye kullanıma eğilimlidir. Uzun süreli kullanımdan sonra kişinin dozu azaltılırsa, opioid yoksunluk belirtileri ortaya çıkabilir. Morfinin yaygın yan etkileri arasında uyuşukluk, kusma ve kabızlık yer alır. Bebeğin sağlığını etkileyebileceğinden, hamilelik veya emzirme döneminde morfin kullanımı için dikkatli olunması tavsiye edilir. ⓘ
Morfin ilk olarak 1803-1805 yılları arasında Alman eczacı Friedrich Sertürner tarafından izole edilmiştir. Bunun genellikle bir bitkiden aktif bir bileşenin ilk izolasyonu olduğuna inanılmaktadır. Merck 1827 yılında ticari olarak pazarlamaya başlamıştır. Morfin, 1853-1855 yıllarında hipodermik şırınganın icadından sonra daha yaygın olarak kullanılmaya başlanmıştır. Sertürner, uykuya neden olma eğilimi nedeniyle maddeye Yunan rüya tanrısı Morpheus'tan esinlenerek morphium adını vermiştir. ⓘ
Morfinin birincil kaynağı afyon haşhaşının samanından elde edilen izolasyondur. 2013 yılında yaklaşık 523 ton morfin üretilmiştir. Yaklaşık 45 tonu doğrudan ağrı için kullanılmış olup son yirmi yılda %400 artış göstermiştir. Bu amaçla kullanımın çoğu gelişmiş ülkelerde gerçekleşmiştir. Morfinin yaklaşık yüzde 70'i hidromorfon, oksimorfon ve eroin gibi diğer opioidlerin yapımında kullanılmaktadır. Amerika Birleşik Devletleri'nde Çizelge II, Birleşik Krallık'ta Sınıf A ve Kanada'da Çizelge I uyuşturucusudur. Dünya Sağlık Örgütü'nün Temel İlaçlar Listesi'nde yer almaktadır. Morfin birçok ticari isim altında satılmaktadır. 2019 yılında, 3 milyondan fazla reçete ile Amerika Birleşik Devletleri'nde en sık reçete edilen 163. ilaç olmuştur. ⓘ
| Morfin ⓘ | |
|---|---|
 | |
| Sistematik (IUPAC) adı | |
| 3,6-dihidroksi-4,5-epoksi-17-metilmorfinan-7-en | |
| Kimlik belirteçleri | |
| CAS numarası | 57-27-2 |
| ATC kodu | N02 AA01 |
| PubChem | 5288826 |
| DrugBank | APRD00215 |
| Kimyasal özellikler | |
| Kimyasal formül | C17H19NO3 |
| Moleküler ağırlık | 285,4 g/mol |
| Farmakokinetik özellikler | |
| Biyoyararlanım | ~%15 |
| Proteine bağlanma | %30-40 |
| Metabolizma | %90 hepatik |
| Yarılanma ömrü | 2-3 saat |
| Atılma | %90 renal |
| Tedavi bilgileri | |
| Gebelik kategorisi |
ABD - C Avustralya - C |
Morfin çok etkili bir opiat ağrı kesici ilaç etken maddesidir, opioidlerin tipik aktif maddesidir ve bu grubun prototipidir. Ham afyonda %10-12 oranında mevcuttur. Molekül DSÖ'nün Temel İlaçlar Listesi'nde yer almaktadır. ⓘ
Tıbbi kullanımları
Ağrı
Morfin öncelikle hem akut hem de kronik şiddetli ağrıları tedavi etmek için kullanılır. Analjezi süresi yaklaşık üç ila yedi saattir. Bulantı ve kabızlık gibi yan etkiler nadiren tedaviyi durdurmayı gerektirecek kadar şiddetlidir. ⓘ
Miyokard enfarktüsüne bağlı ağrılarda ve doğum sancılarında kullanılır. Bununla birlikte, morfinin ST yükselmesi olmayan miyokard enfarktüsü durumunda mortaliteyi artırabileceğine dair endişeler mevcuttur. Morfin geleneksel olarak akut pulmoner ödem tedavisinde de kullanılmaktadır. Ancak 2006 yılında yapılan bir incelemede bu uygulamayı destekleyen çok az kanıt bulunmuştur. 2016 yılında yapılan bir Cochrane incelemesi, morfinin kanser ağrısının giderilmesinde etkili olduğu sonucuna varmıştır. ⓘ
Şiddetli kronik ağrılar veya diğer analjeziklere dirençli kanser ağrılarında, kas ağrısı ve idrar yolu bozukluklarında kullanılır. ⓘ
Nefes darlığı
Morfin, hem kanser hem de kanser dışı nedenlere bağlı nefes darlığı semptomlarının azaltılmasında faydalıdır. İleri evre kanser veya son evre kardiyorespiratuar hastalıklar gibi durumlardan kaynaklanan istirahat halinde veya minimal eforda nefes darlığı durumunda, düzenli, düşük doz sürekli salınımlı morfin nefes darlığını güvenli bir şekilde önemli ölçüde azaltır ve faydaları zaman içinde korunur. ⓘ
Opioid kullanım bozukluğu
Morfin ayrıca Avusturya, Almanya, Bulgaristan, Slovenya ve Kanada'da metadon veya buprenorfini tolere edemeyen opioid bağımlılığı olan kişiler için opiat ikame tedavisi (OST) için yavaş salınımlı bir formülasyon olarak da mevcuttur. ⓘ
10 mg morfin içeren 1 mililitrelik ampul ⓘ
Damar, cilt altı ve kasa verilir. Ortalama 10 mg verilir. Pediatrik doz 10 mg'ı (0.1-0.2 mg/kg) geçmemelidir. ⓘ
Kontrendikasyonlar
Bu grup ilaçlar, solunum sistemi, obstrüktif solunum yolu hastalıkları veya solunum ile ilintili hastalıkları (astım gibi) olan vakalarda uygulanmamalıdır. İlaç bağımlılığı olan veya bu yönde eğilimi olan vakalarda uygulanmaz. Etken maddeye ve diğer narkotik analjeziklere aşırı duyarlılığı olduğu bilinen vakalarda kontrendikedir. Prostat büyümelerinde kullanılmaz, tam blok oluşturabileceği için mesane duvarı yırtılmalarına sebep olabilir. Epilepsilerde, kafa içi basıncının yüksek olduğu durumlarda, böbrek üstü bezi disfonksiyonlarında kullanılmamalıdır. Akut karaciğer yetmezliği veya karaciğerde işlev kaybıyla birlikte olan vakalarda, hamilelerde, emzirenlerde, bebeklerde ve pre-operatif yatıştırıcı olarak uygulanmaz. Nedeni bilinmeyen akut abdominal sendrom, kraniyal travma ve intrakraniyal basınç artışı, konvülzif durumlar, akut alkolik intoksikasyon ve delirium tremens, 30 aylıktan küçük çocuklar ve MAO inhibitörleriyle tedavi durumlarında kontrendikedir. ⓘ
Morfinin göreceli kontrendikasyonları şunları içerir:
- uygun ekipman mevcut olmadığında solunum depresyonu
- Daha önce morfinin akut pankreatitte kontrendike olduğu düşünülse de, literatür incelendiğinde buna dair bir kanıt bulunamamıştır. ⓘ
Yan etkiler
- Yaygın ve kısa vadeli
- Kaşıntı
- Mide bulantısı
- Kusma
- Kabızlık
- Uyuşukluk
- Ağız kuruluğu
- Solunum depresyonu
- Kaşıntı
- Diğer
- Opioid bağımlılığı
- Baş dönmesi
- Azalmış cinsel dürtü
- İştah kaybı
- Bozulmuş cinsel işlev
- Testosteron seviyelerinde azalma
- Depresyon
- Bağışıklık Yetmezliği
- Opioid kaynaklı anormal ağrı duyarlılığı
- Düzensiz adet kanaması
- Düşme riskinde artış
- Yavaş nefes alma
- Halüsinasyonlar ⓘ
Kabızlık
Loperamid ve diğer opioidler gibi morfin de bağırsak kanalındaki myenterik pleksusa etki ederek bağırsak hareketliliğini azaltır ve kabızlığa neden olur. Morfinin gastrointestinal etkilerine öncelikle bağırsaktaki μ-opioid reseptörleri aracılık eder. Mide boşalmasını inhibe ederek ve bağırsağın itici peristaltizmini azaltarak, morfin bağırsak geçiş hızını azaltır. Bağırsak salgısının azalması ve bağırsak sıvı emiliminin artması da kabızlaştırıcı etkiye katkıda bulunur. Opioidler ayrıca nitrik oksit oluşumunun engellenmesinden sonra tonik bağırsak spazmları yoluyla dolaylı olarak bağırsak üzerinde etkili olabilir. Bu etki, nitrik oksit öncüsü L-argininin bağırsak hareketliliğinde morfinin neden olduğu değişiklikleri tersine çevirdiği hayvanlarda gösterilmiştir. ⓘ
Hormon dengesizliği
Klinik çalışmalar, diğer opioidler gibi morfinin de her iki cinsiyetten kronik kullanıcılarda sıklıkla hipogonadizme ve hormon dengesizliklerine neden olduğu sonucuna varmaktadır. Bu yan etki doza bağlıdır ve hem terapötik hem de eğlence amaçlı kullanıcılarda görülür. Morfin, lüteinizan hormon seviyelerini baskılayarak kadınlarda adet kanamasını engelleyebilir. Birçok çalışma, kronik opioid kullanıcılarının çoğunda (belki de %90'ında) opioid kaynaklı hipogonadizm olduğunu göstermektedir. Bu etki, kronik morfin kullanıcılarında gözlenen osteoporoz ve kemik kırılması olasılığının artmasına neden olabilir. Çalışmalar bu etkinin geçici olduğunu göstermektedir. 2013 itibariyle, düşük doz veya akut morfin kullanımının endokrin sistem üzerindeki etkisi belirsizdir. ⓘ
İnsan performansı üzerindeki etkileri
İncelemelerin çoğu opioidlerin duyusal, motor veya dikkat yetenekleri testlerinde insan performansında asgari düzeyde bozulmaya yol açtığı sonucuna varmaktadır. Bununla birlikte, son çalışmalar morfinin neden olduğu bazı bozuklukları gösterebilmiştir ki morfinin bir merkezi sinir sistemi depresanı olduğu düşünüldüğünde bu şaşırtıcı değildir. Morfin, kritik titreşim frekansında (genel MSS uyarılmasının bir ölçüsü) işlev bozukluğu ve Maddox kanat testinde (gözlerin görsel eksenlerinin sapmasının bir ölçüsü) performans bozukluğu ile sonuçlanmıştır. Morfinin motor beceriler üzerindeki etkilerini araştıran az sayıda çalışma bulunmaktadır; yüksek dozda morfin parmak vurma ve düşük sabit izometrik kuvvet seviyesini koruma becerisini bozabilir (yani ince motor kontrolü bozulur), ancak hiçbir çalışma morfin ile kaba motor beceriler arasında bir korelasyon göstermemiştir. ⓘ
Bilişsel yetenekler açısından, bir çalışma morfinin anterograd ve retrograd hafıza üzerinde olumsuz bir etkisi olabileceğini göstermiştir, ancak bu etkiler minimal ve geçicidir. Genel olarak, toleranslı olmayan deneklerde akut opioid dozlarının bazı duyusal ve motor yeteneklerde ve belki de dikkat ve bilişte küçük etkiler yarattığı görülmektedir. Morfinin etkilerinin opioid naif deneklerde kronik opioid kullanıcılarına göre daha belirgin olması muhtemeldir. ⓘ
Şiddetli, kronik ağrıyı yönetmek için Kronik Opioid Analjezik Tedavisi (COAT) kullananlar gibi kronik opioid kullanıcılarında, davranış testleri çoğu durumda algı, biliş, koordinasyon ve davranışta normal işleyiş göstermiştir. 2000 yılında yapılan bir çalışmada, COAT hastalarının güvenli bir şekilde motorlu araç kullanıp kullanamayacakları analiz edilmiştir. Bu çalışmadan elde edilen bulgular, istikrarlı opioid kullanımının araç kullanmaya özgü yetenekleri önemli ölçüde bozmadığını göstermektedir (buna fiziksel, bilişsel ve algısal beceriler dahildir). COAT hastaları, başarılı performans için yanıt verme hızı gerektiren görevleri (örn. Rey Karmaşık Şekil Testi) hızlı bir şekilde tamamlamış, ancak kontrollere göre daha fazla hata yapmıştır. COAT hastaları görsel-mekânsal algı ve organizasyonda (WAIS-R Blok Tasarım Testinde gösterildiği gibi) herhangi bir eksiklik göstermemiş, ancak anlık ve kısa süreli görsel hafızada (Rey Karmaşık Şekil Testi - Hatırlama'da gösterildiği gibi) bozulma göstermiştir. Bu hastalar üst düzey bilişsel becerilerde (örn. planlama) herhangi bir bozulma göstermemiştir. COAT hastalarının talimatları takip etmekte zorlandıkları ve dürtüsel davranış eğilimi gösterdikleri görülmüştür, ancak bu istatistiksel anlamlılığa ulaşmamıştır. Bu çalışmanın, kronik opioid kullanımının psikomotor, bilişsel veya nöropsikolojik işlevsellik üzerinde küçük etkileri olduğu fikrini destekleyen, COAT hastalarının alana özgü eksiklikleri olmadığını ortaya koyduğunu belirtmek önemlidir. ⓘ
Pekiştirme bozuklukları
Bağımlılık

Morfin yüksek derecede bağımlılık yapıcı bir maddedir. Daha önce afyon bağımlısı olan bireylerde eroin ve morfinin fizyolojik ve öznel etkilerini karşılaştıran kontrollü çalışmalarda, denekler bir ilacı diğerine tercih etmemişlerdir. Eşdeğer, enjekte edilen dozlar karşılaştırılabilir etki süreçlerine sahipti ve deneklerin kendi kendilerine değerlendirdikleri coşku, hırs, sinirlilik, rahatlama, uyuşukluk veya uyku hali duygularında hiçbir fark yoktu. Aynı araştırmacılar tarafından yapılan kısa süreli bağımlılık çalışmaları, toleransın hem eroin hem de morfine benzer bir oranda geliştiğini göstermiştir. Opioidler hidromorfon, fentanil, oksikodon ve pethidin/meperidin ile karşılaştırıldığında, eski bağımlıların eroin ve morfini güçlü bir şekilde tercih ettikleri görülmüştür; bu da eroin ve morfinin kötüye kullanım ve bağımlılığa özellikle yatkın olduğunu düşündürmektedir. Morfin ve eroinin öfori ve diğer olumlu öznel etkiler yaratma olasılığı da diğer opioidlere kıyasla çok daha yüksektir. Eski uyuşturucu bağımlıları tarafından diğer opioidler yerine eroin ve morfinin tercih edilmesinin nedeni eroinin (morfin diasetat, diamorfin veya diasetil morfin olarak da bilinir) morfinin bir esteri ve bir morfin ön ilacı olması, yani aslında in vivo olarak özdeş ilaçlar olmaları olabilir. Eroin, beyin ve omurilikteki opioid reseptörlerine bağlanmadan önce morfine dönüştürülür, burada morfin bağımlı bireylerin aradığı öznel etkilere neden olur. ⓘ
Tolerans
Toleransın nasıl geliştiğine dair opioid reseptör fosforilasyonu (reseptör konformasyonunu değiştirir), reseptörlerin G-proteinlerinden işlevsel olarak ayrılması (reseptör duyarsızlaşmasına yol açar), μ-opioid reseptör içselleştirmesi veya reseptör aşağı regülasyonu (morfinin etki edebileceği mevcut reseptör sayısını azaltır) ve cAMP yolunun yukarı regülasyonu (opioid etkilerine karşı düzenleyici bir mekanizma) dahil olmak üzere çeşitli hipotezler ortaya atılmıştır (Bu süreçlerin gözden geçirilmesi için bkz. Koch ve Hollt. ) CCK, opioid toleransından sorumlu bazı karşı düzenleyici yollara aracılık edebilir. CCK-antagonisti ilaçların, özellikle de proglumidin, morfine tolerans gelişimini yavaşlattığı gösterilmiştir. ⓘ
Bağımlılık ve yoksunluk
Morfin dozunun kesilmesi, barbitüratlar, benzodiazepinler, alkol veya sedatif-hipnotiklerin aksine, sağlıklı kişilerde kendi başına ölümcül olmayan prototipik opioid yoksunluk sendromunu yaratır. ⓘ
Akut morfin yoksunluğu, diğer opioidlerle birlikte, bir dizi aşamadan geçerek ilerler. Diğer opioidlerin her birinin yoğunluğu ve uzunluğu farklıdır ve zayıf opioidler ve karışık agonist-antagonistler en yüksek seviyeye ulaşmayan akut yoksunluk sendromlarına sahip olabilir. Yaygın olarak belirtildiği üzere bunlar
- Evre I, son dozdan 6 saat ila 14 saat sonra: Uyuşturucu özlemi, anksiyete, sinirlilik, terleme ve hafif ila orta derecede disfori
- Evre II, son dozdan 14 saat ila 18 saat sonra: Esneme, yoğun terleme, hafif depresyon, göz yaşarması, ağlama, baş ağrısı, burun akıntısı, disfori, ayrıca yukarıdaki semptomların yoğunlaşması, "yen uykusu" (uyanık trans benzeri bir durum)
- Evre III, son dozdan 16 saat ila 24 saat sonra: Rinore (burun akıntısı) ve yukarıdakilerin diğerlerinde artış, göz bebeklerinde büyüme, piloereksiyon (tüylerin diken diken olması - 'cold turkey' deyiminin kökeni olduğu iddia edilir, ancak aslında bu deyim ilaç tedavisi dışında ortaya çıkmıştır), kas seğirmeleri, sıcak basması, soğuk basması, ağrıyan kemikler ve kaslar, iştah kaybı ve bağırsak kramplarının başlaması
- Evre IV, son dozdan 24 saat ila 36 saat sonra: Şiddetli kramp ve istemsiz bacak hareketleri ("alışkanlığı tekmeleme" huzursuz bacak sendromu olarak da adlandırılır), gevşek dışkı, uykusuzluk, kan basıncında yükselme, vücut ısısında orta derecede yükselme, solunum sıklığında ve tidal hacimde artış, taşikardi (nabızda yükselme), huzursuzluk, bulantı dahil olmak üzere yukarıdakilerin hepsinde artış
- Evre V, son dozdan 36 saat ila 72 saat sonra: Yukarıda artış, fetal pozisyon, kusma, bazen yiyeceklerin ağızdan sistem dışına geçiş süresini hızlandırabilen serbest ve sık sıvı ishal, 24 saatte 2 kg ila 5 kg kilo kaybı, artmış beyaz hücre sayısı ve diğer kan değişiklikleri
- Aşama VI, yukarıdakilerin tamamlanmasından sonra: İştahın ve normal bağırsak fonksiyonunun geri kazanılması, çoğunlukla psikolojik olan ancak ağrıya karşı artan hassasiyet, hipertansiyon, kolit veya motilite ile ilgili diğer gastrointestinal rahatsızlıkları ve her iki yönde de kilo kontrolü ile ilgili sorunları da içerebilen postakut ve kronik semptomlara geçişin başlaması ⓘ
Yoksunluğun ileri aşamalarında, bazı hastalarda ultrasonografik pankreatit kanıtları gösterilmiştir ve muhtemelen pankreatik Oddi sfinkterinin spazmına bağlanmaktadır. ⓘ
Morfin bağımlılığıyla ilişkili yoksunluk belirtileri genellikle bir sonraki planlanan doz zamanından kısa bir süre önce, bazen de son uygulamadan birkaç saat sonra (genellikle 6 saat ila 12 saat) yaşanır. Erken belirtiler arasında gözlerde sulanma, uykusuzluk, ishal, burun akıntısı, esneme, disfori, terleme ve bazı durumlarda güçlü bir uyuşturucu arzusu yer alır. Sendrom ilerledikçe şiddetli baş ağrısı, huzursuzluk, sinirlilik, iştahsızlık, vücut ağrıları, şiddetli karın ağrısı, bulantı ve kusma, titreme ve daha da güçlü ve yoğun uyuşturucu arzusu ortaya çıkar. Şiddetli depresyon ve kusma çok yaygındır. Akut yoksunluk döneminde, sistolik ve diyastolik kan basınçları genellikle premorfin seviyelerinin ötesinde artar ve kalp krizi, kan pıhtılaşması veya felce neden olma potansiyeline sahip kalp atış hızı artar. ⓘ
Kızarma (sıcak basması), bacaklarda tekme hareketleri ("alışkanlığı bırakmak") ve aşırı terleme ile dönüşümlü olarak titreme veya tüylerin diken diken olduğu soğuk basması ("cold turkey") da karakteristik semptomlardır. Kas spazmları gibi sırt ve ekstremitelerdeki kemik ve kaslarda şiddetli ağrılar meydana gelir. Bu sürecin herhangi bir noktasında, yoksunluk belirtilerini önemli ölçüde tersine çevirecek uygun bir narkotik verilebilir. Başlıca yoksunluk belirtileri son dozdan sonra 48 saat ile 96 saat arasında zirve yapar ve yaklaşık 8 ila 12 gün sonra azalır. Sağlık durumu kötü olan ağır bağımlı kullanıcılar tarafından ani yoksunluk çok nadiren ölümcüldür. Morfin yoksunluğunun alkol, barbitürat veya benzodiazepin yoksunluğundan daha az tehlikeli olduğu düşünülmektedir. ⓘ
Morfin bağımlılığı ile ilişkili psikolojik bağımlılık karmaşık ve uzun sürelidir. Morfine duyulan fiziksel ihtiyaç geçtikten çok sonra bile, bağımlı kişi genellikle morfin (veya diğer uyuşturucuların) kullanımı hakkında düşünmeye ve konuşmaya devam edecek ve morfinin etkisi altında olmadan günlük faaliyetlerle başa çıkmakta garip veya bunalmış hissedecektir. Morfinden psikolojik yoksunluk genellikle çok uzun ve acı verici bir süreçtir. Bağımlılar sıklıkla şiddetli depresyon, anksiyete, uykusuzluk, ruh hali değişimleri, amnezi (unutkanlık), düşük özgüven, kafa karışıklığı, paranoya ve diğer psikolojik bozukluklar yaşarlar. Müdahale edilmediği takdirde sendrom kendi seyrinde ilerleyecek ve psikolojik bağımlılık da dahil olmak üzere açık fiziksel semptomların çoğu 7 ila 10 gün içinde ortadan kalkacaktır. Ne fiziksel çevre ne de kötüye kullanıma katkıda bulunan davranışsal motivasyonlar değiştirilmediğinde, morfin yoksunluğundan sonra yüksek bir nüks olasılığı vardır. Morfinin bağımlılık yapıcı ve pekiştirici doğasının kanıtı nüksetme oranıdır. Morfin (ve eroin) bağımlıları, tüm uyuşturucu kullanıcıları arasında en yüksek nüks oranlarından birine sahiptir ve bazı tıp uzmanlarının tahminlerine göre bu oran %98'e kadar çıkmaktadır. ⓘ
Toksisite
| Morfinin Özellikleri ⓘ | |||||
|---|---|---|---|---|---|
| Molar kütle | 285.338 g/mol | ||||
| Asitlik (pKa) |
| ||||
| Çözünürlük | 20 °C'de 0,15 g/L | ||||
| Erime noktası | 255 °C | ||||
| Kaynama noktası | 190 °C süblimleşir | ||||
Büyük bir doz aşımı, kişi derhal tıbbi yardım almazsa asfiksi ve solunum depresyonu nedeniyle ölüme neden olabilir. Doz aşımı tedavisi nalokson uygulanmasını içerir. Nalokson morfinin etkilerini tamamen tersine çevirir ancak opiyat bağımlısı kişilerde yoksunluğun hemen başlamasına neden olabilir. Morfinin etki süresi naloksonunkinden daha uzun olduğu için birden fazla doz gerekebilir. ⓘ
Morfin sülfat ve diğer preparatların insanlar için LD50 değeri kesin olarak bilinmemektedir. Askerler arasında aşırı dozda morfin kullanımı üzerine yapılan düşük kaliteli bir çalışmada ölümcül dozun erkeklerde 0,78 mcg/ml (ortalama 90 kg yetişkin bir erkek için ~71 mg) ve kadınlarda 0,98 mcg/ml (ortalama 75 kg bir kadın için ~74 mg) olduğu bildirilmiştir. Dozun oral, parenteral veya IV olup olmadığı belirtilmemiştir. Literatürde genellikle laboratuvar hayvanları üzerinde yapılan çalışmalara atıfta bulunulmaktadır. Ciddi ilaç bağımlılığında (yüksek tolerans) günde 2000-3000 mg tolere edilebilir. ⓘ
Farmakoloji
Farmakodinamik
| Bileşik | Yakınlıklar (Ki) | Oran | Ref | ||
|---|---|---|---|---|---|
| MOR | DOR | KOR | MOR:DOR:KOR | ||
| Morfin | 1,8 nM | 90 nM | 317 nM | 1:50:176 | |
| (-)-Morfin | 1,24 nM | 145 nM | 23,4 nM | 1:117:19 | |
| (+)-Morfin | >10 μM | >100 μM | >300 μM | ND | |
| Bileşik | Rota | Doz |
|---|---|---|
| Kodein | PO | 200 mg |
| Hidrokodon | PO | 20-30 mg |
| Hidromorfon | PO | 7,5 mg |
| Hidromorfon | IV | 1,5 mg |
| Morfin | PO | 30 mg |
| Morfin | IV | 10 mg |
| Oksikodon | PO | 20 mg |
| Oksikodon | IV | 10 mg |
| Oksimorfon | PO | 10 mg |
| Oksimorfon | IV | 1 mg |
Morfin prototipik opioiddir ve diğer opioidlerin test edildiği standarttır. Ağırlıklı olarak μ-δ-opioid (Mu-Delta) reseptör heteromeri ile etkileşime girer. μ-bağlanma bölgeleri, insan beyninde, posterior amigdala, hipotalamus, talamus, nucleus caudatus, putamen ve bazı kortikal alanlarda yüksek yoğunlukta olmak üzere ayrı ayrı dağılmıştır. Ayrıca omuriliğin lamina I ve II (substantia gelatinosa) içindeki primer afferentlerin terminal aksonlarında ve trigeminal sinirin spinal çekirdeğinde bulunurlar. ⓘ
Morfin bir fenantren opioid reseptör agonistidir - ana etkisi merkezi sinir sistemindeki μ-opioid reseptörüne (MOR) bağlanmak ve onu aktive etmektir. MOR'daki içsel aktivitesi büyük ölçüde teste ve test edilen dokuya bağlıdır; bazı durumlarda tam agonist iken bazı durumlarda kısmi agonist veya hatta antagonist olabilir. Klinik ortamlarda, morfin temel farmakolojik etkisini merkezi sinir sistemi ve gastrointestinal sistem üzerinde gösterir. Terapötik değeri olan birincil etkileri analjezi ve sedasyondur. MOR'un aktivasyonu analjezi, sedasyon, öfori, fiziksel bağımlılık ve solunum depresyonu ile ilişkilidir. Morfin aynı zamanda bir κ-opioid reseptörü (KOR) ve δ-opioid reseptörü (DOR) agonistidir. KOR'un aktivasyonu spinal analjezi, miyozis (nokta göz bebekleri) ve psikotomimetik etkilerle ilişkilidir. DOR'un analjezide rol oynadığı düşünülmektedir. Morfin σ reseptörüne bağlanmamasına rağmen, (+)-pentazosin gibi σ reseptör agonistlerinin morfin analjezisini inhibe ettiği ve σ reseptör antagonistlerinin morfin analjezisini arttırdığı gösterilmiştir, bu da σ reseptörünün morfinin etkilerine aşağı yönde katılımını düşündürmektedir. ⓘ
Morfinin etkileri nalokson ve naltrekson gibi opioid reseptör antagonistleri ile önlenebilir; morfine karşı tolerans gelişimi ketamin veya dekstrometorfan gibi NMDA reseptör antagonistleri ile engellenebilir. Uzun süreli ağrı tedavisinde morfinin kimyasal olarak farklı opioidlerle rotasyonu, özellikle levorfanol, ketobemidon, piritramid ve metadon ve türevleri gibi morfinle çapraz toleransı önemli ölçüde azalttığı bilinen ajanlar olmak üzere, uzun vadede toleransın büyümesini yavaşlatacaktır; bu ilaçların tümü aynı zamanda NMDA antagonisti özelliklere sahiptir. Morfin ile çapraz toleransı en az olan güçlü opioidin metadon veya dekstromoramid olduğuna inanılmaktadır. ⓘ

Gen ifadesi
Çalışmalar morfinin bir dizi genin ifadesini değiştirebileceğini göstermiştir. Tek bir morfin enjeksiyonunun, mitokondriyal solunumda yer alan proteinler ve hücre iskeleti ile ilgili proteinler için iki ana gen grubunun ifadesini değiştirdiği gösterilmiştir. ⓘ
Bağışıklık sistemi üzerindeki etkileri
Morfinin uzun zamandır merkezi sinir sistemi hücrelerinde ifade edilen reseptörler üzerinde etkili olduğu ve ağrı kesici ve analjezi sağladığı bilinmektedir. 1970'lerde ve 80'lerde, opioid uyuşturucu bağımlılarının enfeksiyon riskinin arttığını gösteren kanıtlar (artan pnömoni, tüberküloz ve HIV/AIDS gibi) bilim insanlarını morfinin bağışıklık sistemini de etkileyebileceğine inanmaya yöneltmiştir. Bu olasılık, kronik morfin kullanımının bağışıklık sistemi üzerindeki etkisine olan ilgiyi artırmıştır. ⓘ
Morfinin bağışıklık sistemini etkileyebileceğini belirlemenin ilk adımı, merkezi sinir sistemi hücrelerinde ifade edildiği bilinen opiat reseptörlerinin bağışıklık sistemi hücrelerinde de ifade edildiğini tespit etmekti. Bir çalışma, doğuştan gelen bağışıklık sisteminin bir parçası olan dendritik hücrelerin opiat reseptörleri sergilediğini başarıyla göstermiştir. Dendritik hücreler, bağışıklık sisteminde iletişim araçları olan sitokinlerin üretilmesinden sorumludur. Aynı çalışma, farklılaşmaları sırasında kronik olarak morfinle tedavi edilen dendritik hücrelerin, T hücrelerinin (adaptif bağışıklık sisteminin başka bir hücresi) çoğalmasını, büyümesini ve farklılaşmasını teşvik etmekten sorumlu bir sitokin olan daha fazla interlökin-12 (IL-12) ve B hücresi bağışıklık tepkisini teşvik etmekten sorumlu bir sitokin olan daha az interlökin-10 (IL-10) ürettiğini göstermiştir (B hücreleri enfeksiyonla savaşmak için antikor üretir). ⓘ
Sitokinlerin bu şekilde düzenlenmesi p38 MAPK'lara (mitojenle aktive olan protein kinaz) bağlı yol üzerinden gerçekleşiyor gibi görünmektedir. Genellikle, dendritik hücre içindeki p38, ligand LPS (lipopolisakkarit) yoluyla aktive olan TLR 4'ü (toll benzeri reseptör 4) ifade eder. Bu da p38 MAPK'nın fosforile olmasına neden olur. Bu fosforilasyon, IL-10 ve IL-12 üretmeye başlamak için p38 MAPK'yı aktive eder. Dendritik hücreler farklılaşma süreçleri sırasında kronik olarak morfine maruz bırakılıp ardından LPS ile muamele edildiklerinde, sitokinlerin üretimi farklıdır. Morfinle muamele edildikten sonra, p38 MAPK IL-10 üretmez, bunun yerine IL-12 üretimini tercih eder. Bir sitokin üretiminin diğerine göre hangi mekanizma ile arttığı tam olarak bilinmemektedir. Büyük olasılıkla morfin, p38 MAPK'nın fosforilasyonunun artmasına neden olmaktadır. IL-10 ve IL-12 arasındaki transkripsiyonel düzeydeki etkileşimler, IL-10 üretilmediğinde IL-12 üretimini daha da artırabilir. Bu artan IL-12 üretimi T-hücresi bağışıklık yanıtının artmasına neden olur. ⓘ
Morfinin bağışıklık sistemi üzerindeki etkileri üzerine yapılan daha ileri çalışmalar, morfinin nötrofil ve diğer sitokinlerin üretimini etkilediğini göstermiştir. Sitokinler ani immünolojik yanıtın (inflamasyon) bir parçası olarak üretildiklerinden, ağrıyı da etkileyebilecekleri öne sürülmüştür. Bu şekilde, sitokinler analjezik gelişimi için mantıklı bir hedef olabilir. Son zamanlarda yapılan bir çalışmada, morfin uygulamasının akut immünolojik yanıt üzerindeki etkilerini gözlemlemek için bir hayvan modeli (arka pençe kesisi) kullanılmıştır. Arka pençe insizyonunu takiben, ağrı eşikleri ve sitokin üretimi ölçülmüştür. Normalde, enfeksiyonla mücadele etmek ve iyileşmeyi kontrol etmek (ve muhtemelen ağrıyı kontrol etmek) için yaralı bölgede ve çevresinde sitokin üretimi artar, ancak kesi öncesi morfin uygulaması (0.1 mg/kg ila 10.0 mg/kg) yara çevresinde bulunan sitokin sayısını doza bağlı bir şekilde azaltmıştır. Yazarlar, yaralanma sonrası akut dönemde morfin uygulamasının enfeksiyona karşı direnci azaltabileceğini ve yaranın iyileşmesini bozabileceğini öne sürmektedir. ⓘ
Farmakokinetik
Emilim ve metabolizma
Morfin ağızdan, dil altından, bukkal, rektal, subkutan, intranazal, intravenöz, intratekal veya epidural olarak alınabilir ve bir nebülizör yoluyla solunabilir. Eğlence amaçlı bir uyuşturucu olarak, solumak daha yaygın hale gelmektedir ("Chasing the Dragon"), ancak tıbbi amaçlar için intravenöz (IV) enjeksiyon en yaygın uygulama yöntemidir. Morfin kapsamlı bir ilk geçiş metabolizmasına tabidir (büyük bir kısmı karaciğerde parçalanır), bu nedenle ağızdan alındığında dozun yalnızca %40 ila %50'si merkezi sinir sistemine ulaşır. Subkutan (SC), intramüsküler (IM) ve IV enjeksiyondan sonra ortaya çıkan plazma seviyelerinin hepsi karşılaştırılabilir. IM veya SC enjeksiyonlardan sonra, morfin plazma seviyeleri yaklaşık 20 dakika içinde pik yapar ve oral uygulamadan sonra seviyeler yaklaşık 30 dakika içinde pik yapar. Morfin öncelikle karaciğerde metabolize olur ve bir doz morfinin yaklaşık %87'si uygulamadan sonraki 72 saat içinde idrarla atılır. Morfin, faz II metabolizma enzimi UDP-glukuronozil transferaz-2B7 (UGT2B7) tarafından glukuronidasyon yoluyla öncelikle morfin-3-glukuronid (M3G) ve morfin-6-glukuronide (M6G) metabolize edilir. Morfinin yaklaşık %60'ı M3G'ye ve %6 ila %10'u M6G'ye dönüştürülür. Metabolizma sadece karaciğerde gerçekleşmekle kalmaz, aynı zamanda beyin ve böbreklerde de gerçekleşebilir. M3G opioid reseptörüne bağlanmaz ve analjezik etkisi yoktur. M6G μ-reseptörlerine bağlanır ve insanlarda morfinin yarısı kadar güçlü bir analjeziktir. Morfin ayrıca az miktarda normorfin, kodein ve hidromorfona metabolize olabilir. Metabolizma hızı cinsiyet, yaş, diyet, genetik yapı, hastalık durumu (varsa) ve diğer ilaçların kullanımına göre belirlenir. Morfinin eliminasyon yarı ömrü yaklaşık 120 dakikadır, ancak erkekler ve kadınlar arasında küçük farklılıklar olabilir. Morfin yağda depolanabilir ve bu nedenle ölümden sonra bile tespit edilebilir. Morfin kan-beyin bariyerini geçebilir, ancak zayıf lipid çözünürlüğü, protein bağlanması, glukuronik asit ile hızlı konjugasyon ve iyonizasyon nedeniyle kolayca geçemez. Morfinden türetilen eroin, kan-beyin bariyerini daha kolay geçerek daha güçlü hale gelir. ⓘ
Uzatılmış salım
Ağızdan alınan morfinin etkisi daha uzun süren ve günde bir kez verilebilen uzatılmış salımlı formülasyonları vardır. Bu morfin formülasyonlarının marka isimleri Avinza, Kadian, MS Contin ve Dolcontin'dir. Sürekli ağrılar için, 24 saatte bir (Kadian için) veya iki kez (MS Contin için) verilen uzatılmış salımlı morfinin rahatlatıcı etkisi, hemen salımlı (veya "normal") morfinin birden fazla uygulamasıyla aşağı yukarı aynıdır. Uzatılmış salımlı morfin, atak ağrısı durumunda gerektiğinde, her biri genellikle 24 saatlik uzatılmış salımlı dozun %5 ila %15'inden oluşan, hemen salımlı morfin "kurtarma dozları" ile birlikte uygulanabilir. ⓘ
Vücut sıvılarında tespit
Morfin ve başlıca metabolitleri olan morfin-3-glukuronid ve morfin-6-glukuronid bir immünoassay kullanılarak kan, plazma, saç ve idrarda tespit edilebilir. Bu maddelerin her birini ayrı ayrı test etmek için kromatografi kullanılabilir. Bazı test prosedürleri metabolik ürünleri immünoassayden önce morfine hidrolize eder, bu da ayrı ayrı yayınlanan sonuçlardaki morfin seviyelerini karşılaştırırken dikkate alınmalıdır. Morfin ayrıca katı faz ekstraksiyonu (SPE) ile tam kan örneklerinden izole edilebilir ve sıvı kromatografi-kütle spektrometresi (LC-MS) kullanılarak tespit edilebilir. ⓘ
Kodein veya haşhaş tohumu içeren yiyeceklerin yutulması yanlış pozitif sonuçlara neden olabilir. ⓘ
1999 yılında yapılan bir inceleme, nispeten düşük dozlardaki eroinin (hemen morfine metabolize olur) kullanımdan sonra 1-1,5 gün boyunca standart idrar testleriyle tespit edilebileceğini tahmin etmektedir. 2009 yılında yapılan bir incelemede, analit morfin ve tespit sınırı 1 ng/ml olduğunda, 20 mg intravenöz (IV) morfin dozunun 12-24 saat boyunca tespit edilebilir olduğu belirlenmiştir. Tespit sınırının 0,6 ng/ml olması da benzer sonuçlar vermiştir. ⓘ
Doğal oluşum

Morfin, Papaver somniferum haşhaşının olgunlaşmamış tohum saplarının derinlemesine çizilmesiyle elde edilen kurutulmuş lateks olan afyonda bulunan en bol opiattır. Morfin genellikle afyonun kuru ağırlığının %8-14'ü kadardır, ancak özel olarak yetiştirilmiş çeşitler %26'ya ulaşır veya hiç morfin üretmez (%1'in altında, belki de %0,04'e kadar). Afyon haşhaşının 'Przemko' ve 'Norman' çeşitleri de dahil olmak üzere son çeşitleri, oksikodon ve etorfin gibi yarı sentetik ve sentetik opioidlerin ve diğer bazı ilaç türlerinin üretiminde kullanılan diğer iki alkaloid olan thebaine ve oripavine üretmek için kullanılır. P. bracteatum morfin veya kodein ya da diğer narkotik fenantren tipi alkaloidler içermez. Bu tür daha ziyade bir tebain kaynağıdır. Morfinin diğer Papaverales ve Papaveraceae türlerinin yanı sıra bazı şerbetçiotu ve dut ağacı türlerinde de bulunduğu doğrulanmamıştır. Morfin en çok bitkinin yaşam döngüsünün erken dönemlerinde üretilir. Ekstraksiyon için optimum noktadan sonra, bitkideki çeşitli işlemler kodein, tebain ve bazı durumlarda ihmal edilebilir miktarlarda hidromorfon, dihidromorfin, dihidrokodein, tetrahidro-tebain ve hidrokodon üretir (bu bileşikler daha ziyade tebain ve oripavinden sentezlenir). ⓘ
Memelilerin beyninde, morfin eser miktarda sabit durum konsantrasyonlarında tespit edilebilir. İnsan vücudu ayrıca nöropeptid olarak işlev gören ve morfine benzer etkileri olan kimyasal olarak ilişkili endojen opioid peptidler olan endorfinleri de üretir. ⓘ
İnsan biyosentezi
Morfin, insanlarda beyaz kan hücreleri de dahil olmak üzere çeşitli insan hücreleri tarafından sentezlenebilen ve bu hücrelerden salınabilen endojen bir opioiddir. Bir sitokrom P450 izoenzimi olan CYP2D6, insanlarda morfinin biyosentetik yolu boyunca kodeinden morfin ve tiraminden dopamin biyosentezini katalize eder. İnsanlarda morfin biyosentetik yolu aşağıdaki gibi gerçekleşir:
L-tirozin → para-tiramin veya L-DOPA → dopamin → (S)-norlaudanosolin → (S)-retikülin → 1,2-dehidroretinülinyum → (R)-retikülin → salutaridin → salutaridinol → thebaine → neopinone → codeinone → kodein → morfin
(S)-Norlaudanosoline (tetrahidropapaveroline olarak da bilinir), L-DOPA ve dopaminin bir metaboliti olan 3,4-dihidroksifenilasetaldehitten (DOPAL) de sentezlenebilir. Parkinson hastalığının tedavisi için L-DOPA alan bireylerde endojen kodein ve morfinin idrar konsantrasyonlarının önemli ölçüde arttığı bulunmuştur. ⓘ
Afyon haşhaşında biyosentez
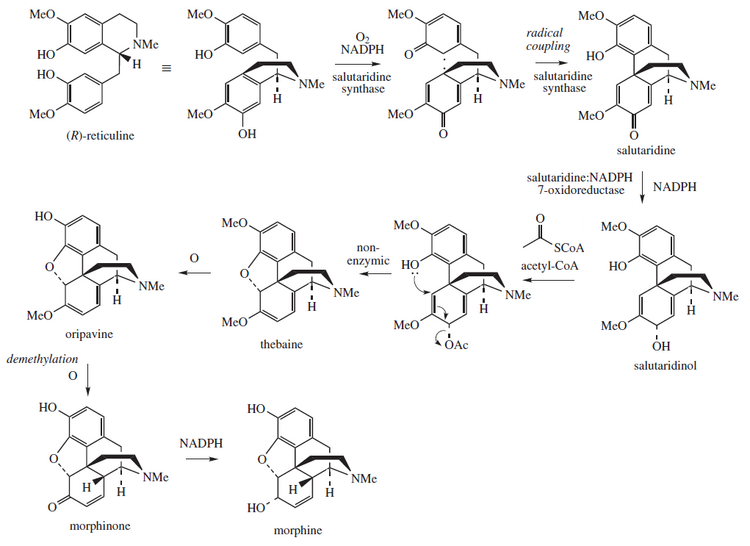
Morfin, afyon haşhaşında tetrahidroizokinolin retikülinden biyosentezlenir. Salutaridin, thebaine ve oripavine dönüştürülür. Bu süreçte yer alan enzimler salutaridin sentaz, salutaridin:NADPH 7-oksidoredüktaz ve kodeinon redüktazdır. Araştırmacılar genetiği değiştirilmiş mayada morfin üreten biyosentetik yolu yeniden üretmeye çalışıyorlar. Haziran 2015'te S-retikülin şekerden üretilebildi ve R-retikülin morfine dönüştürülebildi, ancak ara reaksiyon gerçekleştirilemedi. Ağustos 2015'te mayada tebain ve hidrokodonun ilk tam sentezi rapor edildi, ancak sürecin ticari kullanıma uygun olması için 100.000 kat daha üretken olması gerekiyor. ⓘ
Kimya
Morfin yapısının unsurları, morfinan ailesi (levorfanol, dekstrometorfan ve diğerleri) ve morfin benzeri niteliklere sahip birçok üyesi olan diğer gruplar gibi tamamen sentetik ilaçlar oluşturmak için kullanılmıştır. Morfinin ve yukarıda bahsedilen sentetiklerin modifikasyonu, emetikler, uyarıcılar, antitüsifler, antikolinerjikler, kas gevşeticiler, lokal anestezikler, genel anestezikler ve diğerleri gibi diğer kullanım alanlarına sahip narkotik olmayan ilaçların da ortaya çıkmasına neden olmuştur. Morfin türevi agonist-antagonist ilaçlar da geliştirilmiştir. ⓘ
Yapı tanımı



Morfin, iki ek halka kapanışına sahip bir benzilizokinolin alkaloididir. Auburn Üniversitesi, Harrison Eczacılık Fakültesi, İlaç Keşif ve Geliştirme Bölümü'nden (eski adıyla Farmasötik Bilimler) Jack DeRuiter'in 2000 yılı Güz dönemi ders notlarında belirttiği gibi, "Morfin molekülünün incelenmesi, farmakolojik profili açısından önemli olan aşağıdaki yapısal özellikleri ortaya koymaktadır...
- Bir benzen halkası (A), iki kısmen doymamış siklohekzan halkası (B ve C), bir piperidin halkası (D) ve bir tetrahidrofuran halkasından (E) oluşan sert bir pentasiklik yapı. A, B ve C halkaları fenantren halka sistemidir. Bu halka sistemi çok az konformasyonel esnekliğe sahiptir...
- İki hidroksil fonksiyonel grubu: bir C3-fenolik [hidroksil grubu] (pKa 9.9) ve bir C6-allilik [hidroksil grubu],
- C4 ve C5 arasında bir eter bağlantısı,
- C7 ve C8 arasında doymamışlık,
- Pozisyon 17'de bir bazik, [tersiyer]-amin fonksiyonu, [ve]
- [Beş] kiralite merkezi (C5, C6, C9, C13 ve C14) ile morfin analjezik etkide yüksek derecede stereoseçicilik sergilemektedir." ⓘ
Morfin ve türevlerinin çoğu optik izomerizm göstermez, ancak morfinan serisi (levorfanol, dekstorfan ve rasemik ana kimyasal rasemorfan) gibi bazı daha uzak akrabalar gösterir ve yukarıda belirtildiği gibi in vivo stereoseçicilik önemli bir konudur. ⓘ
Morfin, morfinan halka sistemine sahiptir. Yapısında bir fenol bir de alkol hidroksili ihtiva eder. Bir veya üç mol su ile beraber kristallenir. 110 °C'de kristal suyunu kaybeder ve 230 °C'de erir. Renksiz kristal haldedir. Soğuk suda 1/5000, sıcak suda 1/500, soğuk alkolde %3,5, sıcak alkolde ise %8 oranında çözünür. Morfinin yapısındaki 5,6,9,13 ve 14 numaralı karbonlar asimetriktir. Doğal olarak elde edilen morfin optikçe aktiftir ve polarize ışığı sola çevirir. Mutlak alkoldeki %1'lik çözeltisinin çevirme açısı; [α]D = -134,9o'dir. ⓘ
Kullanım alanları ve türevleri
Üretilen ruhsatlı morfinin çoğu metilasyon yoluyla kodein yapımında kullanılmaktadır. Aynı zamanda eroin (3,6-diasetilmorfin), hidromorfon (dihidromorfinon) ve oksimorfon (14-hidroksidihidromorfinon) dahil olmak üzere birçok uyuşturucunun öncüsüdür. Morfin ve kodein alt gruplarının her ikisi de yarı sentetik opioidlerin çoğu, aşağıdakilerden bir veya daha fazlasının modifiye edilmesiyle oluşturulur:
- Morfin karbon iskeleti üzerindeki 1. veya 2. pozisyonlarda halojenleme veya başka modifikasyonlar.
- Morfini kodeine dönüştüren metil grubu çıkarılabilir veya geri eklenebilir veya morfin türevi ilaçların kodein analoglarını yapmak için etil ve diğerleri gibi başka bir fonksiyonel grupla değiştirilebilir veya bunun tersi yapılabilir. Morfin bazlı ilaçların kodein analogları genellikle kodein ve morfin, hidrokodon ve hidromorfon, oksikodon ve oksimorfon, nikokodein ve nikomorfin, dihidrokodein ve dihidromorfin vb. gibi daha güçlü ilacın ön ilaçları olarak hizmet eder.
- Fonksiyonel grupların bu pozisyonlara eklenmesi, çıkarılması veya değiştirilmesinin yanı sıra 7 ve 8 pozisyonları arasındaki bağın doyurulması, açılması veya diğer değişiklikler; 7-8 bağının doyurulması, azaltılması, ortadan kaldırılması veya başka şekilde değiştirilmesi ve 14'e bir fonksiyonel grup eklenmesi hidromorfinol verir; hidroksil grubunun bir karbonile oksidasyonu ve 7-8 bağının çiftten teke değiştirilmesi kodeini oksikodona dönüştürür.
- Fonksiyonel grupların 3. veya 6. pozisyonlara eklenmesi, çıkarılması veya değiştirilmesi (dihidrokodein ve ilgili, hidrokodon, nikomorfin); metil fonksiyonel grubunun 3. pozisyondan 6. pozisyona taşınması durumunda, kodein 72 kat daha güçlü olan heterokodein haline gelir ve bu nedenle morfinden altı kat daha güçlüdür
- Fonksiyonel grupların eklenmesi veya 14. pozisyonda diğer modifikasyonlar (oksimorfon, oksikodon, nalokson)
- Genellikle morfin iskeletinin başka yerlerinde molekülde yapılan diğer değişikliklerle birlikte 2, 4, 5 veya 17. pozisyonlarda yapılan modifikasyonlar. Bu genellikle katalitik indirgeme, hidrojenasyon, oksidasyon veya benzeri yöntemlerle üretilen ilaçlarla yapılır ve morfin ve kodeinin güçlü türevleri üretilir. ⓘ
Birçok morfin türevi, başlangıç malzemesi olarak thebaine veya codeine kullanılarak da üretilebilir. Morfinin N-metil grubunun bir N-feniletil grubu ile değiştirilmesi, opiat agonist gücü açısından morfinden 18 kat daha güçlü bir ürünle sonuçlanır. Bu modifikasyonun 6-hidroksilin 6-metilen grubuyla değiştirilmesiyle birleştirilmesi, morfinden yaklaşık 1.443 kat daha güçlü bir bileşik üretir ve bazı ölçütlere göre etorfin (M99, Immobilon sakinleştirici dart) gibi Bentley bileşiklerinden daha güçlüdür. Morfinle yakından ilişkili olan opioidler, artık yaygın kullanımda olmayan bir ilaç olan morfin-N-oksit (genomorfin) ve afyonda bulunan bir alkaloid olan psödomorfin, morfinin bozunma ürünleri olarak oluşur. ⓘ
Bu molekülün kapsamlı bir şekilde incelenmesi ve kullanılması sonucunda, 19. yüzyılın son çeyreğinden bu yana 250'den fazla morfin türevi (kodein ve ilgili ilaçlar da dahil) geliştirilmiştir. Bu ilaçlar, kodeinin analjezik gücünün %25'inden (veya morfinin gücünün %2'sinden biraz fazlası) morfinin birkaç bin katına, nalokson (Narcan), naltrekson (Trexan), diprenorfin (M5050, Immobilon dart için tersine çevirici ajan) ve nalorfin (Nalline) gibi güçlü opioid antagonistlerine kadar çeşitlilik göstermektedir. Bazı opioid agonist-antagonistleri, kısmi agonistler ve ters agonistler de morfinden türetilmiştir. Yarı-sentetik morfin türevlerinin reseptör-aktivasyon profili büyük farklılıklar gösterir ve apomorfin gibi bazıları narkotik etkilerden yoksundur. ⓘ
Tuzlar
Hem morfin hem de hidratlı formu suda çok az çözünür. Bu nedenle ilaç firmaları ilacın sülfat ve hidroklorür tuzlarını üretmektedir; bunların her ikisi de ana moleküllerinden 300 kat daha fazla suda çözünür. Doymuş bir morfin hidrat çözeltisinin pH değeri 8,5 iken, tuzlar asidiktir. Güçlü bir asitten ancak zayıf bir bazdan türedikleri için, her ikisi de yaklaşık pH = 5'tir; sonuç olarak, morfin tuzları enjeksiyona uygun hale getirmek için az miktarda NaOH ile karıştırılır. ⓘ
Morfinin bir dizi tuzu kullanılmaktadır; mevcut klinik kullanımda en yaygın olanları hidroklorür, sülfat, tartarat ve sitrattır; daha az yaygın olarak metobromür, hidrobromür, hidroiodür, laktat, klorür ve bitartrat ve aşağıda listelenen diğerleri. Morfin diasetat (eroin) bir tuz değil, daha ziyade başka bir türevdir, yukarıya bakınız. ⓘ
Morfin mekonat, morfin pektinat, nitrat, sülfat ve diğerleri gibi haşhaştaki alkaloidin önemli bir formudur. Kodein, dihidrokodein ve diğer (özellikle eski) opiyatlar gibi, morfin de bazı tedarikçiler tarafından salisilat tuzu olarak kullanılmıştır ve hem opioid hem de NSAID'nin terapötik avantajını sağlayarak kolayca birleştirilebilir; morfinin çoklu barbitürat tuzları da geçmişte morfin valerat gibi kullanılmıştır, asidin tuzu kediotunun aktif prensibidir. Kalsiyum morfenat, morfin üretiminin çeşitli lateks ve haşhaş-saman yöntemlerinde ara maddedir, daha nadiren sodyum morfenat yerini alır. Morfin askorbat ve tannat, sitrat ve asetat, fosfat, valerat ve diğerleri gibi diğer tuzlar, hazırlama yöntemine bağlı olarak haşhaş çayında mevcut olabilir. ⓘ
Birleşik Devletler Uyuşturucuyla Mücadele İdaresi tarafından raporlama amacıyla listelenen tuzlar, birkaç diğerine ek olarak, aşağıdaki gibidir:
| Kontrollü Maddeler Yasası (CSA) çizelgesi, İdari Kontrollü Maddeler Kod Numarası (ACSCN) ve serbest baz dönüşüm oranı ile birlikte morfinin seçilmiş tuzları. ⓘ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
Üretim

Afyon haşhaşında alkaloidler mekonik aside bağlıdır. Yöntem, ezilmiş bitkiden, mekonik asitten daha güçlü bir asit olan, ancak alkaloid molekülleriyle reaksiyona girecek kadar güçlü olmayan seyreltilmiş sülfürik asit ile ekstrakte etmektir. Ekstraksiyon birçok adımda gerçekleştirilir (bir miktar ezilmiş bitki en az altı ila on kez ekstrakte edilir, bu nedenle pratik olarak her alkaloid çözeltiye girer). Son ekstraksiyon adımında elde edilen çözeltiden alkaloidler ya amonyum hidroksit ya da sodyum karbonat ile çökeltilir. Son adım morfinin saflaştırılması ve diğer afyon alkaloidlerinden ayrılmasıdır. Buna benzer bir Gregory süreci İkinci Dünya Savaşı sırasında Birleşik Krallık'ta geliştirilmiş olup, çoğu durumda kökler ve yapraklar hariç tüm bitkinin sade veya hafif asitli suda haşlanmasıyla başlamakta, ardından konsantrasyon, ekstraksiyon ve alkaloidlerin saflaştırılması aşamalarından geçmektedir. Diğer "haşhaş samanı" işleme yöntemleri (yani kurutulmuş bakla ve saplar) buhar, çeşitli alkol türlerinden biri veya daha fazlası veya diğer organik çözücüler kullanır. ⓘ
Haşhaş samanı yöntemleri Kıta Avrupası ve İngiliz Milletler Topluluğu'nda baskındır ve lateks yöntemi en yaygın olarak Hindistan'da kullanılmaktadır. Lateks yöntemi, olgunlaşmamış baklaların, bu amaç için özel olarak geliştirilmiş bir koruyucuya sahip iki ila beş ağızlı bir bıçakla milimetrenin bir kesri kadar derinliğe kadar dikey veya yatay olarak dilimlenmesini içerebilir ve baklaların çizilmesi beş defaya kadar yapılabilir. Geçmişte Çin'de bazen kullanılan alternatif bir lateks yöntemi de haşhaş başlarını kesmek, içlerinden büyük bir iğne geçirmek ve 24 ila 48 saat sonra kurumuş lateksi toplamaktır. ⓘ
Hindistan'da, lisanslı haşhaş çiftçileri tarafından hasat edilen afyon, devlet işleme merkezlerinde tek tip hidrasyon seviyelerine kadar kurutulmakta ve daha sonra afyondan morfin çıkaran ilaç şirketlerine satılmaktadır. Ancak Türkiye ve Tazmanya'da morfin, haşhaş samanı olarak adlandırılan saplarıyla birlikte tamamen olgunlaşmış kuru tohum kabuklarının hasat edilmesi ve işlenmesiyle elde edilmektedir. Türkiye'de su ekstraksiyon işlemi kullanılırken, Tazmanya'da solvent ekstraksiyon işlemi kullanılmaktadır. ⓘ
Afyon haşhaşı en az 50 farklı alkaloid içerir, ancak bunların çoğu çok düşük konsantrasyondadır. Morfin ham afyondaki başlıca alkaloiddir ve kuru ağırlık olarak afyonun yaklaşık %8-19'unu oluşturur (yetiştirme koşullarına bağlı olarak). Amaca yönelik olarak geliştirilmiş bazı haşhaş türleri artık ağırlıkça %26'ya kadar morfin içeren afyon üretmektedir. Toz haline getirilmiş kurutulmuş haşhaş samanının morfin içeriğini belirlemek için kaba bir kural, lateks yöntemiyle tür veya ürün için beklenen yüzdeyi sekize veya ampirik olarak belirlenen bir faktöre bölmektir; bu genellikle 5 ila 15 arasındadır. Yine Tazmanya'da geliştirilen P. Somniferum'un Norman türü %0,04'e kadar morfin üretir, ancak çok daha yüksek miktarlarda thebaine ve oripavine ile yarı sentetik opioidlerin yanı sıra uyarıcılar, emetikler, opioid antagonistleri, antikolinerjikler ve düz kas ajanları gibi diğer ilaçların sentezlenmesinde kullanılabilir. ⓘ
Macaristan 1950'li ve 1960'lı yıllarda Avrupa'nın toplam ilaç amaçlı morfin üretiminin yaklaşık %60'ını karşılamıştır. Günümüzde Macaristan'da haşhaş tarımı yasaldır, ancak haşhaş tarlaları kanunen 2 dönüm (8.100 m2) ile sınırlandırılmıştır. Çiçek aranjmanlarında kullanılmak üzere çiçekçilerde kurutulmuş haşhaş satmak da yasaldır. ⓘ
1973'te Amerika Birleşik Devletleri'ndeki Ulusal Sağlık Enstitüleri'nde bir ekibin başlangıç malzemesi olarak kömür katranı kullanarak morfin, kodein ve tebainin toplam sentezi için bir yöntem geliştirdiği duyuruldu. Kodein-hidrokodon sınıfı öksürük kesicilerde (bunların hepsi bir ya da daha fazla adımda morfinden yapılabildiği gibi kodein ya da tebainden de yapılabilir) yaşanan kıtlık araştırmanın ilk nedeniydi. ⓘ
Dünya çapında farmasötik kullanım için üretilen morfinin çoğu aslında kodeine dönüştürülmektedir, çünkü kodeinin hem ham afyon hem de haşhaş samanındaki konsantrasyonu morfininkinden çok daha düşüktür; çoğu ülkede kodein kullanımı (hem son ürün hem de öncü olarak) ağırlık bazında en az morfininkine eşit veya daha fazladır. ⓘ
Kimyasal sentez
Marshall D. Gates, Jr. tarafından 1952 yılında geliştirilen ilk morfin total sentezi, total sentezin yaygın olarak kullanılan bir örneği olmaya devam etmektedir. Özellikle Rice, Evans, Fuchs, Parker, Overman, Mulzer-Trauner, White, Taber, Trost, Fukuyama, Guillou ve Stork araştırma grupları tarafından başka sentezler de rapor edilmiştir. Bu polisiklik yapının stereokimyasal karmaşıklığı ve bunun sonucunda ortaya çıkan sentetik zorluk nedeniyle Michael Freemantle, kimyasal bir sentezin afyon haşhaşından morfin üretme maliyetiyle rekabet edebilecek şekilde uygun maliyetli olmasının "pek olası olmadığı" görüşünü dile getirmiştir. ⓘ
Diğer opioidlerin öncüsü
Farmasötik
Morfin, dihidromorfin, hidromorfon, hidrokodon ve oksikodon gibi bir dizi opioidin yanı sıra kendisi de geniş bir yarı sentetik türev ailesine sahip olan kodeinin üretiminde bir öncüdür. ⓘ
Yasadışı
Yasadışı morfin nadiren de olsa reçetesiz satılan öksürük ve ağrı kesici ilaçlarda bulunan kodeinden üretilmektedir. Bir diğer yasadışı kaynak ise uzun salınımlı morfin ürünlerinden elde edilen morfindir. Kimyasal reaksiyonlar morfin, dihidromorfin ve hidrokodonu eroin veya diğer opioidlere dönüştürmek için kullanılabilir [örneğin, diasetildihidromorfin (Paralaudin) ve pastırma]. Diğer gizli dönüşümler - morfinin hidromorfon sınıfı ketonlara veya dihidromorfin (Paramorfan), desomorfin (Permonid), metopon gibi diğer türevlere ve kodeinin hidrokodon (Dicodid), dihidrokodein (Paracodin) vb. maddelere dönüştürülmesi - daha fazla uzmanlık ve tedarik edilmesi daha zor kimyasal ve ekipman türleri ve miktarları gerektirir ve bu nedenle yasadışı olarak daha nadir kullanılır (ancak vakalar kaydedilmiştir). ⓘ
Tarihçe

Afyon bazlı bir iksir Bizans dönemindeki simyacılara atfedilmiştir, ancak spesifik formül Konstantinopolis'in (İstanbul) Osmanlılar tarafından fethi sırasında kaybolmuştur. 1522 civarında Paracelsus, Latince "övmek" anlamına gelen laudāre kelimesinden laudanum adını verdiği afyon bazlı bir iksire atıfta bulunmuş ve bunu güçlü bir ağrı kesici olarak tanımlamış, ancak az kullanılmasını tavsiye etmiştir. Verilen tarif günümüz laudanumundan büyük ölçüde farklıdır. ⓘ
Morfin, haşhaş bitkisinden elde edilen ilk aktif alkaloid olarak Aralık 1804'te Paderborn'da Alman eczacı Friedrich Sertürner tarafından keşfedilmiştir. Sertürner 1817'de kendisine, üç genç çocuğa, üç köpeğe ve bir fareye morfin verdiği deneyleri rapor etti; dört kişi de neredeyse ölüyordu. Sertürner, uykuya yol açma eğilimi nedeniyle morfiyum maddesine Yunan rüya tanrısı Morpheus'un adını vermiştir. Sertürner'in morfiyumu afyondan altı kat daha güçlüydü. İlacın daha düşük dozlarına ihtiyaç duyulduğu için daha az bağımlılık yapacağını varsaydı. Ancak Sertürner ilaca bağımlı hale geldi ve "Felaketin önlenebilmesi için morfiyum adını verdiğim bu yeni maddenin korkunç etkilerine dikkat çekmeyi görevim olarak görüyorum" uyarısında bulundu. ⓘ
İlaç ilk olarak 1817 yılında Sertürner and Company tarafından ağrı kesici olarak ve ayrıca afyon ve alkol bağımlılığının tedavisi için halka pazarlanmıştır. Zehir olarak ilk kez 1822 yılında Fransız Dr. Edme Castaing'in bir hastasını öldürmekten mahkum edilmesiyle kullanılmıştır. Ticari üretim 1827'de Almanya'nın Darmstadt kentinde, Merck ilaç şirketine dönüşen eczane tarafından başladı ve morfin satışları ilk büyümelerinin büyük bir bölümünü oluşturdu. 1850'lerde Alexander Wood, karısı Rebecca'ya bir deney olarak morfin enjekte ettiğini bildirdi; efsaneye göre bu, solunum depresyonu nedeniyle onu öldürdü, ancak kocasından on yıl daha uzun yaşadı. ⓘ
Daha sonra morfinin alkol ya da afyondan daha fazla bağımlılık yaptığı anlaşılmış ve Amerikan İç Savaşı sırasında yaygın kullanımının 400.000'den fazla kişinin morfin bağımlılığı "asker hastalığı "na yakalanmasına yol açtığı iddia edilmiştir. Böyle bir hastalığın aslında uydurma olduğuna dair öneriler olduğu için bu fikir tartışma konusu olmuştur; "asker hastalığı" ifadesinin belgelenmiş ilk kullanımı 1915'te olmuştur. ⓘ
Diasetilmorfin (daha çok eroin olarak bilinir) 1874 yılında morfinden sentezlenmiş ve 1898 yılında Bayer tarafından piyasaya sürülmüştür. Eroin, ağırlık olarak morfinden yaklaşık 1,5 ila 2 kat daha güçlüdür. Diasetilmorfinin lipid çözünürlüğü nedeniyle, kan-beyin bariyerini morfinden daha hızlı geçebilir ve daha sonra bağımlılığın takviye edici bileşenini artırabilir. Bir çalışmada, çeşitli öznel ve nesnel ölçütler kullanılarak, eroinin bağımlılık sonrası hastalara damardan verilen morfine göre göreceli etkisinin 1 mg diamorfin hidroklorüre (eroin) karşılık 1,80-2,66 mg morfin sülfat olduğu tahmin edilmiştir. ⓘ

Morfin, 1914 tarihli Harrison Narkotik Vergi Yasası kapsamında ABD'de kontrollü bir madde haline gelmiştir ve ABD'de reçetesiz bulundurmak suçtur. Morfin, eroin sentezlenip kullanıma girene kadar dünyada en yaygın olarak kötüye kullanılan narkotik analjezikti. Genel olarak, dihidromorfin sentezine kadar (yak. 1900), opioidlerin dihidromorfinon sınıfı (1920'ler) ve oksikodon (1916) ve benzeri ilaçların sentezine kadar, afyon, morfin ve eroin ile aynı etkinlik aralığında başka ilaç yoktu, Sentetikler henüz birkaç yıl uzaktayken (pethidine 1937'de Almanya'da icat edilmiştir) ve yarı sentetikler arasında opioid agonistleri, dihidrokodein (Paracodin), etilmorfin (Dionine) ve benzilmorfin (Peronine) gibi kodein analogları ve türevleriydi. Bugün bile, eroin kıt olduğunda, diğer her şey eşit olduğunda, eroin bağımlıları tarafından en çok aranan reçeteli narkotik morfindir; yerel koşullar ve kullanıcı tercihi, hidromorfon, oksimorfon, yüksek doz oksikodon veya metadonun yanı sıra 1970'lerin Avustralya'sı gibi belirli durumlarda dekstromoramidin bu özel listenin başında yer almasına neden olabilir. Mutlak sayı olarak en fazla eroin bağımlısı tarafından kullanılan durdurucu ilaç muhtemelen kodeindir ve dihidrokodein, haşhaş kapsülü ve haşhaş tohumu çayı gibi haşhaş samanı türevleri, propoksifen ve tramadol de önemli ölçüde kullanılmaktadır. ⓘ
Morfinin yapısal formülü 1925 yılında Robert Robinson tarafından belirlenmiştir. Kömür katranı ve petrol damıtıkları gibi başlangıç maddelerinden morfinin tamamen sentezlenmesine yönelik en az üç yöntemin patenti alınmış olup, bunlardan ilki 1952 yılında Rochester Üniversitesi'nde Dr. Marshall D. Gates, Jr. tarafından duyurulmuştur. Yine de morfinin büyük çoğunluğu haşhaştan ya haşhaşın çentikli, olgunlaşmamış kabuklarından geleneksel lateks toplama yöntemiyle ya da en yaygın olanı 1925 yılında Macaristan'da icat edilen ve 1930 yılında Macar farmakolog János Kabay tarafından duyurulan haşhaş samanı, bitkinin kurutulmuş kabukları ve saplarının kullanıldığı işlemlerle elde edilmektedir. ⓘ
2003 yılında insan vücudunda doğal olarak bulunan endojen morfin keşfedilmiştir. Bu konuda otuz yıl boyunca spekülasyonlar yapıldı çünkü sadece morfine tepki veren bir reseptör olduğu ortaya çıktı: insan dokusundaki μ3-opioid reseptörü. Kanserli nöroblastom hücrelerine tepki olarak oluşan insan hücrelerinin eser miktarda endojen morfin içerdiği bulunmuştur. ⓘ
Toplum ve kültür
Yasal statü
- Avustralya'da morfin, çeşitli başlıklara sahip Eyalet ve Bölge Zehirler Yasaları kapsamında Çizelge 8 uyuşturucu olarak sınıflandırılmıştır.
- Kanada'da morfin, Kontrollü İlaçlar ve Maddeler Yasası kapsamında Çizelge I ilacı olarak sınıflandırılmıştır.
- Fransa'da morfin, Aralık 1970 Fransız Kontrollü Maddeler Yasası'na dayanan en katı kontrollü maddeler çizelgesinde yer almaktadır.
- Almanya'da morfin, Betäubungsmittelgesetz'in Anlage III (CSA Çizelge II'nin eşdeğeri) altında listelenen bir verkehrsfähiges und verschreibungsfähiges Betäubungsmittel'dir.
- İsviçre'de morfin, Almanya'nın ilaca ilişkin yasal sınıflandırmasına benzer şekilde sınıflandırılmıştır.
- Japonya'da morfin, Narkotik ve Psikotropik Kontrol Yasası (麻薬及び向精神薬取締法, mayaku oyobi kōseishinyaku torishimarihō) kapsamında narkotik olarak sınıflandırılmıştır.
- Hollanda'da morfin, Afyon Kanunu kapsamında Liste 1 uyuşturucusu olarak sınıflandırılmıştır.
- Yeni Zelanda'da morfin, 1975 tarihli Uyuşturucuların Kötüye Kullanımı Yasası kapsamında B Sınıfı uyuşturucu olarak sınıflandırılmıştır.
- Birleşik Krallık'ta morfin, 1971 tarihli Uyuşturucuların Kötüye Kullanımı Yasası kapsamında A Sınıfı bir uyuşturucu ve 2001 tarihli Uyuşturucuların Kötüye Kullanımı Yönetmeliği kapsamında 2. Kontrollü İlaç olarak listelenmiştir.
- Amerika Birleşik Devletleri'nde morfin, Kontrollü Maddeler Yasası kapsamında 9300 numaralı ana İdari Kontrollü Maddeler Kodu altında Çizelge II kontrollü madde olarak sınıflandırılmıştır. Morfin ilaçları yıllık üretim kotalarına tabidir; 2017 yılında bu kotalar satış için 35,0 ton üretim ve diğer ilaçlara dönüştürülmek üzere ara ürün veya kimyasal öncü olarak 27,3 ton üretim şeklindeydi. Aşırı seyreltik formülasyonlarda kullanılmak üzere üretilen morfin, üretim kotasının dışında tutulmaktadır.
- Uluslararası alanda (BM) morfin, Narkotik Uyuşturucular Tek Sözleşmesi kapsamında I sayılı cetvelde yer alan bir uyuşturucudur. ⓘ
Tıbbi olmayan kullanım

Opioidler de dahil olmak üzere narkotik ilaçların sağladığı öfori, sıkıntının ve dolayısıyla acının tüm yönlerinin kapsamlı bir şekilde hafifletilmesi, sosyalliğin ve empatinin teşvik edilmesi, "vücudun yüksek olması" ve anksiyoliz, uzun bir süre boyunca ağrı yokluğunda yüksek dozların kullanılmasına neden olabilir ve bu da kullanıcıda ilaca karşı hastalıklı bir özlem uyandırabilir. Tüm opioid ilaç sınıfının prototipi olan morfin, kötüye kullanımına yol açabilecek özelliklere sahiptir. Morfin bağımlılığı, mevcut bağımlılık algısının dayandığı modeldir. ⓘ
Hayvanlar ve insanlar üzerinde yapılan çalışmalar ve klinik deneyimler morfinin bilinen en öforik ilaçlardan biri olduğu ve eroin ile morfinin IV yol hariç diğer yollarla ayırt edilemediği, çünkü eroinin sistemik morfin iletimi için bir ön ilaç olduğu iddiasını desteklemektedir. Morfin molekülündeki kimyasal değişiklikler dihidromorfin, hidromorfon (Dilaudid, Hydal) ve oksimorfon (Numorphan, Opana) gibi diğer öforijeniklerin yanı sıra son üçünün metillenmiş eşdeğerleri olan sırasıyla dihidrokodein, hidrokodon ve oksikodonu da ortaya çıkarmaktadır; eroine ek olarak dipropanoylmorfin, diasetildihidromorfin ve nikomorfin gibi 3,6 morfin diester kategorisinin diğer üyeleri ve desomorfin, hidromorfinol vb. gibi diğer benzer yarı sentetik opiatlar da bulunmaktadır. Dünyanın birçok ülkesinde klinik olarak kullanılmakla birlikte nadiren yasadışı olarak da üretilmektedir. ⓘ
Genel olarak, morfinin tıbbi olmayan kullanımı, reçetelenenden daha fazla veya tıbbi gözetim dışında alınmasını, oral formülasyonların enjekte edilmesini, alkol, kokain ve benzerleri gibi onaylanmamış güçlendiricilerle karıştırılmasını veya tabletleri çiğneyerek veya burundan çekmek veya enjektabl hazırlamak için toz haline getirerek uzatılmış salım mekanizmasını yenmeyi gerektirir. Bu son yöntem, geleneksel afyon içme yöntemleri kadar zaman alıcı ve karmaşık olabilir. Bu ve karaciğerin ilk geçişte uyuşturucunun büyük bir yüzdesini yok etmesi gerçeği, gizli yeniden satıcılar için denklemin talep tarafını etkilemektedir, çünkü birçok müşteri iğne kullanıcısı değildir ve uyuşturucuyu ağızdan almaktan hayal kırıklığına uğramış olabilir. Morfini saptırmak çoğu durumda oksikodon kadar zor ya da daha zor olduğundan, sokakta herhangi bir formda morfin nadirdir, ancak morfin enjeksiyon ampulleri ve flakonları, saf farmasötik morfin tozu ve çözünebilir çok amaçlı tabletler mevcut olduğu yerlerde çok popülerdir. ⓘ
Morfin aynı zamanda eroin üretiminde kullanılan, kendi başına içilebilen ya da çözünebilir bir tuz haline getirilip enjekte edilebilen bir macun halinde de mevcuttur; aynı şey Kompot (Polonya Eroini) ve siyah katran işlemlerinin sondan bir önceki ürünleri için de geçerlidir. Afyonun yanı sıra haşhaş samanı da tek başına ya da 50'den fazla diğer alkaloidle birlikte haşhaş çayından neredeyse farmasötik sınıf morfine kadar değişen saflık seviyelerinde morfin verebilir. Aynı zamanda afyon ve tüm formları, türevleri ve analoglarının aktif narkotik bileşenidir ve eroinin parçalanmasından oluşur ve eksik asetilasyonun bir sonucu olarak birçok yasadışı eroin partisinde bulunur. ⓘ
İsimler
Morfin dünyanın çeşitli yerlerinde birçok farklı marka adı altında pazarlanmaktadır. Eskiden İngiliz İngilizcesinde Morphia olarak adlandırılırdı. ⓘ
Morfinin gayri resmi isimleri şunlardır: Cube Juice, Dope, Dreamer, Emsel, First Line, God's Drug, Hard Stuff, Hocus, Hows, Lydia, Lydic, M, Miss Emma, Mister Blue, Monkey, Morf, Morph, Morphide, Morphie, Morpho, Mother, MS, Ms. Emma, Mud, New Jack Swing (eroinle karıştırılırsa), Sister, Tab, Unkie, Unkie White ve Stuff. ⓘ
MS Contin tabletleri misties, 100 mg uzatılmış salımlı tabletler ise greys ve blockbusters olarak bilinir. "Speedball" kokain, amfetamin, metilfenidat veya benzer ilaçlarla kombine edilen opioid bileşen olarak morfin kullanabilir. "Blue Velvet" morfinin antihistaminik tripelennamin (Pyrabenzamine, PBZ, Pelamine) ile enjeksiyon yoluyla alınan bir kombinasyonudur veya daha az yaygın olarak karışım yutulduğunda veya retansiyon lavmanı olarak kullanıldığında; bu ismin aynı zamanda tripelennamin ve dihidrokodein veya ağızdan alınan kodein tabletleri veya şuruplarının bir kombinasyonunu ifade ettiği de bilinmektedir. "Morphia" morfin için kullanılan eski bir resmi terimdir ve argo bir terim olarak da kullanılmaktadır. "Driving Miss Emma" morfinin damardan uygulanmasıdır. Çok amaçlı tabletler (yutulabilen veya dil altında ya da yanak ve çene arasında çözülebilen kolayca çözünebilen hipodermik tabletler), bazı hidromorfon markaları gibi, Shake & Bake veya Shake & Shoot olarak bilinir. ⓘ
Morfin, özellikle diasetilmorfin (eroin) içilebilir, en yaygın yöntem "Ejderhanın Peşinde" yöntemidir. Kullanımdan hemen önce morfini eroine ve ilgili uyuşturuculara dönüştürmek için asetilasyon yapmak AAing (Asetik Anhidrit için) veya home-bake olarak bilinir ve prosedürün çıktısı da home-bake veya Blue Heroin (Blue Magic eroin veya Blue Morphine veya Blue Morphone olarak bilinen linctus veya yukarıda açıklanan Blue Velvet karışımı ile karıştırılmamalıdır) olarak bilinir. ⓘ
Gelişmekte olan ülkelerde erişim
Morfin ucuz olmasına rağmen, yoksul ülkelerdeki insanlar genellikle morfine erişememektedir. Uluslararası Narkotik Kontrol Kurulu tarafından 2005 yılında yapılan bir tahmine göre, altı ülke (Avustralya, Kanada, Fransa, Almanya, Birleşik Krallık ve Amerika Birleşik Devletleri) dünyadaki morfinin %79'unu tüketmektedir. Dünya nüfusunun %80'ini oluşturan daha az varlıklı ülkeler ise küresel morfin arzının yalnızca %6'sını tüketmektedir. Bazı ülkeler neredeyse hiç morfin ithal etmemekte, bazılarında ise bu ilaç ölüm sırasında şiddetli ağrıları dindirmek için bile nadiren temin edilebilmektedir. ⓘ
Ağrı yönetimi uzmanları, morfinin yetersiz dağıtımını, ilacın bağımlılık ve kötüye kullanım potansiyeline ilişkin yersiz bir korkuya bağlamaktadır. Morfin açıkça bağımlılık yapıcı olsa da, Batılı doktorlar ilacı kullanmanın ve tedavi sona erdiğinde hastayı bırakmanın faydalı olduğuna inanmaktadır. ⓘ
Farmakolojik özellikleri
Diğer opiatlar gibi, örneğin eroin, morfin direkt merkezi sinir sistemine etkir ve analjezik etki ortaya çıkar. Eczacılıkta klorhidratı veya sülfatı halinde ağrı dindirici olarak kullanılır. Genellikle %1'lik çözeltisi halinde kullanılır. Cilt altına 10–20mg enjekte edildiğinde ağrı duygusunu hemen kaldırır. Morfin ağızdan alınırsa etkisi tam olmaz. Çünkü mide ve bağırsakta tam absorbe olmaz. İyi bir ağrı kesicidir. Ancak bağımlılık yapma sakıncası vardır. Mecbur kalınmadıkça kullanılmaz. ⓘ
- 9.8mg / ml 'lik ampul formu için; ⓘ
Uyarılar
Morfin narkotik bir ilaçtır ve tekrarlayan uygulamalarda fiziksel bağımlılık, psişik bağımlılık ve tolerans gelişir. Uzun süreli kullanımlardan sonra ilacın aniden kesilmesi yoksunluk sendromuna neden olur. Yaşlı hastalarda, hepatik ve/veya renal fonksiyon bozukluğu olan hastalarda, hipotiroidizmde veya surrenal yetmezlikte, şokta, uretroprostatik hastalık nedeniyle üriner retansiyon riski olan hastalarda dikkatle kullanılmalı, gerekirse dozaj azaltılmalıdır. Morfin, plasenta bariyerini hızla aşar. Doğumun 2. safhasında (serviks dilatasyonu 4–5cm) veya prematüre doğumlarda, yenidoğan infantta sekonder respiratuvar depresyon riskinden dolayı kullanılmamalıdır. Anne morfin bağımlısıysa, yenidoğan infantta konvülziyonlar, irritabilite, koma, letaliteyle seyredebilen yokluk sendromuna neden olabilir. Yan etki ortaya çıkması halinde veya kullanan vakanın hamile olduğunun anlaşılması gibi durumlarda ilaç derhal kesilmelidir. Diğer bütün narkotik analjeziklerde olduğu gibi yaşlılarda, böbrek ve kronik karaciğer yetmezliği vakalarında doz azaltılarak verilmelidir. Paralitik ileus şüphesi olan vakalarda uygulanmamalıdır veya tedavi sırasında paralitik ileus oluştuğundan şüphelenirse derhal tedavi kesilmeli ve gerekli destekleyici tedbirler alınmalıdır. Sedatif etkisi nedeniyle araba kullanma veya beceri isteyen makine kullanma yeteneğinde önemli azalmalara yol açabilir. Bunun yanı sıra alkol veya diğer santral sinir sistemi depresanı özelliklere sahip ilaçlarla birlikte uygulama bu depresan etkisinin şiddetlenmesine yol açar. ⓘ
İlaç etkileşimleri
MAO inhibitörleriyle tedaviye ara verdikten sonra en az 15 gün içinde narkotik analjezikler kullanılmamalıdır. Pethidinle birlikte kullanım sonucu ciddi veya fatal olaylar gözlenmiştir. Bu tür reaksiyonların diğer santral analjeziklerle oluşup oluşmadığı bilinmemektedir. SSS depresanları ve trisiklik antidepresanlar morfinle birlikte kullanıldıklarında morfinin etkisini ve aşırı dozaj riskini artırırlar. ⓘ

