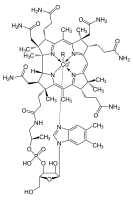
Kobalt
 | |||||||||||||||||||||||||||||||
| Kobalt | |||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Telaffuz | /ˈkoʊbɒlt/ ( | ||||||||||||||||||||||||||||||
| Görünüş | sert parlak mavimsi gri metal | ||||||||||||||||||||||||||||||
| Standart atom ağırlığı Ar°(Co) |
| ||||||||||||||||||||||||||||||
| Periyodik tabloda kobalt | |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| Atom numarası (Z) | 27 | ||||||||||||||||||||||||||||||
| Grup | Grup 9 | ||||||||||||||||||||||||||||||
| Dönem | dönem 4 | ||||||||||||||||||||||||||||||
| Blok | d-blok | ||||||||||||||||||||||||||||||
| Elektron konfigürasyonu | [[[Argon|Ar]]] 3d7 4s2 | ||||||||||||||||||||||||||||||
| Kabuk başına elektron | 2, 8, 15, 2 | ||||||||||||||||||||||||||||||
| Fiziksel özellikler | |||||||||||||||||||||||||||||||
| STP'de Faz | katı | ||||||||||||||||||||||||||||||
| Erime noktası | 1768 K (1495 °C, 2723 °F) | ||||||||||||||||||||||||||||||
| Kaynama noktası | 3200 K (2927 °C, 5301 °F) | ||||||||||||||||||||||||||||||
| Yoğunluk (r.t.'ye yakın) | 8,90 g/cm3 | ||||||||||||||||||||||||||||||
| sıvı olduğunda (m.p.'de) | 8,86 g/cm3 | ||||||||||||||||||||||||||||||
| Füzyon ısısı | 16,06 kJ/mol | ||||||||||||||||||||||||||||||
| Buharlaşma ısısı | 377 kJ/mol | ||||||||||||||||||||||||||||||
| Molar ısı kapasitesi | 24,81 J/(mol-K) | ||||||||||||||||||||||||||||||
Buhar basıncı
| |||||||||||||||||||||||||||||||
| Atomik özellikler | |||||||||||||||||||||||||||||||
| Oksidasyon durumları | -3, -1, 0, +1, +2, +3, +4, +5 (bir amfoterik oksit) | ||||||||||||||||||||||||||||||
| Elektronegatiflik | Pauling ölçeği: 1.88 | ||||||||||||||||||||||||||||||
| İyonlaşma enerjileri |
| ||||||||||||||||||||||||||||||
| Atomik yarıçap | ampi̇ri̇k: 125 pm | ||||||||||||||||||||||||||||||
| Kovalent yarıçap | Düşük dönüş: 126±3 pm Yüksek dönüş: 150±7 pm | ||||||||||||||||||||||||||||||
| Kobaltın spektral çizgileri | |||||||||||||||||||||||||||||||
| Diğer özellikler | |||||||||||||||||||||||||||||||
| Doğal oluşum | ilkel | ||||||||||||||||||||||||||||||
| Kristal yapı | altıgen yakın paketlenmiş (hcp) | ||||||||||||||||||||||||||||||
| Ses hızı ince çubuk | 4720 m/s (20 °C'de) | ||||||||||||||||||||||||||||||
| Termal genleşme | 13,0 µm/(m⋅K) (25 °C'de) | ||||||||||||||||||||||||||||||
| Termal iletkenlik | 100 W/(m⋅K) | ||||||||||||||||||||||||||||||
| Elektriksel direnç | 62,4 nΩ⋅m (20 °C'de) | ||||||||||||||||||||||||||||||
| Manyetik sıralama | ferromanyetik | ||||||||||||||||||||||||||||||
| Young modülü | 209 GPa | ||||||||||||||||||||||||||||||
| Kayma modülü | 75 GPa | ||||||||||||||||||||||||||||||
| Yığın modülü | 180 GPa | ||||||||||||||||||||||||||||||
| Poisson oranı | 0.31 | ||||||||||||||||||||||||||||||
| Mohs sertliği | 5.0 | ||||||||||||||||||||||||||||||
| Vickers sertliği | 1043 MPa | ||||||||||||||||||||||||||||||
| Brinell sertliği | 470-3000 MPa | ||||||||||||||||||||||||||||||
| CAS Numarası | 7440-48-4 | ||||||||||||||||||||||||||||||
| Tarih | |||||||||||||||||||||||||||||||
| Keşif ve ilk izolasyon | Georg Brandt (1735) | ||||||||||||||||||||||||||||||
| Kobaltın ana izotopları | |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
Kobalt, sembolü Co ve atom numarası 27 olan kimyasal bir elementtir. Nikelde olduğu gibi, kobalt da doğal meteorik demir alaşımlarında bulunan küçük birikintiler dışında, yerkabuğunda yalnızca kimyasal olarak birleştirilmiş bir biçimde bulunur. İndirgeyici eritme ile üretilen serbest element sert, parlak, gümüş grisi bir metaldir. ⓘ
Kobalt bazlı mavi pigmentler (kobalt mavisi) eski zamanlardan beri takı ve boyalarda ve cama belirgin bir mavi ton vermek için kullanılmıştır, ancak rengin uzun süre bilinen metal bizmuttan kaynaklandığı düşünülmüştür. Madenciler mavi pigment üreten bazı mineraller için uzun süre kobold cevheri (Almanca cin cevheri) adını kullanmışlardır; bilinen metaller bakımından fakir oldukları ve eritildiklerinde zehirli arsenik içeren dumanlar çıkardıkları için bu şekilde adlandırılmışlardır. 1735 yılında, bu tür cevherlerin yeni bir metale indirgenebildiği bulunmuş (antik çağlardan beri keşfedilen ilk metal) ve sonuçta bu metale kobold adı verilmiştir. ⓘ
Günümüzde bazı kobaltlar, kobaltit (CoAsS) gibi bir dizi metalik tozlu cevherden özel olarak üretilmektedir. Ancak bu element daha çok bakır ve nikel madenciliğinin bir yan ürünü olarak üretilmektedir. Demokratik Kongo Cumhuriyeti (DRC) ve Zambiya'daki Copperbelt, küresel kobalt üretiminin çoğunu sağlamaktadır. Natural Resources Canada'ya göre 2016 yılında dünya üretimi 116.000 ton (114.000 uzun ton; 128.000 kısa ton) olup, bunun %50'sinden fazlasını tek başına Kongo Demokratik Cumhuriyeti gerçekleştirmiştir. ⓘ
Kobalt öncelikle lityum-iyon pillerde ve manyetik, aşınmaya dayanıklı ve yüksek mukavemetli alaşımların üretiminde kullanılır. Kobalt silikat ve kobalt(II) alüminat (CoAl2O4, kobalt mavisi) bileşikleri cam, seramik, mürekkep, boya ve verniklere ayırt edici koyu mavi bir renk verir. Kobalt doğal olarak yalnızca bir kararlı izotop, kobalt-59 olarak bulunur. Kobalt-60, radyoaktif izleyici olarak ve yüksek enerjili gama ışınlarının üretimi için kullanılan ticari açıdan önemli bir radyoizotoptur. ⓘ
Kobalt, kobalaminler olarak adlandırılan bir grup koenzimin aktif merkezidir. Bu türün en iyi bilinen örneği olan B12 vitamini, tüm hayvanlar için gerekli bir vitamindir. İnorganik formdaki kobalt ayrıca bakteriler, algler ve mantarlar için bir mikro besin maddesidir. ⓘ
Kobalt 1773 yılında Georg Brandt tarafından keşfedilmiş metal element. Atom numarası 27, simgesi Co, atom ağırlığı ise 58.9332 g/mol'dür. ⓘ
"Kobalt" iki ya da fazla bileşenli toz metallerin yapıştırılmasında ve kesici takımlarda kullanılır. ⓘ
Co(OH)3 ısıtılarak Co2O3 oksidine dönüştürülür. Daha sonra bu oksit karbon ile indirgenerek saf kobalt elde edilir. ⓘ
Özellikleri

Kobalt, özgül ağırlığı 8,9 olan ferromanyetik bir metaldir. Curie sıcaklığı 1.115 °C (2.039 °F) ve manyetik momenti atom başına 1,6-1,7 Bohr manyetondur. Kobalt, demirin üçte ikisi oranında bağıl geçirgenliğe sahiptir. Metalik kobalt iki kristalografik yapı olarak ortaya çıkar: hcp ve fcc. hcp ve fcc yapıları arasındaki ideal geçiş sıcaklığı 450 °C'dir (842 °F), ancak pratikte aralarındaki enerji farkı o kadar küçüktür ki ikisinin rastgele iç içe geçmesi yaygındır. ⓘ
Kobalt, pasifleştirici bir oksit film tarafından oksidasyondan korunan zayıf indirgeyici bir metaldir. Halojenler ve sülfür tarafından saldırıya uğrar. Oksijen içinde ısıtıldığında Co3O4 oluşur ve 900 °C'de (1.650 °F) oksijen kaybederek CoO monoksitini verir. Metal, 520 K'de flor (F2) ile reaksiyona girerek CoF3 verir; klor (Cl2), brom (Br2) ve iyot (I2) ile reaksiyona girerek eşdeğer ikili halojenürler üretir. Isıtıldığında bile hidrojen gazı (H2) veya azot gazı (N2) ile reaksiyona girmez, ancak bor, karbon, fosfor, arsenik ve sülfür ile reaksiyona girer. Normal sıcaklıklarda mineral asitlerle yavaş, nemli havayla çok yavaş reaksiyona girer ancak kuru havayla reaksiyona girmez. ⓘ
Bileşikler
Kobaltın yaygın oksidasyon durumları arasında +2 ve +3 bulunur, ancak -3 ila +5 arasında değişen oksidasyon durumlarına sahip bileşikler de bilinmektedir. Basit bileşikler için yaygın bir oksidasyon durumu +2'dir (kobalt(II)). Bu tuzlar pembe renkli metal aquo kompleksini oluşturur [Co(H
2O)
6]2+
su içinde. Klorür ilavesi yoğun mavi [CoCl
4]2−
. Boraks boncuk alev testinde, kobalt hem oksitleyici hem de indirgeyici alevlerde koyu mavi renk gösterir. ⓘ
Oksijen ve kalkojen bileşikleri
Çeşitli kobalt oksitleri bilinmektedir. Yeşil kobalt(II) oksit (CoO) kaya tuzu yapısına sahiptir. Su ve oksijen ile kolayca kahverengi kobalt(III) hidroksite (Co(OH)3) oksitlenir. 600-700 °C sıcaklıklarda CoO, spinel yapıya sahip mavi kobalt(II,III) okside (Co3O4) oksitlenir. Siyah kobalt(III) oksit (Co2O3) de bilinmektedir. Kobalt oksitler düşük sıcaklıkta antiferromanyetiktir: CoO (Néel sıcaklığı 291 K) ve Co3O4 (Néel sıcaklığı: 40 K), +2 ve +3 oksidasyon durumlarının bir karışımı ile manyetite (Fe3O4) benzer. ⓘ
Kobaltın başlıca kalkojenitleri arasında siyah kobalt(II) sülfitler, pirit benzeri bir yapıya sahip olan CoS2 ve kobalt(III) sülfit (Co2S3) bulunur. ⓘ
Halojenürler

Kobalt(II)'nin dört dihalidi bilinmektedir: kobalt(II) florür (CoF2, pembe), kobalt(II) klorür (CoCl2, mavi), kobalt(II) bromür (CoBr2, yeşil), kobalt(II) iyodür (CoI2, mavi-siyah). Bu halojenürler susuz ve hidratlı formlarda bulunur. Susuz diklorür mavi iken, hidrat kırmızıdır. ⓘ
Co3+ reaksiyonu için indirgeme potansiyeli
+ e- → Co2+
+1,92 V'tur, klordan klorüre +1,36 V'un ötesindedir. Sonuç olarak, kobalt(III) klorür kendiliğinden kobalt(II) klorür ve klora indirgenecektir. Florun florüre indirgenme potansiyeli +2,87 V gibi çok yüksek olduğundan, kobalt(III) florür az sayıdaki basit kararlı kobalt(III) bileşiklerinden biridir. Bazı florlama reaksiyonlarında kullanılan kobalt(III) florür, su ile şiddetli reaksiyona girer. ⓘ
Koordinasyon bileşikleri
Tüm metallerde olduğu gibi, kobaltın moleküler bileşikleri ve poliatomik iyonları koordinasyon kompleksleri, yani bir veya daha fazla liganda bağlı kobalt içeren moleküller veya iyonlar olarak sınıflandırılır. Bunlar potansiyel olarak sonsuz çeşitlilikte molekül ve iyonların kombinasyonları olabilir, örneğin
- su H
2O, hekzakuokobalt(II) katyonunda olduğu gibi [Co(H
2O)
6]2+
. Bu pembe renkli kompleks, katı kobalt sülfat CoSO'da baskın katyondur.
4-(H
2O)x, x = 6 veya 7 ile ve bunların su çözeltilerinde. - amonyak NH
3, cis-diaquotetraamminecobalt(III) [Co(NH
3)
4(H
2O)
2]3+
, hekzol içinde [Co(Co(NH
3)
4(HO)
2)
3]6−
içinde [Co(NO
2)
4(NH
3)
2]−
(Erdmann tuzunun anyonu) ve [Co(NH
3)
5(CO
3)]−
. - karbonat [CO
3]2−
yeşil triskarbonatokobaltat(III) [Co(CO
3)
3]3−
Anyon. - nitrit [NO
2]−
'de olduğu gibi [Co(NO
2)
4(NH
3)
2]−
. - hidroksit [HO]-
, hekzolde olduğu gibi. - klorür [Cl]-
tetrakloridokobaltat(II) CoCl'de olduğu gibi
4]2−
. - bikarbonat [HCO
3]−
'de olduğu gibi, [Co(CO
3)
2(HCO
3)(H
2O)]3-
. - oksalat [C
2O
4]2−
trizoksalatokobaltat(III) [Co(C
2O
4)3−
3]. ⓘ
Bu bağlı gruplar, elektronegatiflik ve sertlik-yumuşaklık genel ilkelerine göre kobalt atomlarının oksidasyon durumlarının kararlılığını etkiler. Örneğin, Co3+ kompleksleri ammin ligandlarına sahip olma eğilimindedir. Fosfor azottan daha yumuşak olduğu için, fosfin ligandları daha yumuşak Co2+ ve Co+'ya sahip olma eğilimindedir, bir örnek tris(trifenilfosfin)kobalt(I) klorürdür (P(C
6H
5)
3)
3CoCl). Daha elektronegatif (ve daha sert) oksit ve florür Co4+ ve Co5+ türevlerini, örneğin sezyum hekzaflorokobaltat(IV) (Cs2CoF6) ve potasyum perkobaltatı (K3CoO4) stabilize edebilir. ⓘ
Koordinasyon kimyasında Nobel ödüllü bir öncü olan Alfred Werner, ampirik formülü [Co(NH
3)
6]3+
. Belirlenen izomerlerden biri kobalt(III) hekzammin klorürdür. Tipik bir Werner tipi kompleks olan bu koordinasyon kompleksi, altı ammin ortogonal ligand ve üç klorür karşı iyonu tarafından koordine edilen merkezi bir kobalt atomundan oluşur. Amonyak yerine şelatlayıcı etilendiamin ligandları kullanıldığında tris(etilendiamin)kobalt(III) ([Co(en)
3]3+
), optik izomerlere ayrıştırılan ilk koordinasyon komplekslerinden biridir. Kompleks, "üç kanatlı pervane "nin sağ ve sol elli formlarında bulunur. Bu kompleks ilk olarak Werner tarafından sarı-altın iğne benzeri kristaller olarak izole edilmiştir. ⓘ
Organometalik bileşikler
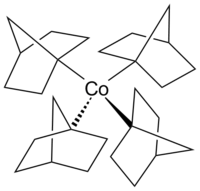
Kobaltosen, demir yerine kobalt içeren ferrosenin yapısal bir analoğudur. Kobaltosen, ferrosene göre oksidasyona karşı çok daha hassastır. Kobalt karbonil (Co2(CO)8) karbonilasyon ve hidrosililasyon reaksiyonlarında bir katalizördür. B12 vitamini (aşağıya bakınız) doğada bulunan organometalik bir bileşiktir ve metal atomu içeren tek vitamindir. Kobaltın nadir görülen +4 oksidasyon durumundaki bir alkilkobalt kompleksi örneği, Bredt kuralına uygun olarak β-hidrojen eliminasyonuna karşı direnci ile dikkat çeken bir geçiş metal-alkil kompleksi olan homoleptik kompleks tetrakis (1-norbornil) kobalt (IV) [de] (Co (1-norb) 4)'tür. Kobalt(III) ve kobalt(V) kompleksleri [Li(THF)
4]+
[Co(1-norb)
4]−
ve [Co(1-norb)
4]+
[BF
4]−
da bilinmektedir. ⓘ
İzotoplar
59Co tek kararlı kobalt izotopudur ve Dünya'da doğal olarak bulunan tek izotoptur. Yirmi iki radyoizotop karakterize edilmiştir: en kararlı olan 60Co'nun yarı ömrü 5.2714 yıldır; 57Co'nun yarı ömrü 271.8 gündür; 56Co'nun yarı ömrü 77.27 gündür; ve 58Co'nun yarı ömrü 70.86 gündür. Kobaltın diğer tüm radyoaktif izotoplarının yarı ömürleri 18 saatten ve çoğu durumda 1 saniyeden kısadır. Bu elementin ayrıca 4 meta durumu vardır ve bunların hepsinin yarı ömrü 15 dakikadan kısadır. ⓘ
Kobalt izotoplarının atom ağırlığı 50 u (50Co) ile 73 u (73Co) arasında değişir. Tek kararlı izotop olan 59Co'dan daha düşük atomik kütle birimi değerlerine sahip izotoplar için birincil bozunma modu elektron yakalamadır ve 59 atomik kütle biriminden daha büyük atomik kütleye sahip izotoplarda birincil bozunma modu beta bozunmasıdır. 59Co'nun altındaki birincil bozunma ürünleri element 26 (demir) izotoplarıdır; bunun üzerindeki bozunma ürünleri element 28 (nikel) izotoplarıdır. ⓘ
Tarih

Kobalt bileşikleri yüzyıllardır cama, sırlara ve seramiklere zengin bir mavi renk vermek için kullanılmıştır. Mısır heykellerinde, M.Ö. üçüncü binyıldan kalma Pers mücevherlerinde, M.S. 79 yılında yok edilen Pompei kalıntılarında ve Çin'de Tang hanedanlığı (M.S. 618-907) ve Ming hanedanlığı (M.S. 1368-1644) dönemlerinden kalma eserlerde kobalt tespit edilmiştir. ⓘ
Kobalt, Bronz Çağı'ndan beri camı renklendirmek için kullanılmıştır. Uluburun batığının kazısında M.Ö. 14. yüzyılda dökülmüş bir külçe mavi cam bulunmuştur. Mısır'daki mavi camlar bakır, demir ya da kobalt ile renklendirilmiştir. En eski kobalt renkli cam Mısır'ın on sekizinci hanedanlığına (MÖ 1550-1292) aittir. Mısırlıların kullandığı kobaltın kaynağı bilinmemektedir. ⓘ
Kobalt kelimesi, madenciler tarafından kobalt cevheri için kullanılan batıl bir terim olan "cin" anlamına gelen kobold'dan, Almanca kobalt'tan türetilmiştir. Bu cevherleri bakır veya gümüş için eritmeye yönelik ilk girişimler başarısız olmuş, bunun yerine sadece toz (kobalt (II) oksit) elde edilmiştir. Birincil kobalt cevherleri her zaman arsenik içerdiğinden, cevherin eritilmesi arseniği oldukça zehirli ve uçucu arsenik okside oksitleyerek cevherin kötü şöhretine katkıda bulunmuştur. ⓘ
İsveçli kimyager Georg Brandt (1694-1768) 1735 civarında kobaltı keşfederek bizmut ve diğer geleneksel metallerden farklı, daha önce bilinmeyen bir element olduğunu göstermiştir. Brandt buna yeni bir "yarı metal" adını verdi. Kobalt metali bileşiklerinin, daha önce kobaltla birlikte bulunan bizmuta atfedilen camdaki mavi rengin kaynağı olduğunu gösterdi. Kobalt, tarih öncesi dönemden bu yana keşfedilen ilk metal oldu. Bilinen diğer tüm metallerin (demir, bakır, gümüş, altın, çinko, cıva, kalay, kurşun ve bizmut) kayıtlı bir kaşifi yoktu. ⓘ
19. yüzyıl boyunca, dünyadaki kobalt mavisi (kobalt bileşikleri ve alümina ile yapılan bir pigment) ve smalt (seramik ve boyacılıkta pigment amaçlı kullanılmak üzere toz haline getirilmiş kobalt camı) üretiminin önemli bir kısmı Norveç Blaafarveværket'te gerçekleştirilmiştir. 16'ncı yüzyılda smalt üretimi için ilk madenler Norveç, İsveç, Saksonya ve Macaristan'da bulunuyordu. 1864'te Yeni Kaledonya'da kobalt cevherinin keşfedilmesiyle Avrupa'da kobalt madenciliği azaldı. 1904'te Kanada'nın Ontario eyaletinde cevher yataklarının keşfedilmesi ve 1914'te Kongo'nun Katanga eyaletinde daha da büyük yatakların bulunmasıyla madencilik faaliyetleri yeniden değişti. Shaba çatışması 1978'de başladığında Katanga Eyaletindeki bakır madenlerinde üretim neredeyse durdu. Bu çatışmanın dünya kobalt ekonomisi üzerindeki etkisi beklenenden daha az oldu: kobalt nadir bulunan bir metaldir, pigment oldukça zehirlidir ve endüstri kobalt malzemelerinin geri dönüşümü için etkili yollar geliştirmişti. Bazı durumlarda endüstri kobalt içermeyen alternatiflere geçebilmiştir. ⓘ
1938 yılında John Livingood ve Glenn T. Seaborg radyoizotop kobalt-60'ı keşfetti. Bu izotop 1950'lerde Columbia Üniversitesi'nde radyoaktif beta bozunumunda parite ihlalini belirlemek için kullanıldı. ⓘ
İkinci Dünya Savaşı'ndan sonra ABD, askeri kullanım için (Almanların yaptığı gibi) kobalt cevheri tedarikini garanti altına almak istedi ve ABD sınırları içinde kobalt aradı. Idaho'da Blackbird kanyonu yakınlarında bir dağın yamacında yeterli miktarda cevher bulundu. Calera Madencilik Şirketi bu bölgede üretime başladı. ⓘ
Kobaltın, yenilenebilir enerjiyle çalışan ve bataryalara bağımlı bir dünyada jeopolitik rekabetin ana nesnelerinden biri olacağı ileri sürülmüştür, ancak bu bakış açısı, genişletilmiş üretim için ekonomik teşviklerin gücünü hafife almakla da eleştirilmiştir. ⓘ
Oluşum
Kobaltın kararlı formu süpernovalarda r-süreci yoluyla üretilir. Dünya kabuğunun %0,0029'unu oluşturur. Serbest kobalt (doğal metal) atmosferdeki oksijen ve okyanustaki klor nedeniyle Dünya'da bulunmaz. Her ikisi de yerkabuğunun üst katmanlarında doğal metal kobaltın oluşmasını engelleyecek kadar bol miktarda bulunur. Son zamanlarda meteorik demir içinde bulunanlar dışında, doğal metal formundaki saf kobalt Dünya'da bilinmemektedir. Element orta düzeyde bir bolluğa sahiptir ancak doğal kobalt bileşikleri çok sayıdadır ve çoğu kaya, toprak, bitki ve hayvanda az miktarda kobalt bileşikleri bulunur. ⓘ
Doğada kobalt sıklıkla nikel ile ilişkilendirilir. Her ikisi de meteorik demirin karakteristik bileşenleridir, ancak kobalt demir meteoritlerde nikele göre çok daha az bulunur. Nikelde olduğu gibi, meteorik demir alaşımlarındaki kobalt, serbest (ancak alaşımlı) metal olarak kalmak için oksijen ve nemden yeterince iyi korunmuş olabilir, ancak her iki element de eski karasal kabukta bu formda görülmez. ⓘ
Bileşik halindeki kobalt bakır ve nikel minerallerinde bulunur. Sülfidik kobaltit (CoAsS), saflorit (CoAs2), glaucodot ((Co,Fe)AsS) ve skutterudit (CoAs3) minerallerinde sülfür ve arsenik ile birleşen ana metalik bileşendir. Kattierit minerali pirit ile benzerlik gösterir ve Katanga Eyaletindeki bakır yataklarında vaesit ile birlikte bulunur. Atmosfere ulaştığında ayrışma meydana gelir; sülfür mineralleri oksitlenir ve pembe eritrit ("kobalt bakışı") oluşturur: Co3(AsO4)2-8H2O) ve sferokobaltit (CoCO3) oluşturur. ⓘ
Kobalt aynı zamanda tütün dumanının da bir bileşenidir. Tütün bitkisi, çevresindeki topraktan kobalt gibi ağır metalleri kolayca emer ve yapraklarında biriktirir. Bunlar daha sonra tütün içimi sırasında solunur. ⓘ
Okyanusta
Kobalt, çoğu okyanus havzasında tespit edilen fotosentez ve azot fiksasyonunda yer alan bir eser metaldir ve fitoplankton ve siyanobakteriler için sınırlayıcı bir mikro besindir. Co içeren kompleks kobalamin sadece siyanobakteriler ve birkaç arkea tarafından sentezlenir, bu nedenle çözünmüş kobalt konsantrasyonları üst okyanusta düşüktür. Mn ve Fe gibi, Co da üst okyanusta fotosentez yoluyla fitoplankton tarafından biyolojik alım ve derin okyanusta süpürme gibi hibrit bir profile sahiptir, ancak çoğu süpürme karmaşık organik ligandlarla sınırlıdır. Co, okyanusta üst okyanusun altına batan organik maddelerin çürümesiyle geri dönüştürülür, ancak çoğu oksitleyici bakteriler tarafından temizlenir. ⓘ
Birçok okyanus kütlesi için kobalt kaynakları, hidrotermal bacalardan gelen bir miktar girdi ile nehirleri ve karasal akıntıyı içerir. Derin okyanusta, kobalt kaynakları, okyanus akıntılarının milyonlarca yıl boyunca tortuyu temizlemek için okyanus tabanını süpürdüğü ve ferromanganez kabuklar olarak oluşmalarına izin verdiği deniz dağlarının (büyük veya küçük olabilir) üstünde bulunur. Deniz tabanının sınırlı bir haritalaması yapılmış olmasına rağmen, ön araştırmalar Clarion Clipperton Bölgesinde büyük miktarda bu kobalt zengini kabukların bulunduğunu göstermektedir; bu bölge, etki alanı içindeki mineral bakımından zengin ortam nedeniyle derin deniz madenciliği girişimleri için artan bir ilgi toplamaktadır. Antropojenik girdi, doğal olmayan bir kaynak olarak ancak çok düşük miktarlarda katkıda bulunur. Okyanuslardaki çözünmüş kobalt (dCo) konsantrasyonları öncelikle çözünmüş oksijen konsantrasyonlarının düşük olduğu rezervuarlar tarafından kontrol edilir. Okyanustaki kobaltın karmaşık biyokimyasal döngüsü hala biraz yanlış anlaşılmaktadır, ancak Güney Atlantik Okyanusu'ndaki Oksijen Minimum Bölgesi (OMZ) gibi düşük oksijen alanlarında daha yüksek konsantrasyon modelleri bulunmuştur. ⓘ
Kobalt, yüksek konsantrasyonlarda deniz ortamları için toksik olarak kabul edilir. Deniz sularında diyatomlar gibi planktonlar için güvenli konsantrasyonlar 18 μg/L civarındadır. Çoğu kıyı toksisite seviyesi, kanalizasyon akışı ve fosil yakıtların yakılması gibi antropojenik girdilerden etkilenmektedir. Eser metallerin daha yüksek seviyelerde bulunduğu kıyı bölgelerinden elde edilen deniz ürünlerinde yüksek Co ve Se seviyeleri kaydedilmiştir. Bilim insanları toksisite tehdidinin farkında olsa da, kirlenmiş su sistemlerindeki cıva ve kurşun gibi diğer eser metallere kıyasla daha az dikkat edilmiştir. ⓘ
Üretim


| Ülke | Üretim | Rezervler |
|---|---|---|
| 64,000 | 3,500,000 | |
| 5,600 | 250,000 | |
| 5,000 | 1,200,000 | |
| 4,300 | 250,000 | |
| 4,200 | 500,000 | |
| 4,000 | 280,000 | |
| 3,800 | 150,000 | |
| 3,200 | 51,000 | |
| 2,900 | 270,000 | |
| 2,800 | - | |
| 2,500 | 29,000 | |
| 1,500 | ||
| 650 | 23,000 | |
| Diğer ülkeler | 5,900 | 560,000 |
| Dünya toplamı | 110,000 | 7,100,000 |
Kobaltın ana cevherleri kobaltit, eritrit, glaucodot ve skutterudittir (yukarıya bakınız), ancak kobaltın çoğu nikel ve bakır madenciliği ve eritme işlemlerinin kobalt yan ürünlerinin indirgenmesiyle elde edilir. ⓘ
Kobalt genellikle bir yan ürün olarak üretildiğinden, kobalt arzı büyük ölçüde belirli bir pazardaki bakır ve nikel madenciliğinin ekonomik fizibilitesine bağlıdır. Kobalt talebinin 2017 yılında %6 oranında artacağı tahmin edilmektedir. ⓘ
Birincil kobalt yatakları, Fas'ın Bou-Azzer bölgesinde tipik olarak görülen ultramafik kayalarla ilişkili hidrotermal yataklarda meydana gelenler gibi nadirdir. Bu tür yerlerde, kobalt cevherleri daha düşük bir konsantrasyonda olsa da özel olarak çıkarılır ve bu nedenle kobalt ekstraksiyonu için daha fazla aşağı akış işlemi gerektirir. ⓘ
Kobalt konsantrasyonuna ve kullanılan cevherin tam bileşimine bağlı olarak kobaltı bakır ve nikelden ayırmak için çeşitli yöntemler mevcuttur. Yöntemlerden biri, yüzey aktif maddelerin cevher bileşenlerine bağlanarak kobalt cevherlerinin zenginleşmesine yol açtığı köpük flotasyonudur. Daha sonraki kavurma işlemi cevherleri kobalt sülfata dönüştürür ve bakır ve demir okside oksitlenir. Su ile liç, sülfatı arsenatlarla birlikte çıkarır. Kalıntılar daha sonra sülfürik asit ile liç edilerek bakır sülfat çözeltisi elde edilir. Kobalt ayrıca bakır eritme cürufundan da süzülebilir. ⓘ
Yukarıda bahsedilen işlemlerin ürünleri kobalt okside (Co3O4) dönüştürülür. Bu oksit, alüminotermik reaksiyonla veya yüksek fırında karbonla indirgenerek metale indirgenir. ⓘ
Ekstraksiyon
Amerika Birleşik Devletleri Jeolojik Araştırmalar Kurumu dünya kobalt rezervlerinin 7.100.000 metrik ton olduğunu tahmin etmektedir. Demokratik Kongo Cumhuriyeti (DRC) şu anda dünyadaki kobaltın %63'ünü üretmektedir. Glencore Plc gibi madencilik üreticilerinin planladığı genişlemeler beklendiği gibi gerçekleşirse bu pazar payı 2025 yılına kadar %73'e ulaşabilir. Ancak Bloomberg New Energy Finance'in tahminlerine göre 2030 yılına gelindiğinde küresel talep 2017'dekinin 47 katı olabilir. ⓘ
Kongo'nun 2002 yılında madencilik yasalarında yaptığı değişiklikler Kongo bakır ve kobalt projelerine yeni yatırımlar çekmiştir. Glencore'un Mutanda Madeni 2016 yılında 24.500 ton kobalt sevkiyatı yaparak Kongo Demokratik Cumhuriyeti'nin üretiminin %40'ını ve küresel üretimin neredeyse dörtte birini karşıladı. Arz fazlasının ardından Glencore, 2019'un sonlarında Mutanda'yı iki yıllığına kapattı. Glencore'un Katanga Madencilik projesi de yeniden başlıyor ve Glencore'a göre 2019 yılına kadar 300.000 ton bakır ve 20.000 ton kobalt üretmesi bekleniyor. ⓘ


Küresel elektrikli batarya tedarik zincirinde kullanılan kobalt fiyatları, 2018'in başlarında ton başına 100.000 ABD Dolarının üzerine çıkarak on yılın en yüksek seviyelerine ulaştıktan sonra, takip eden 2 yıl içinde %45 oranında geriledi. Elektrikli (EV) araç talebinin 2020 ve 2021'de artmasıyla birlikte, kobalt fiyatları Ocak 2021'de yükselişe geçti. Mart 2021 kobalt fiyat endeksi, fiyatların aylık bazda artarak 19 Mart 2021'de ton başına 54.000 ABD dolarına ulaştığını ve 2 ayda %35'lik bir artış kaydettiğini gösteriyor. ⓘ
Kobalt, Amerika Birleşik Devletleri, Japonya, Kore Cumhuriyeti, Birleşik Krallık ve Avrupa Birliği tarafından kritik bir mineral olarak sıralanmaktadır. ⓘ
Demokratik Kongo Cumhuriyeti
2005 yılında en büyük kobalt üreticisi Demokratik Kongo Cumhuriyeti'nin Katanga Eyaletindeki bakır yataklarıydı. İngiliz Jeolojik Araştırmalar Kurumu'nun 2009 yılında bildirdiğine göre, eskiden Shaba eyaleti olan bu bölge küresel rezervlerin neredeyse %40'ına sahipti. 2015 yılı itibariyle Demokratik Kongo Cumhuriyeti (DKC) dünya kobalt üretiminin %60'ını, tonu 20.000 ila 26.000 $'dan 32.000 tonunu karşılıyordu. Üretimdeki son artış en azından kısmen Kongo Demokratik Cumhuriyeti'nin 2000'li yılların başındaki çok şiddetli iç savaşlar sırasında madencilik üretiminin ne kadar düştüğüne veya ülkenin 2002 yılında yabancı ve çok uluslu yatırımları teşvik etmek için Maden Kanunu'nda yaptığı ve Glencore da dahil olmak üzere bir dizi yatırımcıyı getiren değişikliklere bağlı olabilir. ⓘ
Artizanal madencilik, Demokratik Kongo Cumhuriyeti üretiminin %17 ila %40'ını karşılıyordu. Kongo Demokratik Cumhuriyeti'ndeki yaklaşık 100.000 kobalt madencisi, işçiler, hükümet ve STK yetkilileri ve Washington Post muhabirlerinin izole madenlere yaptıkları ziyaretlerdeki gözlemlerine göre, çok az planlama ve daha az güvenlik önlemi ile yüzlerce metre kazmak için el aletleri kullanıyor. Güvenlik önlemlerinin eksikliği sıklıkla yaralanmalara ya da ölümlere neden oluyor. Sağlık yetkililerine göre madencilik çevreyi kirletiyor ve yerel yaban hayatı ve yerli toplulukları doğum kusurlarına ve solunum güçlüklerine neden olduğu düşünülen zehirli metallere maruz bırakıyor. ⓘ
İnsan hakları aktivistleri, Afrika'daki zanaatkar madenlerinden kobalt çıkarılmasında çocuk işçi kullanıldığını iddia etmiş ve araştırmacı gazetecilik de bunu doğrulamıştır. Bu ifşaat, cep telefonu üreticisi Apple Inc. şirketini 3 Mart 2017'de Demokratik Kongo Cumhuriyeti'ndeki zanaatkar madenlerden kaynak sağlayan Zhejiang Huayou Cobalt gibi tedarikçilerden cevher alımını durdurmaya ve yalnızca işyeri standartlarını karşıladığı doğrulanan tedarikçileri kullanmaya sevk etti. ⓘ
AB ve büyük otomobil üreticileri (OEM) tarafından küresel kobalt üretiminin sürdürülebilir, sorumlu ve tedarik zincirinin izlenebilir bir şekilde tedarik edilmesi ve üretilmesi için küresel bir baskı var. Madencilik şirketleri, OECD Kılavuzuna uygun olarak ESG girişimlerini benimsemekte ve uygulamakta ve Lityum-iyon pillerin tedarik zinciri üretiminde sıfır veya düşük karbon ayak izi faaliyetlerinin kanıtlarını ortaya koymaktadır. Bu girişimler halihazırda büyük madencilik şirketleri, Artisanal ve Küçük Ölçekli Madencilik şirketleri (ASM) ile gerçekleştirilmektedir. Otomobil üreticileri ve batarya üreticisi tedarik zincirleri Tesla, VW, BMW, BASF, Glencore, Sorumlu Kobalt Girişimi ve Kalkınma için Kobalt çalışması gibi çeşitli girişimlere katılmaktadır. BMW Group, 2018 yılında BASF, Samsung SDI ve Samsung Electronics ile ortaklaşa olarak Demokratik Kongo Cumhuriyeti'nde bir pilot madende, zanaatkâr madencilerin ve çevredeki toplulukların koşullarını iyileştirmek ve zorlukları ele almak için bir pilot proje başlatmıştır. ⓘ
Bölgenin siyasi ve etnik dinamikleri geçmişte şiddet olaylarının patlak vermesine, yıllarca süren silahlı çatışmalara ve nüfusun yerinden edilmesine neden olmuştur. Bu istikrarsızlık kobalt fiyatını etkilemiş ve aynı zamanda Birinci ve İkinci Kongo Savaşlarında savaşan taraflar için çatışmaları uzatmak için ters teşvikler yaratmıştır, çünkü elmas madenlerine ve diğer değerli kaynaklara erişim, çoğu zaman soykırıma varan askeri hedeflerini finanse etmeye yardımcı olmuş ve aynı zamanda savaşçıların kendilerini zenginleştirmiştir. Kongo Demokratik Cumhuriyeti 2010'larda komşu askeri güçler tarafından yakın zamanda işgal edilmemiş olsa da, en zengin maden yataklarından bazıları Tutsiler ve Hutuların hala sık sık çatıştığı, huzursuzluğun daha küçük ölçekte de olsa devam ettiği ve mültecilerin hala şiddet olaylarından kaçtığı bölgelere bitişiktir. ⓘ
2007'de Kongo'daki küçük zanaatkar madencilik girişimlerinden çıkarılan kobalt tek bir Çinli şirkete, Kongo DongFang International Mining'e tedarik edildi. Dünyanın en büyük kobalt üreticilerinden biri olan Zhejiang Huayou Cobalt'ın bir yan kuruluşu olan Congo DongFang, Apple iPhone'lar gibi her yerde bulunan ürünler için pil üreten dünyanın en büyük pil üreticilerinden bazılarına kobalt tedarik etti. İşgücü ihlalleri ve çevresel kaygılar nedeniyle suçlanan LG Chem, daha sonra OECD yönergelerine uygun olarak Kongo DongFang'ı denetledi. Otomobil şirketleri için de batarya malzemeleri üreten LG Chem, denetlediği tüm tedarikçilerine bir davranış kuralları dayattı. ⓘ
Katanga Eyaletinde Orta Afrika Madencilik ve Keşif Şirketi (CAMEC) tarafından işletilen Mukondo Dağı projesi dünyanın en zengin kobalt rezervi olabilir. Proje 2008 yılında toplam küresel kobalt üretiminin tahminen üçte birini üretmiştir. Temmuz 2009'da CAMEC, Mukondo Dağı'ndan elde ettiği yıllık kobalt konsantresi üretiminin tamamını Çin'in Zhejiang Galico Cobalt & Nickel Materials şirketine teslim etmek üzere uzun vadeli bir anlaşma yaptığını duyurdu. ⓘ
Şubat 2018'de küresel varlık yönetimi şirketi AllianceBernstein, elektrikli araçları çalıştıran lityum-iyon piller için gerekli olan kobalt kaynakları nedeniyle DRC'yi ekonomik açıdan "elektrikli araç çağının Suudi Arabistan'ı" olarak tanımladı. ⓘ
9 Mart 2018'de Devlet Başkanı Joseph Kabila 2002 tarihli maden kanununu güncelleyerek telif ücretlerini arttırdı ve kobalt ile koltanı "stratejik metaller" olarak ilan etti. ⓘ
2002 tarihli maden kanunu 4 Aralık 2018 tarihinde etkin bir şekilde güncellenmiştir. ⓘ
Aralık 2019'da, bir insan hakları STK'sı olan International Rights Advocates, Apple, Tesla, Dell, Microsoft ve Google şirketi Alphabet'e kobalt madenciliğinde "küçük çocukların zalimce ve acımasızca kullanılmasından bilerek yararlandıkları ve bunlara yardım ve yataklık ettikleri" gerekçesiyle önemli bir dava açtı. Söz konusu şirketler çocuk işçiliğine karıştıklarını reddetti. ⓘ
Kanada
2017 yılında bazı keşif şirketleri, önemli yatakların bulunduğuna inanılan Ontario'nun Cobalt bölgesindeki eski gümüş ve kobalt madenlerini araştırmayı planlıyordu. ⓘ
Kanadalı Sherritt International, Küba'daki Moa madenlerinde bulunan nikel yataklarındaki kobalt cevherlerini işlemektedir ve adada Mayari, Camaguey ve Pinar del Rio'da başka madenler de bulunmaktadır. Sherritt International'ın Küba'da nikel ve kobalt üretimine devam eden yatırımları ve 17-20 yıl boyunca madencilik haklarını elde etmesi, komünist ülkeyi 2019 yılında kobalt rezervleri açısından Kanada'nın önünde üçüncü sıraya yerleştirdi. ⓘ
Uygulamalar
2016 yılında 116.000 ton (128.000 kısa ton) kobalt kullanılmıştır. Kobalt yüksek performanslı alaşımların üretiminde kullanılmaktadır. Ayrıca şarj edilebilir pillerin yapımında da kullanılabilmektedir ve elektrikli araçların ortaya çıkışı ve tüketiciler nezdindeki başarısı muhtemelen DRC'nin artan üretimiyle büyük ölçüde ilgilidir. Diğer önemli faktörler ise Glencore gibi yabancı ve çok uluslu şirketlerin yatırımlarını teşvik eden 2002 Maden Kanunu ile Birinci ve İkinci Kongo Savaşlarının sona ermesidir. ⓘ
Alaşımlar
Kobalt bazlı süper alaşımlar tarihsel olarak üretilen kobaltın çoğunu tüketmiştir. Bu alaşımların sıcaklık kararlılığı onları gaz türbinleri ve uçak jet motorları için türbin kanatları için uygun hale getirse de nikel bazlı tek kristalli alaşımlar performans açısından onları geride bırakmaktadır. Kobalt bazlı alaşımlar aynı zamanda korozyona ve aşınmaya dayanıklıdır, bu da onları titanyum gibi zamanla aşınmayan ortopedik implantların yapımında kullanışlı hale getirir. Aşınmaya dayanıklı kobalt alaşımlarının geliştirilmesi 20. yüzyılın ilk on yılında, değişen miktarlarda tungsten ve karbon ile krom içeren stellit alaşımları ile başlamıştır. Krom ve tungsten karbür içeren alaşımlar çok sert ve aşınmaya dayanıklıdır. Vitallium gibi özel kobalt-krom-molibden alaşımları protez parçaları (kalça ve diz protezleri) için kullanılır. Kobalt alaşımları, alerjenik olabilen nikelin yerine diş protezlerinde de kullanılmaktadır. Bazı yüksek hız çelikleri de daha fazla ısı ve aşınma direnci için kobalt içerir. Alnico olarak bilinen alüminyum, nikel, kobalt ve demir ile samaryum ve kobaltın (samaryum-kobalt mıknatıs) özel alaşımları kalıcı mıknatıslarda kullanılır. Ayrıca mücevherat için %95 platin ile alaşımlandırılarak ince döküm için uygun bir alaşım elde edilir ve bu alaşım da hafif manyetiktir. ⓘ
Piller
Lityum kobalt oksit (LiCoO2) lityum-iyon pil katotlarında yaygın olarak kullanılmaktadır. Malzeme, lityum ara katmanlı kobalt oksit katmanlarından oluşur. Deşarj sırasında (yani aktif olarak şarj edilmediğinde) lityum, lityum iyonları olarak serbest bırakılır. Nikel-kadmiyum (NiCd) ve nikel metal hidrit (NiMH) bataryalar da bataryadaki nikelin oksidasyonunu iyileştirmek için kobalt içerir. Transparency Market Research 2015 yılında küresel lityum-iyon pil pazarını 30 milyar dolar olarak tahmin etmiş ve 2024 yılına kadar 75 milyar doların üzerine çıkacağını öngörmüştür. ⓘ
2018 yılında pillerdeki kobaltın çoğu bir mobil cihazda kullanılmış olsa da, kobalt için daha yeni bir uygulama elektrikli arabalar için şarj edilebilir pillerdir. Bu sektörün kobalta olan talebi beş kat artmıştır ve bu da dünyanın daha istikrarlı bölgelerinde yeni hammaddeler bulunmasını acil hale getirmektedir. Elektrikli araçların yaygınlığı arttıkça talebin devam etmesi veya artması beklenmektedir. 2016-2017'deki keşif çalışmaları, onlarca yıl önce birçok gümüş madeninin faaliyetini durdurduğu Cobalt, Ontario çevresindeki bölgeyi de içeriyordu. Elektrikli araçlarda kullanılan kobalt 2018'in ilk yarısında %81 artarak 2019'un ilk yarısında 46,3 GWh batarya kapasitesi için 7.200 tona ulaşmıştır. Kobalt deniz dibindeki kayalarda bol miktarda bulunduğundan elektrikli arabaların geleceği derin deniz madenciliğine bağlı olabilir. ⓘ
Başta Kongo Demokratik Cumhuriyeti'nin zanaatkar madenlerinde olmak üzere kobalt madenciliğinde çocuk ve köle işçiliği defalarca rapor edildiğinden, etik bir tedarik zinciri arayan teknoloji şirketleri bu hammaddede kıtlıkla karşı karşıya kaldı ve 2015'in sonlarında 10 ABD doları olan kobalt metalinin fiyatı Ekim 2017'de dokuz yılın en yüksek seviyesine ulaşarak pound başına 30 ABD dolarını aştı. Aşırı arzın ardından fiyat 2019'da daha normal bir seviye olan 15 dolara düştü. Kongo Demokratik Cumhuriyeti'ndeki artizanal kobalt madenciliği ile ilgili sorunlara bir tepki olarak, bir dizi kobalt tedarikçisi ve müşterileri, çocuk işçi kullanımını sona erdirmeyi ve Kongo Demokratik Cumhuriyeti'ndeki kobalt madenciliği ve işleme çalışma koşullarını iyileştirmeyi amaçlayan Adil Kobalt İttifakı'nı (FCA) kurdu. FCA üyeleri arasında Zhejiang Huayou Cobalt, Sono Motors, Responsible Cobalt Initiative, Fairphone, Glencore ve Tesla, Inc. bulunmaktadır. ⓘ
Avrupa Birliği tarafından lityum-iyon pil üretiminde kobalt gerekliliklerini ortadan kaldırma olasılığı üzerine araştırmalar yürütülmektedir. Ağustos 2020 itibariyle batarya üreticileri katot kobalt içeriğini kademeli olarak 1/3'ten (NMC 111) 2/10'a (NMC 442) ve şu anda 1/10'a (NMC 811) düşürmüş ve ayrıca Tesla Model 3 gibi elektrikli otomobillerin batarya paketlerine kobalt içermeyen LFP katodu eklemiştir. Eylül 2020'de Tesla, kendi kobalt içermeyen pil hücrelerini üretme planlarını açıkladı. ⓘ
Katalizörler
Birkaç kobalt bileşiği oksidasyon katalizörüdür. Kobalt asetat, ksilenin dökme polimer polietilen tereftalatın öncüsü olan tereftalik aside dönüştürülmesinde kullanılır. Tipik katalizörler kobalt karboksilatlardır (kobalt sabunları olarak bilinir). Ayrıca boyalarda, verniklerde ve mürekkeplerde kuruyan yağların oksidasyonu yoluyla "kurutucu maddeler" olarak kullanılırlar. Aynı karboksilatlar çelik kuşaklı radyal lastiklerde çelik ve kauçuk arasındaki yapışmayı iyileştirmek için kullanılır. Ayrıca polyester reçine sistemlerinde hızlandırıcı olarak kullanılırlar. ⓘ
Kobalt bazlı katalizörler karbon monoksit içeren reaksiyonlarda kullanılır. Kobalt ayrıca karbon monoksitin sıvı yakıtlara hidrojenlenmesi için Fischer-Tropsch işleminde bir katalizördür. Alkenlerin hidroformilasyonunda katalizör olarak genellikle kobalt oktakarbonil kullanılır, ancak bunun yerini Cativa prosesi gibi daha verimli iridyum ve rodyum bazlı katalizörler alır. ⓘ
Petrolün hidrodesülfürizasyonunda kobalt ve molibdenden türetilen bir katalizör kullanılır. Bu işlem, sıvı yakıtların rafine edilmesini engelleyen sülfür safsızlıklarının petrolden temizlenmesine yardımcı olur. ⓘ
Pigmentler ve renklendirme


19. yüzyıldan önce kobalt ağırlıklı olarak pigment olarak kullanılıyordu. Orta Çağ'dan beri mavi renkli bir cam olan smalt yapımında kullanılmaktadır. Smalt, kavrulmuş mineral smaltit, kuvars ve potasyum karbonat karışımının eritilmesiyle üretilir, bu da üretimden sonra ince öğütülmüş koyu mavi bir silikat camı verir. Smalt, camı renklendirmek ve resimlerde pigment olarak yaygın bir şekilde kullanılmıştır. 1780 yılında Sven Rinman kobalt yeşilini ve 1802 yılında Louis Jacques Thénard kobalt mavisini keşfetti. Kobalt mavisi (kobalt alüminat), serulean mavisi (kobalt(II) stannat), kobalt yeşilinin çeşitli tonları (kobalt(II) oksit ve çinko oksit karışımı) ve kobalt menekşe (kobalt fosfat) gibi kobalt pigmentleri, üstün kromatik kararlılıkları nedeniyle sanatçı pigmentleri olarak kullanılmaktadır. Aureolin (kobalt sarısı) artık yerini büyük ölçüde ışığa daha dayanıklı sarı pigmentlere bırakmıştır. ⓘ
Radyoizotoplar
Kobalt-60 (Co-60 veya 60Co) bir gama ışını kaynağı olarak kullanışlıdır çünkü kobaltı nötronlarla bombardıman ederek yüksek aktiviteyle tahmin edilebilir miktarlarda üretilebilir. Enerjileri 1,17 ve 1,33 MeV olan gama ışınları üretir. ⓘ
Kobalt, harici ışın radyoterapisinde, tıbbi malzemelerin ve tıbbi atıkların sterilizasyonunda, sterilizasyon için gıdaların radyasyonla işlenmesinde (soğuk pastörizasyon), endüstriyel radyografide (örneğin kaynak bütünlüğü radyografileri), yoğunluk ölçümlerinde (örneğin beton yoğunluğu ölçümleri) ve tank dolum yüksekliği anahtarlarında kullanılır. Metal, radyasyondan korunma ile ilgili sorunlara neden olan ince bir toz üretme gibi talihsiz bir özelliğe sahiptir. Radyoterapi makinelerinden çıkan kobalt, uygun şekilde atılmadığında ciddi bir tehlike oluşturmuştur ve Kuzey Amerika'daki en kötü radyasyon kirliliği kazalarından biri 1984 yılında, kobalt-60 içeren atılmış bir radyoterapi ünitesinin Meksika'nın Juarez kentindeki bir hurdalıkta yanlışlıkla sökülmesiyle meydana gelmiştir. ⓘ
Kobalt-60'ın radyoaktif yarı ömrü 5.27 yıldır. Potansiyel kaybı, radyoterapide kaynağın periyodik olarak değiştirilmesini gerektirir ve modern radyasyon terapisinde kobalt makinelerinin yerini büyük ölçüde lineer hızlandırıcıların almasının bir nedenidir. Kobalt-57 (Co-57 veya 57Co) en sık tıbbi testlerde, B12 vitamini alımı için bir radyolabel olarak ve Schilling testi için kullanılan bir kobalt radyoizotopudur. Kobalt-57, Mössbauer spektroskopisinde bir kaynak olarak kullanılır ve X-ışını floresan cihazlarında birkaç olası kaynaktan biridir. ⓘ
Nükleer silah tasarımları kasıtlı olarak 59Co içerebilir ve bunların bir kısmı nükleer patlamada aktive olarak 60Co üretebilir. Nükleer serpinti olarak dağılan 60Co bazen kobalt bombası olarak adlandırılır. ⓘ
Diğer kullanım alanları
- Kobalt, çekici görünümü, sertliği ve oksidasyona karşı direnci nedeniyle elektrokaplamada kullanılır.
- Ayrıca porselen emayeler için temel astar kat olarak da kullanılır. ⓘ
Biyolojik rolü
Kobalt tüm hayvanların metabolizması için gereklidir. B12 vitamini olarak da bilinen kobalaminin önemli bir bileşenidir ve kobaltın ultratrace element olarak birincil biyolojik rezervuarıdır. Geviş getiren hayvanların midesindeki bakteriler, kobalt tuzlarını sadece bakteriler veya arkeler tarafından üretilebilen bir bileşik olan B12 vitaminine dönüştürür. Bu nedenle toprakta asgari düzeyde kobalt bulunması otlayan hayvanların sağlığını önemli ölçüde iyileştirir ve başka B12 vitamini kaynakları olmadığı için günde 0,20 mg/kg alım tavsiye edilir. ⓘ
Kobalamin bazlı proteinler kobaltı tutmak için korrin kullanır. Koenzim B12, reaksiyonlara katılan reaktif bir C-Co bağına sahiptir. İnsanlarda B12'nin iki tür alkil ligandı vardır: metil ve adenozil. MeB12 metil (-CH3) grubu transferlerini teşvik eder. B12'nin adenozil versiyonu, bir hidrojen atomunun iki bitişik atom arasında doğrudan aktarıldığı ve ikinci sübstitüentin, X'in, sübstitüentli bir karbon atomu, bir alkolün oksijen atomu veya bir amin olabilen, eşzamanlı olarak değiştirildiği yeniden düzenlemeleri katalize eder. Metilmalonil koenzim A mutaz (MUT) MMl-CoA'yı Su-CoA'ya dönüştürerek protein ve yağlardan enerji elde edilmesinde önemli bir adım atar. ⓘ
Diğer metaloproteinlerden (örneğin çinko ve demir) çok daha az yaygın olmasına rağmen, B12 dışında başka kobaltoproteinler de bilinmektedir. Bu proteinler arasında, insanlarda ve diğer memelilerde görülen ve B12'nin korrin halkasını kullanmayan, ancak kobaltı doğrudan bağlayan bir enzim olan metiyonin aminopeptidaz 2 bulunur. Korrin olmayan bir başka kobalt enzimi de bakterilerde nitrilleri metabolize eden bir enzim olan nitril hidratazdır. ⓘ
Kobalt eksikliği
İnsanlarda kobalt içeren B12 vitamini tüketimi tüm kobalt ihtiyacını karşılar. B12 vitamini ihtiyacını rumende yerleşik bakteriler tarafından sentezlenerek karşılayan sığır ve koyunlar için inorganik kobaltın bir işlevi vardır. 20. yüzyılın başlarında, Yeni Zelanda'nın Kuzey Adası Volkanik Platosu'nda çiftçiliğin gelişimi sırasında, sığırlar "çalı hastalığı" olarak adlandırılan durumdan muzdaripti. Volkanik toprakların sığır besin zinciri için gerekli olan kobalt tuzlarından yoksun olduğu keşfedilmiştir. 1930'larda Güney Avustralya'nın güneydoğusundaki Ninety Mile Çölü'nde koyunlarda görülen "sahil hastalığının" kobalt ve bakır elementlerinin beslenme eksikliğinden kaynaklandığı bulunmuştur. Kobalt eksikliği, hayvanın işkembesine yerleşmesi için ağızdan verilen kille karıştırılmış yoğun kobalt oksit peletleri olan "kobalt mermileri "nin geliştirilmesiyle giderilmiştir. ⓘ
Kobalt eksikliği olan koyunlar ⓘ
Sağlık sorunları
| Tehlikeler | |
|---|---|
| GHS etiketlemesi: | |
Piktogramlar
|
 
|
Sinyal kelimesi
|
Tehlike |
Tehlike bildirimleri
|
H302, H317, H319, H334, H341, H350, H360F, H412 |
Önlem ifadeleri
|
P273, P280, P301+P312, P302+P352, P305+P351+P338, P308+P313 |
| NFPA 704 (yangın elması) | |
Çözünebilir kobalt tuzları için LD50 değerinin 150 ila 500 mg/kg arasında olduğu tahmin edilmektedir. ABD'de, Mesleki Güvenlik ve Sağlık İdaresi (OSHA) işyerinde izin verilen maruz kalma sınırını (PEL) zaman ağırlıklı ortalama (TWA) 0,1 mg/m3 olarak belirlemiştir. Ulusal Mesleki Güvenlik ve Sağlık Enstitüsü (NIOSH) zaman ağırlıklı ortalama 0,05 mg/m3 tavsiye edilen maruz kalma sınırı (REL) belirlemiştir. IDLH (yaşam ve sağlık için hemen tehlikeli) değeri 20 mg/m3'tür. ⓘ
Ancak, kronik kobalt yutulması ölümcül dozdan çok daha düşük dozlarda ciddi sağlık sorunlarına neden olmuştur. 1966 yılında Kanada'da bira köpüğünü stabilize etmek için kobalt bileşiklerinin eklenmesi, bira içenlerin kardiyomiyopatisi olarak bilinen toksin kaynaklı kardiyomiyopatinin kendine özgü bir formuna yol açmıştır. ⓘ
Ayrıca, Uluslararası Kanser Araştırma Ajansı (IARC) Monograflarına göre kobalt metalinin kansere neden olduğundan şüphelenilmektedir (yani, muhtemelen kanserojen, IARC Grup 2B). ⓘ
Solunduğunda solunum problemlerine neden olur. Ayrıca dokunulduğunda cilt sorunlarına neden olur; nikel ve kromdan sonra kobalt, kontakt dermatitin önemli bir nedenidir. ⓘ